Антибіотики (властивості, застосування, взаємодія) - М.П. Черенько 1999
Хірургічна інфекція. Загальні питання
ПОНЯТТЯ, Класифікація, ЗБУДНИКИ
Людину як складову частину біоценозу оточує величезний світ мікроорганізмів, хоч багато останніх перебувають з організмом людини в мирних стосунках (Сапрофіти-коменсали) або навіть у взаємовигідних, наприклад, деякі мікроорганізми кишечнику (мутуалізм), багато з них за певних умов спричинюють його захворювання (патогенні мікроорганізми). Таких хвороб (інфекційних) дуже багато — понад 500. До групи збудників цих захворювань належить багато мікробів, вірусів, грибів та найпростіших. Найбільшу роль серед них відіграють мікроби та віруси.
Ще до відкриття мікробіологами ворожого людині світу мікробів лікарі (Frocastoro, 1478—1559; Д. Самойлович, 1744—1805, та ін.) висловлювали припущення про їх існування на підставі спостереження за епідеміями так званих морових чи повальних хвороб (чума, холера, віспа тощо), відомих ще з давніх часів. Деякі з цих хвороб, особливо холера та чума, набували характеру пандемій і зводили в могилу сотні тисяч і мільйони людей.
Лікарі здогадувались, що ці хвороби передаються від людини до людини внаслідок прямих контактів між ними (хворими і здоровими), а також через повітря, їжу та воду. Гіпотетичних істот чи носіїв хвороби називали контагіями, прилипливими міазмами (міазма — гр. забруднення). Відносно цих захворювань (зокрема, венеричних) і було введено Гуфеландом у 1841 р. термін «інфекція» (infectium), що у перекладі з латини означає зараження. Цей термін дуже влучно віддзеркалює суть явища. Пізніше, після відкриття вченими (Л. Пастер, Р. Кох, А. Ієрсен, Д. Івановський та ін.) більшості збудників як повальних хвороб, так і нагноєння ран і нагнійних захворювань, термін «інфекція» стали застосовувати щодо всіх форм патології, спричинених мікроорганізмами (бактеріями, вірусами, грибами та найпростішими). У сучасному розумінні поняття «інфекція» означає таку форму взаємодії мікро- та макроорганізмів, яка зумовлює розвиток у останнього захворювання. Для розвитку інфекції потрібні збудник її — мікроб, проникнення його в Організм та певні умови в середовищі, до якого він потрапляє. Ототожнювання інфекції із збудниками її (мікробами, вірусами тощо) не є науковим.
Серед численних видів інфекції велику групу складає так звана хірургічна. Під хірургічною інфекцією розуміють такі захворювання інфекційного генезу, які або причинно пов’язані з хірургічним (механічним) втручанням, нанесенням ран (інфекційні ускладнення ран, зокрема, нагноєння останніх та ранова токсикоінфекція), або які для свого Лікування потребують чи можуть потребувати на якомусь етапі свого перебігу механічного втручання (інфекційні захворювання, що спричинюють місцеве руйнування тканин та органів і накопичення в них токсичного гнійного ексудату та мертвих клітин — абсцес, Флегмона, карбункул, Остеомієліт, мастит, апендицит, Перитоніт тощо).
Хірургічні форми інфекції спричинюються різними збудниками, переважно мікробами — як поодинокими, так і асоціаціями з кількох мікробів, тобто ця інфекція полімікробна. Вона не має чітко визначеного інкубаційного періоду, за умови дотримання санітарно-гігієнічних умов не загрожує епідемічним поширенням. Нехірургічні інфекційні захворювання, що мають переважно циклічний характер, зумовлюються специфічним збудником (мікробом, вірусом тощо), тобто є моноінфекцією. Вони небезпечні через загальнотоксичний вплив, а не місцеве руйнування тканин (хоча багато форм інфекції іноді призводять до нього, наприклад, до перфорації стінки кишки при черевному тифі, дизентерії тощо). Циклічні інфекційні захворювання потребують спеціальних протиепідемічних заходів для обмеження їх поширення.
Хірургічна інфекція, основу якої складає гнійна інфекція, дуже поширена і часто ускладнює операційні втручання, стала малочутливою до антибіотиків. На думку вчених, вона є гальмом на шляху подальшого розвитку хірургії. Серед хворих загальних хірургічних стаціонарів пацієнти з хірургічною інфекцією складають не менше третини, а серед причин смерті в госпіталях вона посідає друге місце. Частота розвитку ранової хірургічної інфекції після оперативних втручань на внутрішніх органах складає 10—25 % і більше, що набагато перевищує рівень ускладнень інфекцією не тільки чистих, але й контамінованих ран (менше 5 %).
Поряд із збільшенням кількості випадків інфекційних ускладнень та захворювань спостерігається значна зміна профілю інфекцій — збільшення питомої ваги грамнегативної (синьогнійної палички, коліформної та ін.) та змішаної — банальної гноякової в асоціації з неклостридіальною анаеробною (бактероїдною).
Загальними причинами поширення хірургічної інфекції та зміни її профілю є такі: порушення асептичного режиму в хірургічних закладах, зокрема в операційних та перев’язочних; виникнення полірезистентних штамів патогенної мікрофлори в хірургічних відділеннях (госпіталізм); складні довготривалі оперативні втручання; зниження імунобіологічної реактивності організму через погіршення еколога на планеті; значне збільшення кількості оперованих людей похилого та старечого віку з їх численними супутніми хворобами, насамперед серцево-судинними, пухлинними, урологічними; зростання кількості хворих на Цукровий діабет та інші хвороби обміну серед оперованих; широке застосування різноманітних ецдопротезів та ксеноматеріалів; переоцінка ролі антибіотиків у профілактиці інфекції та недосконалість технології їх використання; запровадження в хірургічну практику нових оперативних втручань у широкому масштабі в короткі терміни; низький рівень технічного виконання великої кількості оперативних втручань, особливо ургентних; запровадження в лікувальну практику особливо інтенсивної терапії, моніторингового контролю та сучасних технічних засобів (ендотрахеальні трубки, канюлі, катетери різного призначення тощо).
Хірургічна інфекція класифікується на такі форми: за перебігом — на гостру та хронічну, за характером збудника інфекції — на гостру гнійну та гнильну, гостру специфічну та гостру анаеробну клостридіальну і неклостридіальну. Гостра специфічна та анаеробна клостридіальна інфекції за своїм походженням є рановими токсикоінфекціями, інші види — бактеріально-токсичними (як рановими, так і нерановими).
Хронічна інфекція поділяється на хронічну гнійну неспецифічну та хронічну специфічну.
Збудниками гострої і хронічної гнійної та гнильної інфекції є стафіло-, стрепто-, менінго-, гонококи, кишкова паличка (Esherichia coli), синьогнійна паличка, неклостридіальні анаероби—протей, бактероїди тощо.
Специфічна гостра інфекція — правець, сибірка, дифтерія ран, сказ — зумовлюються паличкою правця, сибірки, дифтерії та вірусом сказу.
Гостра анаеробна інфекція спричинюється споротворчими клостридіями: Cl. perfrinqenes, Cl. oedemotiens seu novyi, Cl. septicum, Cl. hystoliticum.
Збудниками хронічної гнійної неспецифічної інфекції є ті самі мікроби, що зумовлюють і гостру гнійну інфекцію.
Збудники хронічної специфічної інфекції — палички туберкульозу, сифілісу, гриби—актиноміцети тощо.
Детальна характеристика морфологічних, культуральних, ферментативних, токсичних та антигенних властивостей згаданих головних збудників хірургічної інфекції наводиться в спеціальній літературі. Ми вкажемо лише на деякі властивості цих збудників та шляхи їх поширення з клінічного боку.
Серед збудників найчисленнішої групи хірургічних інфекцій, тобто гнійної та гнильної, переважають грампозитивні стафіло- та стрептококи і грамнегативні — кишкова паличка, синьогнійна паличка, протей та бактероїди.
Стафілокок (Staphilococcus aureus) — один із найпоширеніших збудників гнійної інфекції. Деякі хвороби у 95— 100 % випадків спричинюються саме цим мікробом (фурункул, карбункул, мастит, остеомієліт, панарицій тощо). Два інших види стафілококів — Stahp. cpidermidis та Staph, saprophyticus — відіграють незначну роль у розвитку патологій. Це шароподібний мікроб діаметром 0,5—1,5 мкм, який належить до факультативних анаеробів, тобто може жити і в безкисневому середовищі, розташовується у вигляді неправильних скупчень (виноградних грон). Дуже поширений у природі, живе на поверхні шкіри та на предметах, у повітрі, в кишечнику.
Стафілокок — мікроб, який є дуже стійким до зовнішніх впливів у сухому середовищі (може жити 3—6 міс), при температурі 80 °С гине через 10—15 хв. Дуже чутливий до деяких засобів, особливо до брильянтового зеленого.
Стафілокок виробляє понад 25 екзотоксинів, білків та ферментів патогенності. Ці Ферменти мають протеолітичні та сахаролітичні властивості. Головні екзотоксини — гемолізини, яким властиві гемолітична, летальна і дермонекротична дія, та ентеротоксин. Продукує фібринолізин, гіалуронідазу, коагулазу (коагулює плазму) та інші ферменти патогенності. Більшість видів виробляють пенщиліназу (В-лакгамазу), яка руйнує пеніцилін.
Стафілокок володіє великою здатністю до Мутації, що через поширення антибіотикотерапії зумовило появу дуже резистентних до антибіотиків, зокрема першого покоління, штамів його. Стафілокок часто спричинює інфекцію в асоціації з іншими мікробами, особливо стрептококами та кишковою паличкою.
Стрептокок (Stieptoccus pyoqenes) — грампозитивний кок, має кулясту чи овальну форму, діаметр 0,8—1,0 мкм. У культурі розташовується парами чи ланцюгами. Факультативний анаероб, деякі форми, — анаероби. Виробляють сильні екзотоксини — гемолізин, лейкоцидин, летальний та інші токсини, а також ендотоксин. Існує дуже багато видів стрептококів — 21. Головна з них — група А. До її складу входять гемолітичний стрептокок — головний патогенний варіант, умовнопатогенний а-стрептокок. Із інших груп, зокрема із групи Д, важливе патогенне значення має фекальний стрептокок. До родини стрептококів належить також пневмокок. Ферменти патогенності стрептокока — гіалуронідаза, фібринолізин, стрептокіназа, дезоксирибонуклеаза. Перший із них підвищує проникність, другий — зумовлює лізис фібрину.
Анаеробні стрептококи — Pepto-streptococcus putridus і Panaerobius — спричинюють пуерперальний Сепсис. Виділяються з гнійних та некротичних тканин з гнильним запахом.
Стрептокок є головним збудником багатьох гнійних та негнійних інфекцій, а саме: бешихи, ангіни, скарлатини, ендокардиту, сепсису, остеомієліту, лімфангіїту, лімфаденіту, гломерулонефриту тощо. Часто він входить до складу асоціації з іншими коками, зокрема стафілококом. Головний шлях зараження — повітряно-крапельний. Імунітет після перенесення стрептококової інфекції малонапружений і нетривалий. Іноді навіть буває гіперсенсибілізація. Стрептококи стійкі як у сухому середовищі, так і в низькотемпературному. Гине (крім ентерокока) при температурі 56 °С за 30 хв.
Менінгокок (Meningococc) — грам- негативний кок, діаметр його 0,6— 0,8 мкм. Аероб і факультативний анаероб. Під час його аутолізу виділяється ендотоксин. Екзотоксинів він не виробляє. Спричинює Гнійний менінгіт. Зараження відбувається повітряно-крапельним шляхом. Джерело інфекції — бацилоносії, реконвалесценти.
Гонокок (Gonococc) — диплокок діаметром 0,6—1 мкм. Грамнегативний анаероб. Екзотоксину не виробляє. Ендотоксин виділяється у разі автолізу. Зараження відбувається статевим шляхом. Уражує слизову оболонку сечівника, шийки матки та кон’юнктиви.
Кишкова паличка (Eshelichia coli) — паличка з заокругленими кінцями завдовжки 1,5—4 мкм; грамнегативна. Живе у кишечнику людини, умовно-патогенний мікроб. Міститься в землі, воді, повітрі, на предметах. Факультативний анаероб. Продукує нейротропний екзотоксин і виділяє у разі лізису ентеротропний ендотоксин. Їй притаманні активні ферментативні властивості. Розкладає пептон, утворюючи аміни, аміак, сірководень, меркаптани, індол, скатол тощо. Ферментує Вуглеводи з утворенням кислот.
Патогенні серотипи можуть бути причиною епідемічного ентероколіту, переважно у дітей віком до трьох років. Патогенні для тварин (кролів, мишей, морських свинок). Зумовлює харчові отруєння у разі масивного забруднення продуктів чи води. Збудник шильної інфекцій — гнильної флегмони, перитоніту, ран, інфекцій сечовивідних шляхів тощо. Часто приєднується до інших видів гноєродної інфекції, входячи з ними в асоціацію. Резистентність палички невелика.
Протей (Proteus) — факультативний анаероб завдовжки 1—3 мкм. Спор не утворює. Є п’ять видів протею, головні — Proteus vulqatis та Proteus mirabilis. Умовнопатогенний. Останнім часом часто зустрічається при харчових отруєннях у дітей та гнійних процесах у дорослих (отит, цистит, ранова інфекції в асоціаціях зі стафілококом та синьогнійною паличкою).
Псевдомонас (Pseudomons aeruqinosa), або синьогнійна паличка, — грамнегативна бактерія завдовжки 1,5—3 мкм. Облігатний аероб. Ферментує глюкозу з утворенням кислоти, продукує сірководень. Зустрічається в грунті, воді, рослинах, виділяється часто з опікових поверхонь, з ран та сечівника. Спричинює місцеві та загальні гнійні процеси (отит, пієліт, цистит, інфікування ран, сепсис). Інфекції зумовлюють виснаження організму, частіше спостерігаються у дітей. Продукує антагоністичний антибіотик — піоциназу. Нестійкий до дезінфікуючих засобів. При температурі 60 °С гине за 1 год. Чутливий до поліміксину, неоміцину.
Бактероїди (Bacteroides) — грамнегативні, облігатні анаероби. Дрібні палички. Не утворюють спор, живуть у кишечнику, рідше — в сечовивідних шляхах та органах Дихання. Із 22 видів найчастіше спостерігаються В. fragliis та В. melaninoqenicus. Патогенні в асоціаціях з іншими мікробами — стафілококом, кишковою паличкою, зумовлюють гнильну Інфекцію. Чутливі до хлорамфеніколу, еритроміцину, кліндоміцину.
ЗБУДНИКИ ГОСТРОЇ СПЕЦИФІЧНОЇ ІНФЕКЦІЇ
Паличка дифтерії (родина Соrуnebacterium). Аероб чи факультативний анаероб завдовжки 1—8 мкм, на кінцях має булавоподібні потовщення (звідси назва Соrуnа — булава,
ciphter — плівка). Джерелом мікроба є хворі на дифтерію та бацилоносії. Продукує сильні екзотоксини — гістотоксини, гемолізин та дермонекротоксин. У ділянці проникнення утворюється плівка з великою кількістю бактерій. Дія токсину зумовлює некроз і дифтерійне запалення слизових оболонок. У разі всмоктування їх виникає ураження нервової системи, міокарда та паренхіматозних органів.
Паличка сибірки — Bacillus anthracis. Спричинює захворювання людей і тварин. Назва походить від епідемії захворювання у Сибіру в 1786— 1788 та 1875 рр. Це велика паличка з обрубаними та увігнутими кінцями, завдовжки 5—10 мкм. Розташовується поодиноко та попарно, а в мазку з осаду культури утворює довгі ланцюжки. Грампозитивна. Утворює спори в центрі клітини. При температурі понад 42 °С і нижче 18 °С спори не утворюються. Аероб і факультативний анаероб. Виробляє токсини — запальний та летальний, який бере участь у патогенезі інфекції, а також імуногенний (протективний). Вегетативні форми нестійкі і гинуть при температурі 80 °С через 3—5 хв. Спори гинуть у автоклаві при температурі 120 °С за 15 хв.
Джерелом інфекції для людини є хвора на сибірку тварина (м’ясо, Шкіра, шерсть, кістки, навіть тварин, що давно загинули). Інкубаційний період — 3—5 діб. Форми хвороби — шкірна, кишкова, легенева та септична. Постійний імунітет має антимікробний характер.
Паличка правцю (Clostridium tetani) — паличка завдовжки 4 — 10 мкм, що утворює кінцеві спори, які надають мікробу форми барабанної палички. Грампозитивна. Рухома. Продукує сильний екзотоксин, який складається з 2 компонентів — тетаноспазміну та тетаногемолізину. У разі орального Введення токсин інактивується і тому неотруйний. Імунітет антитоксичний. Паличка живе в кишечнику тварин і людини і з їх екскрементами потрапляє в землю, де може довго зберігатись на великій глибині (до 1 м). Особливо велику кількість містять добре угноєні землі.
Сказ (Lyssa,; rabies) спричинюється вірусом, який живе в кишечнику гризунів та хижаків. Періодичні захворювання спостерігаються після посиленого розмноження гризунів. Людина заражується при укусах й навіть облизуванні пошкодженої шкіри чи слизових оболонок хворими тваринами — собаками, лисицями, вовками. Поширюється нервами і, досягнувши спинного та головного мозку, уражує їх нейрони.
ЗБУДНИКИ ГОСТРОЇ АНАЕРОБНОЇ (ГАЗОВОЇ) ІНФЕКЦІЇ
До цієї групи збудників входять переважно 4 види клостридій. Газотворна клостридія (Cl. peifnngenes) — бактерія з заокругленими кінцями завдовжки 1—1,5 мкм. Грампозитивна, утворює капсули та спори. Анаероб. Може зустрічатись як у монокультурі, так і (переважно) в асоціаціях з іншими клостридіями, а також із стафіло-, стрептококом, кишковою паличкою. Головний токсин цієї клостридії (лецитиназа) має некротичну, нейротоксичну, гемотоксичну та летальну дію. Ферменти патогенності — гіалуронідаза, фібринолізин, колагеназа та ДНКаза. Cl. perfrmgens — найчастіший збудник анаеробної інфекції. Cl. Oedematiens (клостридія набряку) — велика бактерія завдовжки 4—20 мкм з субтермінальними спорами. Грампозитивна, рухома. Виділяє (штами А і В) летальний та некротичний токсини. а-Токсин не зумовлює гемолізу, a порушує проникність (капілярна отрута) судин і спричинює набряк тканин. ß-Токсин виробляють штами В i Д.
Він володіє некротичним та гемолітичним ефектом. Утворює індол та сірководень. Спори клостридії живуть до 25 років, не втрачаючи вірулентності. При кип’ятінні гине за 3 хв, пряме сонячне світло вбиває паличку за добу.
Cl. septicum — септична клостридія — паличка завдовжки 3—10 мкм, зустрічається в асоціації рідше, ніж дві попередні.
Cl. hystoliticum — паличка завдовжки 3—5 мкм. Грампозитивна, анаероб, споротворча. Не ферментує вуглеводи. Утворює багато сірководню. Виробляє А-токсин (летальний і некротичний), ß-токсин (колагеназа), гематоксин (протеїназа), а також е-гемолізин. Головний а-токсин. Зустрічається дуже рідко (у 2—3% хворих).
При анаеробній клостридіальній інфекції у досліджуваному матеріалі завжди з рани висівають асоціації анаеробів з іншими мікробами.
Усі види клостридій спричинюють зараження у разі потрапляння їх у рану. Як мешканці товстої кишки вони найчастіше забруднюють рани, що локалізуються на нижніх кінцівках, сідницях та промежині. Інфекція може ускладнювати також операційні рани на травному каналі, а також рани після ампутації нижньої кінцівки з приводу атеросклеротичної гангрени. Поширенню інфекції сприяють крововтрата, фізичне виснаження, переохолодження, психотравма тощо.
ШЛЯХИ ПРОНИКНЕННЯ ПАТОГЕННИХ МІКРООРГАНІЗМІВ У ОРГАНІЗМ ЛЮДИНИ ТА МЕХАНІЗМИ ЇХ АГРЕСІЇ. МЕХАНІЗМИ ЗАХИСТУ ЛЮДИНИ. Патогенез ІНФЕКЦІЇ
Шляхи проникнення мікроорганізмів у Тканини і порожнини тіла. Місце проникнення збудника інфекції в організм називають воротами інфекції. Мікрофлора, що спричиняє хірургічну інфекцію, проникає в організм різними шляхами — контактним, повітряно-крапельним та повітряно- пиловим ззовні, переважно через пошкодження шкіри та слизових оболонок, рідше — з ендогенних джерел. Порушення цілості загального покриву виникають головним чином унаслідок механічних травм (рани, садна, подряпини, укуси тощо) і фізичних — термічної (Опіки, відмороження), електричної та радіаційної, а також хімічної (опіки внаслідок дії кислот, основ, інших хімічних речовин). Механічні пошкодження можуть бути як значними за розмірами (рани різного походження, відкриті переломи тощо), так і невеликими, так званими мікротравмами, на які не завжди людина, особливо під час роботи, звертає належну увагу. Подібні до механічних мікротравм пошкодження можуть виникати внаслідок укусів та ужалення різноманітних комах — комарів, ос, бджіл, джмелів, оводів, кліщів тощо. Комахи, поряд із механічними ушкодженнями шкіри, сприяють проникненню мікрофлори та розвитку інфекції через токсичний ефект на тканини, що спричиняє місцеві зміни, зокрема судинну реакцію (крововилив, свербіння) та розчухування шкіри в місці укусу чи ужалення.
Поряд із названими штучними воротами в тканинах механічного та іншого генезу мікрофлора може, за певних умов, проникати в організм і через природні канали та протоки — травний і сечовий канали та дихальні шляхи, протоки сальних, потових, слинних, сльозових, молочних залоз та інших. Ці умови можуть бути як місцевими, так і загальними. Проникненню та розвитку мікрофлори сприяють забруднення шкіри, підвищення її пітливості, порушення прохідності анатомічних шляхів, каналів та проток і вільного виділення з них секретів унаслідок ураження їх пухлинним процесом, закриття каменем (слинним, сечовим), стороннім тілом чи конденсованим власним секретом, наприклад, закриття протоки сальної залози (камедон), дистрофічні та функціональні порушення цих органів (наприклад, атрофія миготливого епітелію бронхів у курців, яка призводить до послаблення його дренувальної функції і очищення бронхів). Лише в рідкісних випадках вхідні ворота залишаються невідомими. У цьому разі кажуть про криптогенне (kryptos — прихований, krypta — щілина) проникнення мікрофлори, чи криптогенну інфекцію. Найчастіше воротами її бувають ендогенні джерела, наприклад, лакуни в мигдаликах, яснах, зубах, рубцях, особливо в гранул омах навколо сторонніх тіл.
Загальними умовами, які мають значення для проникнення мікроорганізмів природними шляхами в організм, є порушення загального кровообігу, дихання, обміну речовин (цукровий діабет, гіпопротеїнемія, гіповітамінози тощо), недокрів’я, стан імунодефіциту та ін.
Механізм агресії збудників хірургічної інфекції не відрізняється від механізму агресії патогенної мікрофлори взагалі. Серед чинників агресії патогенних мікроорганізмів головними є їх кількість, інвазивність та вірулентність, здатність утворювати капсулу тощо. Інвазивність — здатність проникати в тканини інфікованого, точніше забрудненого, мікробами організму. Поширенню в організмі мікроорганізмів сприяють деякі ферменти та токсини з властивостями ферментів. Серед них — гіалуронідаза, яка руйнує гіалуронову кислоту (полісахарид — основну субстанцію сполучної тканини), котра чинить опір проникненню сторонніх тіл у тканини. Такий фермент утворює багато патогенних мікробів, зокрема стафілококи, анаеробні клостридії тощо.
До чинників поширення належать також такі ферменти, як фібринолізин, що притаманний багатьом збудникам гнійної інфекції, та нейроамінідаза, яку продукують багато патогенних мікробів (стрептокок, дифтерійна паличка, анаеробні клостридії тощо).
Велику роль у проникненні мікрофлори в організм відіграють їх токсини, зокрема екзотоксини (білкові речовини), які блокують захисні засоби клітин. Екзотоксини виробляють стрепто-, стафілококи, синьогнійна паличка, палички правцю і сибірки, анаеробні клостридії та ін. Інвазія мікробів, збудників деяких хірургічних інфекцій, насамперед ранових токсикоінфекцій (правець, анаеробна клостридіальна інфекція), сприяє капсулотворенню. Висока вірулентність (вірулентність — ступінь патогенності) зумовлює й високу інвазивність. Вірулентність патогенних мікробів в умовах широкого (й нерідко з порушенням схеми) застосування антибіотиків та внаслідок пасажу (від хворих до здорових) штамів мікробів у госпіталях (госпіталізм) різко підвищується, що значно збільшує імовірність проникнення мікробів у організм та можливість розвитку їх у останньому. Вірулентність мікроорганізмів часто підвищується в умовах забруднення рани чи іншого місця їх проникнення в організм асоціацією мікробів різних видів, наприклад, анаеробів і аеробів, унаслідок взаємного підсилення їх патогенних властивостей (так званий синергізм мікробів). Вірулентність багатьох видів патогенної мікрофлори пов’язана із стійкістю їх токсинів до деяких середовищ організмів (наприклад, токсини стафілококу та газотворчої клостридії не руйнуються травним соком шлунка), а також мутаціями низки мікроорганізмів, зокрема стафілококів, які супроводжуються появою в останніх ферментів, що руйнують антибіотики (бета-лактамаза).
У процесі співіснування людини з ворожим мікросвітом живих істот — мікробів, вірусів, грибів, найпростіших — сформувалася складна і доволі ефективна система захисту. Успішна боротьба з хірургічною інфекцією неможлива без розуміння цієї системи захисту людини (господаря) від агресивної дії мікробів та вірусів.
Система захисту є багатоповерхова і складається як з природжених, переважно неспецифічних, так і набутих, головним чином специфічних, засобів. Захист проти мікробів залежить від функції імунної системи.
Першим рубежем захисту, одним із найголовніших, є загальний покрив — шкіра та слизові оболонки і їх структурні елементи. У разі цілості шкіра та слизові оболонки непроникні для мікробів. Лише золотистий стафілокок може іноді проникати в волосяний мішечок та Сальні залози неушкодженої шкіри. Роль механічного бар’єру шкіри добре ілюструється на прикладі опіків, за яких пошкодження покриву призводить до розвитку інфекції. За допомогою структурних елементів покриву, залоз з наявними в них молочною, соляною, жирними та іншими кислотами, муцином та лізоцимом тощо, а також функції війочок миготливого епітелію, кашлю, чхання, виділення слизу, сечі механічно (змивання, видалення) та хімічно знезаражуються мікроорганізми, що потрапляють на поверхню тіла людини та в порожнини і канали його організму.
Якщо мікрофлора проникає, пенетрує через цей перший (шкірний та слизової оболонки) бар’єр, що буває переважно у разі його пошкодження, в дію вступає другий, Кров’яно-клітинний бар’єр, або система захисту, головними складовими якої є запалення та фагоцитоз.
Пошкодження покриву (як механічне, так і мікробне) спричинює запальну місцеву реакцію, яка головним чином опосередкована хініновою системою та іншими вазоактивними субстанціями. Вони запускають у дію гуморально-клітинну систему захисту проти інфекції. Головними складовими цієї системи захисту є гуморальні, хімічні руйнівні агенти (лізоцим, протеолітичні ферменти, система комплементу, С-реактивний та катіонні протеїни, фібриноген, інтерферон та ін.) та клітини крові і сполучної тканини — нейтрофіли (мікрофаги), система мононуклеарних фагоцитів (макрофаги) та кілери.
Хімічні агенти крові діють на збудників інфекції як безпосередньо бактерицидно та бактеріостатично, так і сприяючи фагоцитозу (опсонізація веде до хемотаксису, прилипання фагоцитів до мікробів, поглинання та переварювання останніх фагоцитами). При цьому нейтрофілам належить провідна роль у фагоцитозі гноєтворних бактерій (екстрацелюлярних паразитів). Макрофаги борються з мікробами та вірусами, що проникли в клітини і паразитують у них.
Хоч механізм знищення мікробів шляхом фагоцитозу невідомий, проте низка важливих ланцюгів його з’ясована. Злиття фагосоми з мікробом усередині мікрофага (утворення фаголізосоми) супроводжується утворенням пероксидаз та перекису водню (мієлопероксидазна система), які як самостійно, так і шляхом галогенізації (хлорування та йодування) згубно діють на поглинуту мікробну клітину. Крім цього, кисеньзалежного механізму, в фаголізосомі діють і кисень-незалежні чинники — виділяються бактерицидні та бактеріостатичні речовини — катіонні білки з протеїназною дією, гідролітичні ензими — катепсин, лізоцим, молочна кислота, лактоферин та інші субстанції. Процес, що відбувається у фаголізосомі, закінчується дегрануляцією лейкоцита, знищенням мікроба і викидом продуктів розпаду назовні.
Для реалізації захисної дії фагоцитозу та інтралейкоцитарної протимікробної системи потрібні добра перфузія тканин кров’ю та оксигенація крові.
Третю стратегічну лінію захисту утворюють специфічні механізми набутого імунітету, які вступають у дію тоді, коли патогенному мікроорганізму вдається (різними шляхами, включно з мутацією) уникнути нищівної дії попередніх ліній захисту.
Перелік захисних бар’єрів організму людини від інфекції свідчить про значний арсенал їх, вироблений у процесі еволюції, до певної міри достатній, аби знищити збудників інфекції, що потрапили в нього. Про це свідчить повсякденний клінічний досвід. Наприклад, у роки Великої Вітчизняної війни серед ран м’яких тканин, не підданих первинній хірургічній обробці, близько 20 % (всі ці рани забруднені патогенною мікрофлорою) гоїлись без нагноєння. Вражаючим є приклад залізнично-транспортних відкритих травм: у 100 % випадків вони забруднені анаеробною мікрофлорою, але анаеробна інфекція розвивається лише у 1 %. Це саме стосується гнійної інфекції м’яких тканин — за наявності на шкірі практично у всіх людей збудників цієї інфекції захворювання спостерігається лише у невеликої частини людей. Але й за наявності у людини могутньої системи захисту проти інфекції остання є однією з найчастіших форм хірургічної патології: близько 30 % хворих загальнохірургічних стаціонарів — це хворі з хірургічною інфекцією (В.І. Стручков, 1981). Американські хірурги також вказують на високу питому вагу хірургічної інфекції. Це свідчить про велику здатність інфекції долати захисні бар’єри людини. Вона виробилась у процесі взаємодії з організмом людини. Особливо небезпечної стійкості і вірулентності набувають патогенні мікроби внаслідок так званого пасажу через зараження від одного хворого до здорових, тобто госпіталізму.
Висока вірулентність притаманна таким мікроорганізмам, умови природного мешкання котрих близькі до тих, у які вони потрапили (наприклад, мікроби, які вегетують у кишечнику та ротовій порожнині людини чи тварини тощо). Вірулентність мікробів може різко підвищуватись у разі забруднення рани асоціаціями мікробів, тобто поліінфекцією, внаслідок посилення агресивних якостей одного виду за рахунок другого (синергізм мікробів).
У патогенезі хірургічної інфекції, зокрема гнійної (ранова та ін.), велике значення мають масивність мікробів та їх вірулентність. Установлено, що критичний рівень збудників гнійної інфекції, за якого можливий розвиток останньої, складає 105—106 мікробних тіл на 1 г тканини. У разі високого рівня мікробного забруднення імовірність розвитку інфекції дуже збільшується. У більшості випадків інфекція розвивається при рівні мікробів 108—1012 мікробних тіл на 1 г тканини. Незважаючи на наявність у патогенної мікрофлори засобів для подолання механізмів захисту організму, розвитку в ньому інфекційного процесу, вони не мають фатального значення. Для реалізації агресивних властивостей мікрофлори, що проникла в тканини, потрібні наявність дефектів у захисній системі організму та допоміжні різноманітні місцеві й загальні чинники.
Під час травми з пошкодженням шкіри чи слизових оболонок патогенна мікрофлора практично долає цей перший захисний бар’єр вільно. Особливо небезпечним, з огляду на можливість розвитку інфекції в організмі, є пошкодження покриву тіла з утворенням ранового каналу в порожнину судин, через який патогенні мікроби безпосередньо потрапляють у Кровообіг. Це іноді буває під час проведення лікувальних та діагностичних процедур (катетеризація та канюляція судин) з порушенням асептики. Такий прямий шлях проникнення збудників інфекції, оминаючи передні лінії захисту, за певних умов (масивність мікробної інвазії, висока вірулентність мікрофлори, підвищена чутливість організму до інфекції чи зниження у хворого імунітету) може спричинити розвиток загальної хірургічної інфекції — ангіогенного сепсису. Подібну загрозу щодо ангіогенного сепсису внаслідок надходження патогенної мікрофлори в систему кровообігу створює інфекційне ураження вен та артерій (тромбофлебіт та васкуліт), особливо у разі переходу інфекції на судини з сусідніх тканин, нерідко з деструкцією їх стінки (арозія).
Розвитку інфекції, крім уже зазначеного масивного зараження потенційно патогенними мікробами, сприяють анатомо-фізіологічні особливості тканин у ділянці вхідних воріт, насамперед зниження їх перфузії кров’ю та оксигенізації. Тканини та ділянки тіла й органи, які добре постачаються кров’ю (ГОЛОВА, м’язи, обличчя, шия, руки, Печінка, Нирка, Селезінка, Легені тощо), рідше уражуються інфекцією, ніж жирова тканина, сухожилки, кістки, суглоби тощо.
Велику роль у патогенезі інфекції відіграють місцеве Порушення кровообігу різного генезу (атеросклероз і зумовлена ним оклюзія судин, унаслідок тугого накладання бинтової пов’язки, надмірного натягу країв рани під час її зашивання та накладання великої кількості швів, застосування електрокоагуляції для гемостазу), наявність гематоми та сторонніх тіл у рані, особливо речовин, що підвищують вірулентність мікробів (земля, гній, солі кальцію, магнію, заліза та ін.).
Надзвичайну роль у розвитку інфекції, особливо ранової, відіграє наявність великої кількості ушкоджених тканин в рані, ділянці забиття, опромінення, у зоні введення лікарських речовин, зокрема гіпертонічних розчинів тощо.
Загальними умовами, що сприяють розвитку інфекції, є такі: набутий та природжений імунодефіцит, анемія, гіпопротеїнемія, гіповітаміноз, захворювання серця та судин (Гіпертонічна хвороба та атеросклероз, недостатність кровообігу тощо), ожиріння, алкоголізм, похилий вік з притаманним йому зниженням імунітету та численними супутніми хворобами — такими, як цукровий діабет, злоякісні пухлини та хвороби крові, цироз печінки, гіперкортицизм, у тому числі й пов’язаний з тривалим лікуванням деяких хвороб (Бронхіальна астма, так звані колагенози тощо), та інші порушення обміну; негігієнічний стан шкіри, погане Харчування, перевтома, переохолодження, нервове виснаження, передопераційний госпіталізм, ургентний характер операції, затримка з первинною допомогою та хірургічною обробкою рани, дуже велика тривалість операції (понад 3 год) тощо. Треба зазначити, що багато ліків, зокрема антибіотиків, знижуючи активність сапрофітної мікрофлори кишечнику та деяких інших порожнин (зокрема, ротової) послаблюють опір патогенній мікрофлорі (дисбактеріоз), зокрема грибковій (кандидози) та анаеробній (бактероїдна).
Локалізація хірургічної інфекції великою мірою визначається функціональним навантаженням ділянок тіла, яке зумовлює насамперед їх підвищену травматизацію (кисті, стопи і пальці рук та ніг тощо).
Місце початкового клінічного прояву інфекції, локалізації її називається первинним осередком інфекції. У більшості випадків він збігається з вхідними воротами, за винятком лише криптогенної, або ендогенної.
МІСЦЕВА ТА ЗАГАЛЬНА РЕАКЦІЇ НА ІНФЕКЦІЮ. Клініка ТА Діагностика
Розвиток інфекції, як ранової, так і інфекційних хірургічних захворювань, супроводжується місцевими та загальними клінічними проявами й симптомами, а також низкою змін у організмі. Місцеві ознаки зовнішніх форм інфекції — це класичні прояви запалення, а саме: почервоніння шкіри, гіперемія (rubor), набряк чи припухлість тканин (tumor), підвищення місцевої температури (color), біль (dolor) та порушення функції (functiolaesa) ураженого органа. Інфікування супроводжується гіперемією тканин по краях рани, накопиченням і виділенням з рани в початковій стадії серозного, а пізніше гнійного чи гнійно-гнильного або навіть гнійно-геморагічного ексудату. Гнійний ексудат, в якому, окрім рідини, що містить білок, яка просочується через стінку судин з крові, є велика кількість лейкоцитів та продуктів розщеплення загиблих клітин і мікробів. Запалення при нагноєних ранах або у разі хірургічних інфекційних захворювань спричинює інфільтрацію тканин ексудатом та нагромадження останнього в тканинах навколо вхідних воріт інфекції (інокуляція). Ексудат призводить до некрозу клітин у центрі осередку та їх розплавлення. Так формується в тканинах порожнина, наповнена гноєм, тобто абсцес або флегмона.
Екстравазальний ексудат навколо первинного осередку інфекції, хоч і сприяє деструкції, але за рахунок стиснення та блокування кровоносних і лімфатичних судин обмежує проникнення мікробів та поширення інфекції за його межі. Поряд із механічним обмеженням поширення мікробів та їх токсинів лейкоцити, що проникають з ексудатом до осередку, утворюють навколо нього так званий лейкоцитарний вал, що стає антибактеріальним бар’єром завдяки поглинанню лейкоцитами мікробів (фагоцитозу).
Другим бар’єром, який перешкоджає поширенню інфекції, гнійного запалення, є розростання (внаслідок гіпоксії в інфільтрованих тканинах) навколо осередку сполучнотканинної оболонки, так званої гнійної мембрани (membrana piogenica). Вона перетворює місцевий осередок інфекції на обмежену форму — абсцес або абсцедуючу флегмону.
Проте у багатьох випадках гнійної інфекції місцевих механізмів захисту з різних причин буває недостатньо (вони не встигають розвинутися внаслідок високої вірулентності мікробів чи масивності їх інвазії або через порушений імунний захист), і тоді мікроби та їх токсини поширюються по тканинах чи органах через лімфатичні та Кровоносні судини, а також контактним шляхом (per contuitatem). Контактний шлях характерний для поширення інфекції з внутрішніх органів на навколишні тканини та органи, зокрема на серозні оболонки порожнин (черевна, грудна, черепа, суглобів). Так, у разі запалення червоподібного відростка чи жовчного міхура інфекційний процес нерідко поширюється на очеревину, спричинюючи перитоніт, а запальний процес в легенях (Пневмонія, абсцес легень тощо), переходячи на плевру, ускладнюється плевритом.
Шлях поширення інфекції по продовженню спостерігається у разі інфекції в обмежених фасціальними листками тканинах та органах, в фасціальних мішках, якими у разі накопичення в них гнійного ексудату та підвищення тиску поширюється мікрофлора на далеку відстань від первинного осередку. Наприклад, при глибоких флегмонах шиї інфекція фасціальними проміжками поширюється на Середостіння, зумовлюючи медіа-стиніт. Такий тип поширення інфекції призводить до розвитку масивних («безмежних») флегмон, які без інтенсивного лікування можуть спричинити загальну інфекцію та смерть хворого. За своєчасного та енергійного лікування навіть дуже поширений інфекційний запальний процес (флегмона) може бути локалізований і ліквідований. У разі розвитку інфекції в підшкірній основі та шкірі класичні симптоми запалення добре помітні. Крім них, дуже часто спостерігаються такі ознаки, як флюктуація гнояка під час пальпації та рожеві смуги на шкірі, що йдуть від гнояка вгору — висхідний лімфангіїт, а також запальний набряк лімфатичних регіональних вузлів, рідше — ознаки запалення та тромбозу венозних судин. При гнильній та анаеробній неклостридіальній і особливо клостридіальній інфекції поряд із запальним процесом нерідко виявляють різко виражений, а іноді превалюючий, альтеративний некротичний компонент. Тканини, зокрема шкіра, підшкірна основа, фасції, м’язи на широкій площі бувають змертвілі, мають чорно-багровий або темно-сірий колір.
Якщо осередок інфекції локалізується в глибині тканин чи у внутрішніх органах, виявити його за допомогою простого фізичного дослідження буває нелегко і доводиться застосовувати допоміжні Методи дослідження як місця підозрюваної локалізації гнояка, так і загального стану людини. У цих випадках, окрім виявлення клінічних ознак, використовують допоміжні методи дослідження обміну речовин, складу крові та функціональних параметрів внутрішніх органів (печінки, нирок), вивчають гемограму (при інфекції підвищується рівень лейкоцитів, зокрема нейтрофілів, зростає кількість незрілих їх форм; збільшується ШОЕ). Визначають склад білків плазми (фібриноген, С-реактивний протеїн, катіонні білки, ІМУНОГЛОБУЛІНИ), протеолітичні ферменти (рівень їх збільшується). Проводять мікробіологічні (бактеріемія) та імунологічні дослідження крові. Для виявлення глибоких осередків використовують також різні Інструментальні методи дослідження — рентгенологічний, радіологічний, ультрасонографію, комп’ютерну томографію, ядерно-магнітний Резонанс, термографію тощо.
Загальні явища у разі розвитку інфекції різко виражені: гарячка, підвищення температури тіла від незначних, субфебрильних, до високих показників — понад 38 °С (фебрильна Температура), озноб. Останній зумовлений токсичним впливом на ЦНС, зокрема іпоталамічні центри терморегуляції. Проявами токсемії є зниження чи втрата апетиту, головний біль, слабкість, пітливість тощо. Інтоксикація спричинює також низку інших змін у організмі: тахікардію, підвищення серцевого викиду та нерідко артеріального тиску, а також підвищення основного обміну, гіпервентиляцію легень, збільшення втрат рідини, кількості лейкоцитів у крові (від 8000—10 000 до 15 000 в 1 мм і навіть більше — залежно від величини осередку та реакції організму на інфекцію), зростання числа паличко-ядерних лейкоцитів та іноді появу юних форм лейкоцитів (зсув формули білої крові вліво — збільшення кількості незрілих форм лейкоцитів нейтрофільного ряду). Інтоксикація зумовлюється як мікробними екзо- та ендотоксинами, так і продуктами запалення й деструкції тканин. Різко виражені загальні зміни в організмі хворого, спричинені місцевою гнійною хірургічною інфекцією, точніше інтоксика
цією, називаються гнійно-резорбтивною гарячкою. Поряд із інтоксикацією у деяких хворих може бути епізодична бактеріемія, але вона головним чином буває у разі поширення збудника інфекції плином крові та лімфи по всьому організму і свідчить про генералізацію інфекції, розвиток сепсису, з яким треба диференціювати гнійно-резорбтивну гарячку. Гнійно-резорбтивна гарячка швидко регресує після радикального хірургічного втручання на осередку, чого не буває при сепсисі.
Клінічний перебіг інфекції багато в чому залежить і від особливостей реакції (реактивності) організму хворого. Вона може бути адекватною стосовно обсягу осередку, тобто пропорційною до нього, проявляється як місцевими ознаками запалення, так і загальними. Така реакція носить назву нормергічної. Вона буває у більшості хворих. Але через ендогенні та екзогенні причини, зокрема екологічні впливи, реакція у частини хворих може бути як маловираженою (ііпергічною), так і надмірною (гіперергічною). Гіпергічна реакція характеризується незначними місцевими запальними змінами і майже не має загальних проявів, гіперергічна супроводжується бурхливими запальними місцевими змінами, іноді з некрозом тканин, з високою температурою тіла, інтоксикацією.
Клінічний досвід свідчить, що нормергічна реакція найбільшою мірою відповідає оптимальному стану імунітету, гіперергічна спостерігається частіше у разі недостатнього розвитку імунітету, рідше — при доброму його стані (частіше буває у людей похилого та старечого віку). Гіперергічна реакція, хоч і вважається ознакою високого рівня механізмів імунітету, але як вияв алергії, підвищеної чутливості до інфекції (часто внаслідок сенсибілізації до цієї мікрофлори), надто активної боротьби з нею (утворення токсичних комплексів антиген — антитіло тощо) також є небезпечною через можливе різке неконтрольоване порушення функцій різних органів та організму в цілому (тяжкий анафілактичний шок, набряк легенів, бронхоспазм тощо). Тому хворі з гіпергічною та гіперергічною реакцією на інфекцію потребують застосування для їх лікування імунокоректорів.
Лікування хірургічної інфекції є однією з найактуальніших і складних проблем хірургії у зв’язку з великим поширенням цієї інфекції і недостатньою ефективністю антимікробних заходів, зокрема антибіотиків. Лікування інфекції повинно бути комплексним, індивідуальним, цілеспрямованим, енергійним і своєчасним. Воно передбачає застосування хірургічних і консервативних методів. Залежно від цих чинників та характеру нозологічної форми інфекції (ранова, інфекція порожнин, інфекційні ураження внутрішніх органів тощо) терапія суттєво відрізняється як за формою (консервативна чи хірургічна), так і за змістом та обсягом. Треба враховувати вікові особливості організму хворого, вид збудника, стадію та ступінь прояву запального процесу тощо.
ЛІКУВАННЯ ХВОРИХ З ІНФЕКЦІЄЮ
Незалежно від характеру лікувальних заходів метою місцевої терапії є: а) зменшення чи ліквідація больових відчуттів; б) обмеження поширення запального процесу та деструкції тканин; в) налагодження доброго відтоку ексудату з осередку, що сприяє зменшенню інтоксикації та кількості мікрофлори в зоні інфекції; г) гальмування розвитку чи зменшення кількості мікрофлори у осередку інфекції.
У початковій стадії гнійної інфекції — серозного запалення — місцеве лікування здійснюється консервативними заходами, серед яких головним є іммобілізація ураженого органа, накладання (при зовнішній локалізації) пов’язок — примочок з 95 % етанолом, який шляхом дегідратації тканин зменшує їх набряк і біль та порушення кровообігу; опромінення осередку інфекції ультрависокої частоти променями (УВЧ) чи опромінення розфокусованим промінням лазера — таке опромінення має протизапальну дію. Якщо осередок інфекції локалізується на кінцівках, зокрема на пальцях, добрий ефект забезпечує провідникова новокаїнова блокада 0,25—0,5 % розчином новокаїну з антибіотиками за Вишневським проксимальніше від осередку на рівні незапалених тканин (біля основи пальця при підшкірних панариціях кінцевої чи середньої фаланги або на рівні дистальної частини передпліччя при початкових формах сухожильного панарицію та флегмонах кистей) або коротка новокаїнова блокада навколо осередку інфекції, але не через запалені тканини (наприклад, ретромаммарна блокада при маститі). Одночасно з такою блокадою на осередок накладають масляно-бальзамну пов’язку Вишневського. Ураженому органу створюють підвищене положення (за допомогою пов’язки чи підставки) для зменшення припливу та поліпшення відпливу крові. В останні роки повідомляється про терапевтичну ефективність постійного гальванічного струму, між електродами якого розміщують уражений орган чи все тіло (А.В. Алексеенко, В.В. Тарабанчук, 1991). Паралельно з місцевим консервативним лікуванням у більшості випадків проводять і загальну терапію протимікробними засобами — антибіотиками чи іншими препаратами (перорально або ін’єкційним шляхом у відповідних дозах та з урахуванням чутливості інфекції до антибіотика).
Треба наголосити, що лише консервативна місцева терапія здатна обірвати тільки початкові форми запалення (головним чином серозного) в м’яких тканинах (поверхневий панарицій, інфільтрат в зоні рани, мастит, еритематозна та еритематозно-бульозна бешиха тощо). Її продовжують лише тоді, коли через 12—24 год є відчутні ознаки поліпшення стану хворого, регрес місцевих симптомів. Якщо ж такого ефекту немає, але немає й погіршення, то воно може бути продовженим у деяких випадках ще максимально на добу чи дві. Якщо і після цього стан хворого не поліпшується, зокрема зберігаються біль та інші місцеві симптоми, треба вдаватись до хірургічного лікування. В початковій стадії лікування особливо важливим є своєчасне визначення необхідності в оперативному втручанні.
Хірургічне втручання є провідним у місцевому лікуванні хірургічної інфекції. Воно або використовується за неефективності консервативної терапії, розпочатої в ранній стадії розвитку інфекції, або застосовується зразу первинно за наявності уже чітко сформованого осередку гнійної інфекції. Хірургічне втручання складається частіше з широкого розтину гнояка чи абсцесу, флегмони, панарицію, маститу тощо з видаленням некротичних тканин та гною або повного вирізування осередку, видалення інфікованого органа (червоподібного відростка, жовчного міхура, яєчника тощо) чи осередку в м’яких тканинах, якщо він невеликий і анатомічні умови не лімітують об’єму втручання Рідше при інфекції з утворенням обмежених порожнин, заповнених гноєм (амебні абсцеси печінки, поверхневий абсцес, абсцес легенів піддіафрагмальний чи навіть поверхнева абсцедуюча флегмона), застосовують прокол гнояка (пункція) чи невеликий розріз з уведенням у нього дренажу для пасивного чи, частіше, активного відсмоктування гнійного ексудату з одночасним промиванням порожнини антисептиками через цей чи інший введений у порожнину дренаж з уведенням у порожнину антибіотиків (при легеневих та інших глибоких абсцесах).
Розрізування гнійного осередку є найважливішим елементом ліквідації болю, призупинення деструкції тканин, поширення інфекції та зниження інтоксикації. Цим довгий час і обмежувались. Подальше лікування гнійної рани проводилось консервативно до повного її очищення і загоєння. У кращому разі для прискорення закриття очищеної гранулюючої рани на неї накладали вторинні шви. Але такий метод має той недолік, що при цьому дуже довго триває процес загоєння рани; її дефект закривається грануляціями і лише потім поволі вкривається епітелієм.
Останнім часом хірурги перейшли на так званий активний хірургічний метод лікування гнійних ран, який деякою мірою ліквідує означений недолік та прискорює закриття ранового дефекту. Його суть полягає в тому, що гнійний фокус по можливості повністю вирізується і рана після введення в неї дренажу та промивання порожнини антисептиками закривається первинним швом (з припливно-відпливним промиванням порожнини рани). Якщо ж осередок інфекції великий і неможливо його повністю вирізати, його широко розкривають і видаляють усі просочені гноєм та некротичні тканини, інтенсивно (перманентно чи фракційно) промивають рану для прискорення очищення і після цього, з початком активного її гранулювання, закривають ранніми вторинними швами. При цьому порад із механічним втручанням та промиванням гнояка широко використовують аплікацію на осередок інфекції протеолітичних ферментів, сорбентів різного виду (дебризан — з декстранових полімерів; тканинні), обробляють його УФО, ультразвуком (гравітаційна кавітація). У аеротерапевтичних ізольованих та загальних (АТУ) камерах проводять лікування відкритим способом.
Іноді для припинення подальшого розвитку гнійної хірургічної інфекції в черевній порожнині, зокрема в очеревині чи в тканинах таза, у разі порушення цілості кишечника (поранення його чи перфорація внаслідок патологічного процесу тощо) порад із розкриттям гнійного вогнища та видаленням його джерела (перфорованої пухлиною кишки, гнійного оофаросальпінгіту тощо) виконують такі втручання, як виведення з черевної порожнини назовні проксимального кінця (після видалення ушкодженої чи ураженої петлі) кишки або накладання калостоми на сигмовидну ободову кишку у разі пошкодження прямої кишки. Цим запобігають недостатності в умовах перитоніту кишкових анастомозів, інфікуванню тканин таза при проходженні калових мас через ушкоджену пряму кишку з незашитою раною.
Хірургічне втручання при анаеробній хірургічній інфекції відрізняється від такого при гнійній інфекції. Анаеробну інфекцію первинно лікують винятково хірургічним шляхом і оперативне втручання при ній завжди має значно більший об’єм, ніж при гнійній: повне видалення осередку в межах здорових тканин, навіть якщо для цього потрібно видалити орган, зокрема ногу чи руку. Якщо неможливо повністю видалити уражені тканини, їх широко розтинають. Рани при анаеробній інфекції не закривають після операції швами доти, доки не переконаються в повній ліквідації інфекції. їх дренують трубчастими дренажами з подальшим зрошенням розчинами окислювачів — перекисом водню або марганцевокислого калію. Допоміжним лікувальним заходом у післяопераційний період при анаеробній інфекції є Гіпербарична оксигенація.
Місцеве лікування гнояків після їх розтину в класичному варіанті вимагає врахування як характеру збудника інфекції та анатомо-фізіологічних особливостей локалізації, так і фази ранового процесу — очищення, проліферації і рубцювання. Залежно від виду збудника вибирають відповідний антисептик чи антибіотик (якщо вони показані після операції).
Анатомо-фізіологічні особливості осередку, топографічні взаємовідношення між ним та судинами і нервами вимагають відповідного вибору місця для розрізів та типу дренажа. Розрізи при гнійній інфекції повинні проводитись через центр або в найнижчому місці осередку для найкращого його очищення від гною. При цьому треба дотримувати загального
правила нанесення розрізів. Т. Кохер рекомендував робити їх паралельно напрямку силових ліній. У цьому разі вдається одержати максимальний косметичний ефект. У деяких випадках відходять від цього правила. Так, не бажано робити розрізи над магістральними судинами при гнояках у їх проекції, а також прямих розрізів над гнійними норицями в кістках при остеомієліті. У цьому разі розріз роблять дещо збоку і паралельно судині та збоку і паралельно довгій кістці з утворенням (відсепаруванням) шкірно-клітинного клаптя в напрямку гнояка (таким чином відкривається доступ до його центру). Це запобігає арозії судини, формуванню хірургічної виразки, рецидиву остеомієліту.
Хірургічне втручання на осередку інфекції звичайно супроводжується дренуванням порожнини гнійної рани чи будь-якої іншої гнійної порожнини. Дренажі, що для цього використовують, бувають різні за складом матеріалу та технологією їх дії. Найпоширенішим видом дренажу при поверхневих гнійних порожнинах є хлорвінілова чи гумова трубка діаметром 0,5—0,7 см з 2—3 бічними отворами на внутрішньопорожнинному кінці (мал. 62), рідше — гумова чи марлева (суха чи з маззю) стрічка. Цими дренажами з відкритої порожнини гнійний ексудат та залишки змертвілих тканин відтікають пасивно, під впливом гравітації. Вони одночасно є і розпірками між краями гнійної рани, які роблять останню відкритою на потрібний період.
Трубчасті дренажі різного хімічного складу — хлорвінілові, силіконові або гумові — можуть бути закритими, сифонними чи напівзакритими промивними (перманентно чи фракційно). Якщо гнійна порожнина не розкривається, наприклад, при плевриті, піддіафрагмальному абсцесі, її дренування може бути здійснено закритим дренажем, введеним у неї через шкірний прокол троакаром. Якщо зовнішній кінець дренажу (прикритий надягненим на нього гумовим прорізаним пальцем з рукавички) опускають у скляну банку з антисептиком, то такий дренаж називається сифонним (мал. 63). Якщо в порожнину вводять два дренажі, то по одному з них антисептичний розчин для промивання постійно чи періодично вводиться (звичайно крапельно), а по другому — промивна рідина з ексудатом та залишками некротичних тканин пасивно відтікає. У разі напівзакритої форми відплив здійснюється частково і в пов’язку через отвір у рані — такий дренаж називається припливно-відпливним (мал. 64).
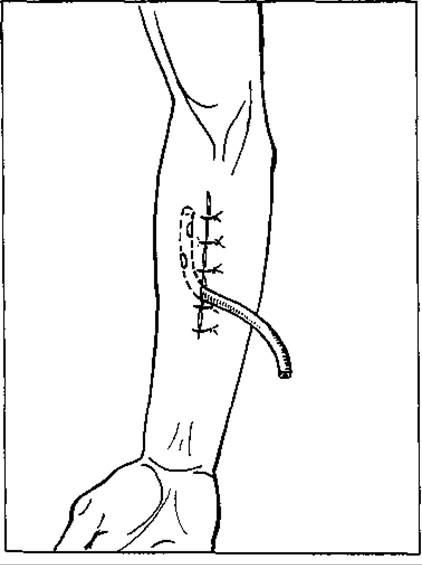
Мал. 62. Відкритий пасивний дренаж рани
У двопросвітних дренажах спеціальної конструкції промивання і відтік з порожнини відбувається через дренаж (трубку). Поряд з такими активно-пасивними, постійної чи періодичної дії, припливно-відпливними дренажами широке застосування мають трубчасті закриті дренажі, призначені для аспірації через них гнійного ексудату та введення, інстиляції в гнійну порожнину (абсцес легень, печінки) антибіотиків чи антисептиків, а також закриті дренажі для активної вакуумної постійної аспірації гнійного ексудату з різних порожнин. Це вакуумний дренаж Редона, один кінець якого з бічними отворами вводиться в гнійну порожнину, а другий з’єднується з герметично закритою склянкою з низьким тиском у ній, в яку аспірується гнійний ексудат, завдяки чому спадається гнійна порожнина. Склянка може бути замінена гумовим балоном («грушею»), під час стискання стінок якої створюється в ній вакуум, який і зумовлює відсмоктування ексудату до розправлення балона внаслідок заповнення його (мал.65).
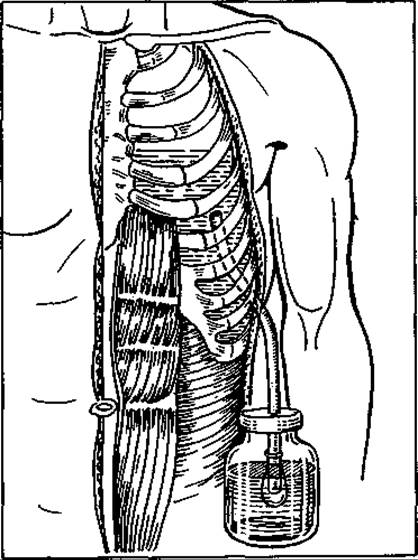
Мал. 63. Закритий сифонний дренаж плевральної порожнини за методом Бюлау
Другий вид закритого вакуумного аспіраційного дренажу, який дозволяє дозувати розрідження в системі, застосовується при лікуванні гнійного плевриту. Він складається з трубки (силіконова чи гумова, стінки яких не спадаються), введеної в нижній відділ плевральної порожнини і з’єднаної своїм зовнішнім кінцем із апаратом А.А. Боброва з двох скляних, сполучених між собою банок, або трьох, також сполучених, скляних ампул, в яких переливання асептичної рідини із розташованої вгорі банки в нижню утворює вакуум і забезпечує присмоктування ексудату (мал. 66).
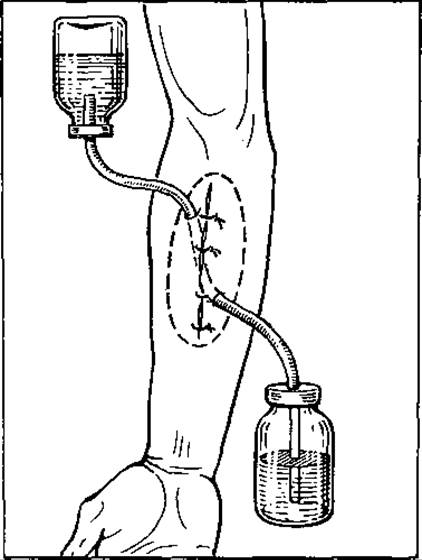
Мал. 64. Припливно-відпливне (промивне) дренування рани
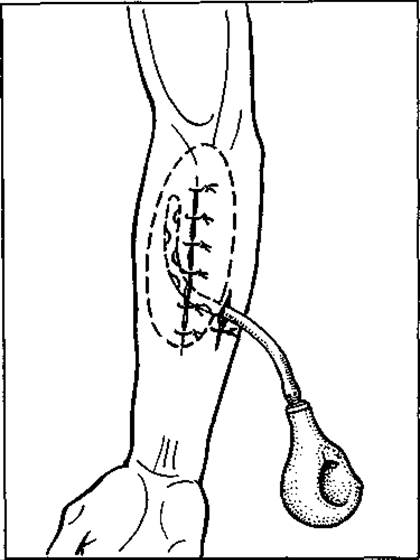
Мал. 65. Вакуумне дренування рани за методом Редона
Хоча зараз у гнійній хірургії застосовують головним чином трубчасті, рідше — рукавично-трубчасті дренажі, але й марлеві дренажі, незважаючи на дуже швидку втрату ними своїх дренажних якостей після намокання, інколи застосовують поряд із трубчастими. їх уводять не стільки для дренування, скільки для обмеження осередків інфекції в черевній порожнині, для гемостатичних цілей при капілярних кровотечах у гнійних осередках у черевній порожнині, а також у великих гнійних зовнішніх порожнинах для підтримки зяяння останніх з метою запобігання передчасному утворенню ізольованих камер у них тощо.
Дренажі, особливо не термолабільні — гумові, скляні, не можна розміщувати поруч із судинами, щоб не спричинити тромбозу їх або пролежнів (ерозію). Вони повинні бути ізольовані від судин м’якими тканинами.
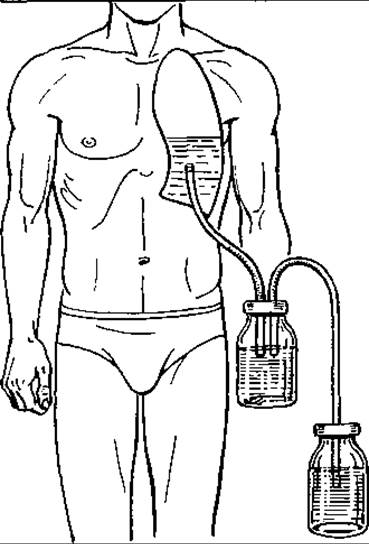
Мал. 66. Вакуумне дренування з дозованим розрідженням за допомогою апарата Боброва
Найбільш вживаними трубчастими як одно-, так і двопросвітні. Останні дренажами є силіконові, хлорвінілові не спадаються і не закупорюються та інші пластикові термолабільні — гноєм.
ЗАГАЛЬНЕ ЛІКУВАННЯ ХВОРИХ З ХІРУРГІЧНОЮ ІНФЕКЦІЄЮ
Загальне лікування необхідне всім хворим з інфекцією, незалежно від її виду — будь це ускладнення рани, в тому числі й післяопераційної, чи хірургічне інфекційне захворювання, оскільки не існує суто місцевих видів інфекції. Кожна інфекція супроводжується загальними явищами, зумовленими інтоксикацією. Джерела інтоксикації — мікроби та їх токсини, продукти розпаду загиблих тканин, неспецифічні продукти обміну, в тому числі так звані середньомолекулярні пептиди. Загальне лікування хворих насамперед передбачає створення оптимальних умов для реалізації своїх, ендогенних, механізмів захисту від мікробної токсичної агресії — інтоксикації. Хворому повинен бути забезпечений стан фізичного та психічного спокою, мають бути усунені всілякі несприятливі подразники, насамперед біль. Хворому приділяють максимальну увагу, пояснюють йому характер захворювання та окреслюють вимоги до нього, виконання яких допоможе якнайшвидшому одужанню. Стаціонарним хворим забезпечують добрі умови, збалансоване в якісному та кількісному відношенні харчування. Це важлива складова і передумова загального лікування.
Комплекс загальних заходів лікування може бути різноманітним за складом та призначенням. Але незалежно від цього від повинен спрямовуватися на: 1) припинення розвитку та поширення інфекції; 2) зниження й ліквідацію інтоксикації організму; 3) активізацію захисних сил організму та регенеративно-репаративних можливостей хворого; 4) корекцію порушень функції органів та систем, спричинених інфекцією; 5) прискорення загоєння і ліквідацію місцевого осередку.
Дезінтоксикація здійснюється різними шляхами, серед яких головним є знищення мікробів, зменшення концентрації токсинів та мікробів, їх розведення, нейтралізація токсинів зв’язуванням їх або інактивацією і виведення. Загальні заходи, спрямовані на гальмування розвитку, знищення мікрофлори, припинення її поширення полягають насамперед у призначенні антимікробних засобів резорбтивної дії, зокрема антибіотиків та хіміопрепаратів (ентерально чи парентерально). Звичайно їх призначають або при лікуванні місцевої інфекції без хірургічного втручання, або після нього (за деяких форм інфекції). Незалежно від останнього нерідко залишається загроза поширення патогенної мікрофлори (великий, осередок інфекції або її небезпечна локалізація, недостатня опірність організму та ін.). Наприклад, при гематогенному остеомієліті, гнійному артриті чи сухожильному панариції, великих флегмонах чи карбункулах, у хворих на цукровий діабет та багатьох інших видах інфекції місцеве хірургічне втручання доповнюється застосуванням або антибіотиків, або антимікробних хіміопрепаратів (сульфаніламіди, фторквіноли, зокрема ципрофлоксацин та його аналоги тощо). Застосування цих протимікробних засобів повинно грунтуватись на знанні виду мікроорганізмів та їх чутливості до препарату. Оскільки встановлення цих показників погребує тривалого часу, а гостра інфекція потребує негайного лікування, в багатьох випадках застосовують антибіотики широкого спектру дії або альтернативні хіміопрепарати з високою антибактеріальною активністю.
Серед антибіотиків найбільш уживаними є бензилпеніциліну натрієва сіль, Напівсинтетичні Пеніциліни (ампіцилін тощо), напівсинтетичні Цефалоспорини (цефазим), Аміноглікозиди (гентаміцин, канаміцин), кліндаміцин та інші, а серед антимікробних хіміопрепаратів — метронідазол (активний стосовно анаеробної неклостридіальної мікрофлори), сульфаніламіди та похідні налідиксової кислоти — ципрофлоксацин, флюоронор-флоксацин, цифран та ін.
Слід зазначити, що стрептококи, гонококи, пневмококи, менінгококи, клебсієла, сальмонели, клостридії та деякі інші мікроби зберігають високу чутливість до препаратів групи пеніциліну і тому захворювання, що спричинюються зазначеними мікробами (бешиха, гонорейні сальпінгіти та сальпінго-офорити, менінгіт, пневмококовий перитоніт тощо), треба зразу починати лікувати препаратами групи пеніциліну без визначення антибіотикограми.
Стафілококи та кишкова паличка завдяки здатності до мутації та трансмісивній стійкості (здатності утворювати беталактамазу — фермент, що інактивує пеніцилін та Інші антибіотики) нечутливі до антибіотиків перших поколінь. Тут обов’язково потрібно визначити антибіотикограму. Тому при інфекціях, що спричинюються стафілококами, кишковою паличкою, синьогнійною паличкою, бактероїдами тощо, лікування треба розпочинати з антибіотиків широкого спектра дії в поєднанні з метронідазолом (проти бактероїдів), а з одержанням даних мікробіологічного дослідження та антибіотикограми — засобами цілеспрямованої дії чи коригувати схему лікування.
Треба зазначити, що багато видів патогенних мікробів, збудників гнійної інфекції (стафілокок, синьогнійна паличка, кишкова паличка, неклостридіальна анаеробна мікрофлора) дуже стійкі і до сучасних антибіотиків широкого спектра дії. Навіть у найактивнішого аміноглікозиду (гентаміцину сульфату) ефективність проти стафілококової інфекції не перевищує 70—80 %. Тому у разі тяжких форм інфекції треба користуватися новітніми напівсинтетичними, що стійкі до беталактамаз, які продукуються мікробами, антибіотиками (мефоксин чи мефокситин — препарат IV покоління цефалоспоринів; амоксиклав-амоксицилін у комбінації з клавулановою кислотою, що є інгібітором беталактамаз) та антибактеріальними препаратами із групи фторквінолонів (ципрофлоксацини, ципробай) і кабапенемів (тієнам та ін.).
Ципрофлоксацини та тієнам за протимікробною силою навіть переважають антибіотики. Вони ефективні практично за будь-якої хірургічної інфекції, зумовленої як грампозитивною, так і грамнегативною мікрофлорою, у тому числі бактероїдною.
Детоксикація організму здійснюється багатьма засобами. Розпочинати її треба з найпростіших і найдоступніших. Це насамперед призначення великої кількості рідини (за відсутності протипоказань) та внутрішньовенне введення ізотонічних розчинів натрію хлориду чи натрію лактату або розчинів Рінгера—Локка, Гартмана, лактосолу тощо. У останніх, порад із натрію хлоридом (6—8 г/л), є калію хлорид (0,2 — 0,3 г/л), кальцію хлорид (0,1— 0,2 г/л), натрію гідрокарбонат (немає в розчині Гартмана), натрію лактат — 3,1—3,3 г/л (його нема в розчинах Рінгера та Рінгера—Локка). У лактосолі є, крім того, ще й магнію хлорид. Ізотонічні розчини натрію хлориду (0,9 %) та лактосол є офіційними, виготовляються на заводах медпрепаратів, усі інші — виготовляються в аптеках.
Названі розчини зменшують інтоксикацію шляхом як розведення токсинів, так і підвищення їх виведення з організму з сечею.
Для багатьох хворих введення цих розчинів буває досить (поряд з місцевим втручанням і місцевими заходами) для ліквідації осередку інфекції та детоксикації організму. Але у деяких випадках цих засобів дезінтоксикації, що діють шляхом простого розведення та компенсації гідроіонних порушень, буває замало. Тому призначають засоби спеціальної інфузійно-трансфузійної терапії, а в низці випадків, зокрема при загальній інфекції, ще й інші заходи — штучний гемодіаліз (гемо- та лімфосорбцію тощо).
Серед спеціальних засобів для інфузійної дезінтоксикації, які зв’язують та виводять Токсичні речовини з організму, найбільше поширення мають препарати вінілових сполук — по- лівінілпіролідон, гемодез та полідез, а також перистон та неокомпенсан. У нас головним засобом цього ряду є 6 % розчин низькомолекулярного полівінілпіролідону (неокомпенсан). Цей препарат діє шляхом зв’язування (адсорбції) токсичних речовин у кровоносному руслі та швидкого виведення їх з організму, головним чином, через нирки. Він виводиться з організму протягом 4—9 год (М.Т. Терехов, 1979). Гемодез також сприяє детоксикації шляхом поліпшення мікроциркуляції (усуває стаз еритроцитів) та ліквідації гіпоксії тканин. Вводять гемодез крапельно внутрішньовенно по 10 мл/кг маси тіла для дітей та 400 мл на одну інфузію для дорослих. Повторне вливання можливе не раніше ніж через 12 год. Дія препарату розпочинається через 10—15 хв. Інший препарат — полідез — є низькомолекулярним розчином полівінілового спирту. Застосовується 3 % розчин полідезу в ізотонічному розчині (0,9 %) натрію хлориду в дозі 400— 800 мл на добу у тих самих випадках, що й гемодез.
Поряд із означеними розчинами з метою дезінтоксикації використовують і багато інших речовин, які не тільки зв’язують токсини, але й володіють іншими ефектами, зокрема гемодинамічним, антитромботичним чи реологічним. Їх призначають хворим, у яких інтоксикація поєднується з гіпопротеїнемією, гіпотензією чи порушенням коагуляції крові (тромбоемболічним станом, агрегацією еритроцитів).
Серед цих препаратів широко відомі такі білкові препарати, як альбумін (10—20 % розчин) та протеїн (10 % розчин), що вміщують до 80 % альбуміну та 20 % глобулінів. Вводять їх у дозах по 100 мл та 200—400 мл один раз на добу. Білкові препарати утворюють білкові комплекси з токсинами, зв’язують та утримують в судинах воду (1г альбуміну утримує в судинах 20 мл води), підвищують артеріальний тиск і фільтраційну здатність нирок. Це сприяє виведенню токсинів.
При інфекціях, що супроводжуються гіперкоагуляцією та порушенням мікроциркуляції, які загрожують тромбоемболією, високоефективним є реополіглюкін — низькомолекулярний поліглюкін. Його вводять у дозі 400 мл на добу, ефект зберігається протягом 8 год. Для лікування таких хворих використовують також інші антикоагулянти (гепарин) та дезагреганти (ацетилсаліцилова кислота).
Для дезінтоксикації та знищення мікробів застосовують також білкові імунні препарати гаммаглобулін, антистафілококову плазму. Ці препарати, що вміщують антитіла проти відповідних мікроорганізмів та їх антигенів, зв’язують їх у комплекси антиген — антитіло і нейтралізують, дезактивують. Вони особливо ефективні при гіпогаммаглобулінемії.
Високими дезінтоксикаційними властивостями володіють також осмотичні діуретичні засоби, до яких належать багатоатомні спирти — маннітол та сорбітол. Це шестиатомні спирти, які вводять внутрішньовенно в 10—20 % (маннітол) і 20 % (сорбітол) розчинах у дозах 1—2 г сухої речовини на 1 кг маси тіла. Вони починають діяти через 15 хв, а максимальне сечовиділення спостерігається через 2 год. Більша частина препаратів виводиться протягом доби (до 80 %) нирками, інші ж використовуються організмом як енергетичні речовини. Ці препарати призначають переважно при гострій нирковій недостатності.
У разі винятково тяжкої інфекційної інтоксикації, як це буває при сепсисі, застосовують штучний гемодіаліз, перитонеальний діаліз, гемо- та лімфосорбцію, ультрафіолетове та
лазерне опромінення крові і навіть підключення ксеноселезінки чи печінки, переважно свинячої. Треба пам’ятати, що детоксикація організму — поняття дуже широке і не може бути зведене лише до застосування названих вище препаратів та заходів. Перелічені інфузійні засоби спрямовані головним чином на наслідок інфекції, тобто продукт її. Детоксикаційним ефектом володіють і всі ті засоби, які безпосередньо діють на збудників інфекції (антибіотики та хіміопрепарати) або коригують функції організму, обмін речовин, без нормалізації яких процеси детоксикації не можуть відбуватись повноцінно. Тому поряд із спеціальними, цілеспрямованими засобами не менш важливими в лікуванні хворих з інфекцією є всі інші загальні заходи для лікування хірургічної інфекції. Зокрема, призначають симптоматичні препарати (серцево-судинні, аналгетики, седативні та ін.), імунокоректори та імуностимулятори (тактивін, тімалін, тимоген та ін.), анаболічні гормони та препарати (андростерон, неробол, ретаболіл, солкосерил-розчин тощо), інгібітори протеолізу та простагландинів тощо.
Профілактика ХІРУРГІЧНОЇ ІНФЕКЦІЇ
Великий ризик для здоров’я та величезні економічні витрати, пов’язані з лікуванням хворих, ставлять сьогодні профілактику хірургічної інфекції на вищий ступінь, ніж пошук все нових і переважно малоефективних засобів лікування.
Звичайно, профілактика інфекції є складною уже через свою багатоплановість, пов’язану з безліччю причин розвитку її та умов, що сприяють цьому. Наведений раніше перелік найважливіших загальних причин поширення хірургічної інфекції слугує дороговказом для вибору профілактичних заходів.
Жорсткість асептичного режиму в хірургічних стаціонарах і насамперед у операційних та перев’язочних — нагальне завдання. Це передусім підвищення вимог щодо асептичного режиму до всіх працівників хірургічних та анестезіологічних і реанімаційних відділень, підвищення професіоналізму в здійсненні асептичних заходів та контролю з боку завідувача хірургічного відділення (операційного блоку) та старшої операційної сестри, провітрювання палат, дезінфекція постелі, вологе прибирання тощо. Високий гігієнічний режим у відділенні, гігієна персоналу (спеціальний одяг, виявлення та лікування бацилоносіїв) та хворих (миття хворих під душем з антимікробним милом, повна ізоляція хворих з відкритими вогнищами інфекції від здорових), максимальне скорочення перебування хворих перед операцією у відділенні, уникнення перев’язки в палаті дозволяють зменшити загрозу госпіталізму, контамінації поверхні тіла хворих полірезистентними мікробами.
Ретельне дослідження та обстеження хворих перед операцією з метою виявлення якихось відхилень та порушень у них імунітету й інших чинників ризику і корекція їх зменшують загрозу інфекційних ускладнень після операції. Обмеження інвазивних досліджень суворими показаннями, зістригування, а не гоління Волосся в зоні операційного поля за 30 хв до операції, змазування шкіри операційного поля перед операцією антисептиками, використання водонепроникної білизни для хірургічної бригади, покриття операційного поля після його обробки самоклеючими плівками, через які проводиться розріз, користування гострими інструментами для розтину тканин, бережливе ставлення до останніх, зменшення кількості лігатур, користування в контамінованій рані монофільними, що не мають абсорбуючих властивостей, швами та швами, що розсмоктуються, своєчасна заміна рукавичок у разі їх пошкодження, заміна інструментів після розрізування шкіри — все це сприяє зменшенню ризику щодо розвитку хірургічної інфекції, зокрема інфікування ран. Серед видів хірургічної інфекції найбільшу питому вагу мають інфекція ран та ушкоджень (мікротравми, опіки, відмороження, укуси та ужалення комах тощо), а також післяопераційна (ранова та порожнинна) місцева і загальна інфекції. Тому запобігання цим видам інфекції складає найважливішу проблему. Профілактика інфекції випадкових ран та пошкоджень полягає в своєчасній їх діагностиці, поданні першої медичної допомоги. Добре налагоджена робота травматологічних пунктів, медпунктів, хірургічних кабінетів, станцій «Швидкої допомоги» має величезне значення як для профілактики інфекції, так і нерідко долі потерпілих. У лікуванні цих ран основу складає первинна хірургічна обробка, найкраще в перші 6—12 год після нанесення рани, але не пізніше 24 год, з подальшими допоміжними засобами (дренування порожнини рани, місцеві хімічні та фізичні впливи на неї, асептичні та антисептичні пов’язки, фізметоди, загальні заходи). Поряд із хірургічною обробкою рани в профілактиці ранової специфічної інфекції (правець, сказ) велику роль відіграють імунізація хворих (пасивна, чи пасивно-активна, чи лише активна). Запобігання інфікуванню мікротравм грунтується на санітарній освіті людей та своєчасній обробці мікротравм, зокрема обмиванні пошкодженого місця, якщо воно забруднене, стимулюванні кровотечі з проколу шляхом стискання м’яких тканин з боків у зоні пошкодження, змазуванні місця ушкодження антисептичним засобом — розчином йоду, спирту чи брильянтового зеленого з подальшим закриттям його клеєм БФ-2 чи лейкопластирем або змазуванням ураженого місця антисептичною клеєвою рідиною. Для обробки мікротравм запропоновано багато таких спеціальних антимікробноклейових композицій, які при нанесенні на пошкоджене місце тверднуть. Вони дають одночасно і дезінфікуючі, й герметизуючі ефекти (рідина М.В. Новикова, клей БФ-2 тощо). Велику роль у профілактиці інфекції випадкових ран відіграють радикальне видалення макроскопічно пошкоджених тканин, ретельний гемостаз (краще без електрокоагуляції), негусте накладання швів та розташування їх у безпосередній близькості від краю (не більше 0,5 см), бережливе ставлення до тканин, аподактильна робота та суворе додержання всіх правил асептики під час виконання цієї операції. У разі вимушеної відстрочки хірургічної обробки рани — до 24 год і більше — хворому треба призначити профілактично антибіотики (краще з групи напівсинтетичних пеніцилінів — ампіцилін чи пентрексил та ін.) або один із сульфаніламідних препаратів (сульфадиметоксин та ін.), які затримують розвиток інфекції в рані. У разі запізнілої хірургічної обробки рани, коли в ній уже є ознаки серозного запалення (так звана інфікована рана), для запобігання розвитку в ній гнійного запалення («гнійної рани») рану не зашивають, а дренують і накладають на неї вологовисихаючі антисептичні осмотичні пов’язки. Ефективними є фізіотерапевтичні процедури, відкрите лікування в асептичних камерах чи аеротерапевтичних установках (АТУ) та загальні заходи (антибіотикотерапія тощо). Раннє закриття рани, аж до пластичного (невільним чи вільним клаптем шкіри), є добрим профілактичним засобом проти розвитку інфекції в ній. Таким самим важливим заходом є введення після обробки контамінованих ран або інфікованої рани (стадія серозного запалення) в їх порожнину припливного чи припливно- відпливного дренажу з антисептиком до повної ліквідації ознак запалення.
Для профілактики інфікування порожнин (черевної, плевральної, черепа, суглобів) важливе значення мають рання діагностика гострих захворювань органів цих порожнин, запобігання забрудненню їх вмістом та матеріалом з уражених органів та тканин, видалення під час операції залишків крові та інших речовин (шматочків тканини, рідин) шляхом вимивання та аспірації їх з тих порожнин, в яких виконувалось оперативне втручання. В багатьох випадках виконують дренування порожнини (трубками, катетерами) з метою як відсмоктування залишків ексудату, так і введення через трубчасті дренажі антисептиків чи антибіотиків. У профілактиці післяопераційної інфекції не можна переоцінити роль ліквідації в передопераційний період латентних осередків інфекції, анемії, гіпоксемії, дефіциту білків (гіпопротеїнемії), електролітів та порушень інших видів обміну, особливо вуглеводного (у хворих на цукровий діабет) тощо.
Важлива роль належить також достатнім доступам при операціях, досконалим оперативній техніці та анестезії, а також безпосередній профілактичній антибіотикотерапії (за 1—2 год перед операцією) в максимальній добовій дозі (внутрішньовенно чи внутрішньом’язово) при втручаннях у хворих з дуже забрудненими ранами та інфекційно-запальними хірургічними процесами у внутрішніх органах та у хворих, у яких втручання виконуються на товстій та прямій кишках, на серці та судинах з протезуванням, у хворих на цукровий діабет та ін. Профілактична антибіотикотерапія (Хіміотерапія) рекомендується в таких випадках:
1) при випадкових забруднених ранах, які не можуть бути своєчасно хірургічно оброблені;
2) при всіх забруднених мікробами операційних ранах;
3) при всіх ранах з ендопротезуванням;
4) при операціях у людей з інфекцією чи у тих, хто щойно перехворів на інфекційну хворобу;
5) при операціях у хворих з попереднім ураженням серцевих клапанів (для профілактики ендокардиту);
6) при операціях «чисто-забруднених», коли розкривають порожнину кишки, жовчних шляхів тощо.
Профілактично застосовують антибіотики широкого спектру дії.
Велике значення мають догляд за хворими та ранами, відповідні санітарно-гігієнічні умови в палатах перебування хворих, раціональне загальне лікування хворих (вітамінізоване харчування, корекція гідроіонного балансу та інших порушень обміну, оксигенація, використання імунних, гормональних та ферментних препаратів).
Особливу увагу в профілактиці післяопераційної інфекції треба приділяти підвищенню кваліфікації хірургів, особливо тих, хто чергує на невідкладній допомозі, та персоналу відділень інтенсивної терапії і реанімації, боротьбі з бацилоносійством, яке особливо часто спостерігається у персоналу хірургічних відділень.
У запобіганні інфекційним хірургічним захворюванням мають велике значення добре налагоджені санітарно-гігієнічні умови на виробництві та в побуті, заходи з техніки безпеки на виробництві та своєчасна обробка мікротравм, лікування прихованих осередків латентної інфекції та загальних системних хвороб (серцево-судинних, обмінних, ендокринних, алергічних та інших), запобігання та боротьба з ожирінням, заняття фізкультурою, оздоровчим спортом, загартування.
Безумовно, для профілактики хірургічної інфекції не досить лише медичних заходів. Останні можуть бути ефективні лише на тлі економічного добробуту людей та сприятливих екологічних умов їх проживання.
Последнее обновление: 14/02/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.