Антибіотики (властивості, застосування, взаємодія) - Посохова К.А., Вікторов О.П. 2005
Принципи раціональної антибіотико-терапії
І. Наявність обгрунтованих показань до призначення антибіотика.
Ретельний підбір пацієнтів, які дійсно потребують антибактеріальної терапії, особливо важливий в амбулаторній практиці при інфекційних процесах, які часто зустрічаються. Зокрема, при гострих респіраторних вірусних інфекціях антибактеріальні антибіотики, які не впливають на віруси, хворим не показані. Вони застосовуються при виникненні бактерійних ускладнень або ж для їх профілактики при хронічних процесах (наприклад, при хронічному бронхіті), коли є значний ризик їх загострення на фоні пригнічення активності імунної системи вірусними агентами. Невиправдано часто антибіотики застосовують для Лікування інфекцій верхніх дихальних шляхів у дітей. При цьому лікар виходить із помилкової точки зору, що слизово-гнійні виділення з носа є незаперечною ознакою бактерійної інфекції. Не потрібне призначення антибіотиків у багатьох випадках при запаленні
середнього вуха. Визнана помилковою тривала терапія тетрациклінами або макролідами пацієнтів із вугрями.
Селективна деконтамінація шлунково-кишкового тракту, яка набула поширення в пацієнтів відділень інтенсивної терапії, як свідчать результати останніх досліджень, не тільки не покращує результатів лікування, але призводить до поширення антибіотикорезистентних грампозитивних мікроорганізмів. Тому її необхідно використовувати лише за строгими показаннями.
Надто широко використовують антибіотики і для профілактики інфекцій у хірургії. Зокрема, у США за останні 15 років призначення їх з цією метою у 40-75 % випадків було необгрунтованим. На сьогодні помилковою вважається антибіотикопрофілактика у таких випадках: при проведенні УЗД-контрольованої трансректальної біопсії простати, при проведенні ендоскопічної ретроградної холецистопанкреатографії, для попередження менінгіту при переломах основи черепа, за наявності постійного катетера сечового міхура в дітей, при неускладнених ранах, при передчасних пологах, при лікуванні дітей з інфекціями верхніх дихальних шляхів, при лікуванні гострих бронхітів у дорослих без супровідної патології.
При хронічних гнійних процесах (хронічному абсцесі, остеомієліті, емпіємі тощо) призначення антибіотиків переслідує мету попередження поширення інфекції внаслідок руйнування тканинних бар’єрів при хірургічних методах санації гнійного вогнища.
При деяких гострих інфекціях у разі їх легкого перебігу (наприклад, при гастроентериті) віддають перевагу симптоматичному лікуванню, тому що призначення антибіотиків може сприяти формуванню носійства.
II. Вибір найбільш активного і найменш токсичного препарату та своєчасність його призначення хворому.
Препарати, що є найефективнішими при певному виді інфекції, до яких чутлива більшість штамів даного збудника, називаються препаратами першого вибору (першого ряду, першої групи). Альтернативні препарати (другого ряду) призначаються тоді, коли препарати першої групи неефективні або коли штам виділеного збудника найчутливіший саме до них. Препарати резерву використовують лише у крайніх випадках (при неефективності першої і другої груп антибіотиків); як правило, вони викликають багато ускладнень.
Список антибіотиків, які є препаратами першого вибору й альтернативними для різних видів мікроорганізмів, що викликають інфекційні процеси, представлений у додатку 2.
Перед початком лікування, до першого Введення антибіотика, необхідно взяти матеріал для бактеріологічного дослідження (Кров, екскрети та ін.) - провести визначення збудника та його чутливості до антибактеріальних агентів (антибіотикограма). Якщо забір матеріалу здійснено навіть після одного введення антибіотика або іншого антибактеріального засобу, справжнього збудника визначити часто не вдається.
При деяких інфекціях вибір антибактеріального засобу повністю грунтується на клінічному діагнозі. Це можливо тоді, коли мікроорганізм, що викликає захворювання, є типовим для даної патології: при крупозній пневмонії в осіб молодого віку - це найчастіше пневмокок; при скарлатині, бешиховому запаленні - гемолітичні стрептококи та ін.
Особливо важливою і відповідальною є емпірична терапія інфекцій з тяжким перебігом, коли неможливо відкласти початок призначення антибіотика до отримання результатів антибіотикограми. При цьому антибіотик обирають, грунтуючись на найчастішій етіології інфекцій різної локалізації (Додаток 1) і на узагальнених даних щодо чутливості збудників інфекційних захворювань до антибактеріальних препаратів (додаток 2). Найкращі результати лікування дає тоді, коли одночасно враховують дані з етіологічної структури захворювань та резистентності мікроорганізмів у даному регіоні, ще оптимальніше - у конкретному лікувальному закладі. Надзвичайно важливою є оцінка цих факторів у терапії госпітальних інфекцій. Водночас, все необхідне для бактеріологічного аналізу (кров, гній, сечу, харкотиння, ліквор) беруть до першого введення лікарського засобу. За необхідності, після отримання результатів антибіотикограми, у випадку, коли протягом 3 днів попередньо призначений препарат не дає лікувального ефекту, його замінюють більш ефективним.
При емпіричній терапії тяжких інфекцій надзвичайно важливе значення має своєчасність призначення антибіотиків. Найоптимальнішим вважається варіант, при якому перше введення антибактеріального засобу проводиться вже у приймальному відділенні, одразу після встановлення діагнозу. Така тактика дозволяє істотно зменшити відсоток смертності. Добрі результати вдається отримати й у випадку, коли антибактеріальна терапія розпочинається у перші 8 год після госпіталізації хворого.
Хірургічна антибіотикопрофілактика повинна здійснюватись не раніше ніж за 2 год до початку операції, найкраще - приблизно за 30 хв до розрізу, під час ввідного наркозу.
III. Введення оптимальних доз препарату з оптимальною частотою та врахуванням тяжкості інфекційного процесу.
Чутливість бактерій до антибіотиків у процесі мікробіологічного дослідження визначається МІК, що виражається у мг/л (або ОД/л) і є тією кількістю антибіотика, яка in vitro викликає гальмування росту 90 % штамів збудника.
Як правило, для отримання оптимальної лікувальної дії середня терапевтична концентрація (СТК) антибіотика в крові повинна перевищувати МІК у 3-4 рази. Але у хворих з імунодефіцитом, при важкодоступних вогнищах інфекції (абсцеси, менінгіт) антибіотики необхідно використовувати у дозах, які набагато перевищують МІК.
Якщо дози підібрані неправильно, не створюється СТК препарату в тканинах. Це може зумовити неефективність лікування та формування резистентності мікроорганізмів до препарату. Переривчастий спосіб застосування антибіотиків (певна кількість прийомів на добу) традиційно вважається більш доцільним, ніж їх безперервна інфузія. Кратність введення препарату залежить від часу, протягом якого зберігається його СТК у тканинах (крові, лікворі, інших рідинах і тканинах, де локалізована інфекція). Період напіввиведення антибіотика з організму може бути лише умовним орієнтиром для визначення проміжків часу між його введенням. Разом з тим, визначаючи кратність введення антибактеріальних препаратів, необхідно враховувати механізм їх дії, наявність постантибіотичного ефекту, деякі особливості й умови для оптимального прояву їх антибактеріальної активності.
Звичайно антибактеріальні препарати використовують у дозах, які створюють у тканинах макроорганізму концентрацію, яка перевищує МІК (МПК) для збудника, що викликав захворювання. Разом з тим, багато антибіотиків здатні зберігати свою антимікробну активність в концентраціях, які нижчі, ніж МПК (суб-МПК ефект). Крім того, після виведення антибіотика з організму життєдіяльність (ріст та розмноження) мікроорганізмів може поновлюватись не одразу, а через певний проміжок часу, що отримало назву постантибіотичного ефекту. Наявність в антибіотика постантибіотичного ефекту дозволяє зменшити кратність його застосування протягом доби.
Останнім часом прийнятий розподіл антибіотиків на дозозалежні та часозалежні (табл. 1). До перших належать Аміноглікозиди, фторхінолони, метронідазол, амфотерицин В, до других - бета-лактами, глікопептиди, макроліди, Лінкозаміди.
Таблиця 1. Дозо- та часозалежні антибіотики (И.Г. Березняков, 2002)
|
Дозозалежні антибіотики |
Часозалежні антибіотики |
|
Аміноглікозиди «Нові» макроліди (азитроміцин, кларитроміцин) Фторхінолони Амфотерицин В Метронідазол Кетоліди (телітроміцин) Стрептограміни (хінупристин/дальфопристин) |
Бета-лактами Еритроміцин та інші «старі» макроліди Глікопептиди Кліндаміцин |
Антибактеріальний ефект дозозалежних препаратів прямо залежить від їх концентрації в інфекційному вогнищі. Відповідно найвищу ефективність вони проявляють у високих дозах, які близькі до токсичних. Тому для засобів із дозозалежним ефектом, зокрема аміноглікозидів, більш доцільним є їх одноразове введення у високій дозі (на початку лікування - 6-7 мг/кг, з наступною корекцією після повторних визначень концентрації препаратів у крові). Ефективність часозалежних антибіотиків найбільше визначається тим проміжком часу, протягом якого концентрація препарату в крові перевищує МІК для даного збудника. Причому для найкращої реалізації антибактеріальної дії необхідно, щоб це перевищення зберігалося не менше 40 % інтервалу часу, який проходить між окремими введеннями антибіотика. Саме тому при застосуванні часозалежних препаратів так важливо вводити їх з певною визначеною кратністю протягом доби або ж, у деяких випадках, шляхом внутрішньовенної краплинної інфузії. Враховуючи залежність дії бета-лактамних антибіотиків від часу, їх нерідко вводять методом постійної інфузії.
IV. Вибір оптимального способу введення препарату з урахуванням тяжкості та локалізації інфекційного процесу й особливостей фармакокінетики даного антибіотика.
Парентеральний шлях введення антибіотиків при емпіричній терапії використовують у тяжкохворих пацієнтів з порушенням функції шлунково-кишкового тракту. Таким способом вводять також препарати, що мають низьку біодоступність при прийманні всередину.
У новонароджених при будь-якій локалізації процесу антибіотики призначають переважно внутрішньовенно або внутрішньом’язово; пероральне, ректальне або підшкірне введення в дітей менш ефективне.
При лікуванні неускладнених пневмоній антибіотики доцільно використовувати перорально, внутрішньом’язово або внутрішньовенно, при наявності деструкції легень, абсцесів - шляхом ендобронхіального введення.
У наш час набула поширення ступенева (етапна) терапія антибіотиками: внутрішньовенне їх введення на початку лікування з наступним, після стабілізації стану хворого, переходом на їх пероральне приймання. Для ступеневої терапії використовують препарати, які існують у лікарських формах для парентерального та перорального застосування (табл. 2).
При неускладнених інфекційних діареях антибактеріальні засоби призначають перорально, при проникненні збудника з просвіту кишечника в його стінку, тим більше в системний кровотік, - парентерально.
Таблиця 2. Препарати, які можна використовувати для ступеневої терапії
|
Препарат |
Фармакологічна група |
Біодоступність при пероральному веденні (%) |
Період напіввиведення (год) |
|
Амоксицилін |
Амінопеніциліни |
75-90 |
1-1,5 |
|
Цефрадин |
90 |
1,3 |
|
|
Кларитроміцин |
Макроліди |
50-55 |
5-6 |
|
Еритроміцин |
Макроліди |
35-45 |
1-1,5 |
|
Спіраміцин |
Макроліди |
65-80 |
6-8 |
|
Азитроміцин |
Азаліди |
37 |
20-40 |
|
Ципрофлоксацин |
Фторхінолони |
70-80 |
4 |
|
Левофлоксацин |
Фторхінолони |
98 |
5-7 |
|
Офлоксацин |
Фторхінолони |
98 |
5-7 |
|
Котримоксазол |
Сульфаніламіди |
85-100 |
9-12 |
|
Доксициклін |
90-100 |
18-22 |
|
|
Кліндаміцин |
Лінкозаміди |
90 |
1,5-3,5 |
|
Фосфоміцин |
60 |
2,2 |
|
|
Фузидієва кислота |
90 |
16 |
|
|
Хлорамфенікол |
Хлорамфеніколи |
80 |
1,5-3,5 |
|
Метронідазол |
Антианаеробні |
95 |
8 |
|
Флуконазол |
Протигрибкові |
90-100 |
30 |
При лікуванні менінгітів, енцефалітів внутрішньовенно вводять препарати, що добре проникають через гематоенцефалічний бар’єр, у деяких випадках - безпосередньо в шлуночки мозку (нейрохірургічне втручання).
При деяких інфекціях враховують вплив рН тканин та рідин на прояв активності антибіотиків (табл. 3), зокрема при інфекціях сечовивідних шляхів необхідно враховувати рН сечі.
Пеніциліни ефективні при рН 5,0-6,5, макроліди та аміноглікозиди - при рН 7,5-8,5.
При шкірних інфекціях антибіотики використовують місцево, при локалізації процесу в підшкірній клітковині, м’яких тканинах їх вводять у вену або в м’яз.
У разі глибоких тканинних інфільтратів, пневмоній, інфекцій сечовивідних шляхів для введення антибіотиків іноді користуються методом електрофорезу: з негативного полюса проникає ампіцилін, ампіокс, оксацилін, пеніцилін, метицилін, диклоксацилін, карбеніцилін, еритроміцин; із позитивного - гентаміцин, тобраміцин, сизоміцин, канаміцин, неоміцин, лінкоміцин, кліндаміцин, поліміксин В.
Таблиця 3. Вплив pH на активність антибіотиків (И.Г. Березняков, 2002)
|
Антибіотики |
Активність при рН |
||
|
< 5 |
6 |
7 |
|
|
Бета-лактами |
- |
++ |
+++ |
|
Аміноглікозиди |
- |
+ |
+++ |
|
Хлорамфенікол |
- |
+ |
+++ |
|
Тетрацикліни |
+ |
+++ |
++ |
|
Рифампіцин |
+++ |
++ |
++ |
|
Еритроміцин |
- |
+ |
+++ |
|
Фторхінолони |
- |
+ |
+++ |
V. Встановлення тривалості курсу антибіотикотерапії.
Тривалість лікування залежить від виду збудника, вибраного протимікробного препарату, локалізації інфекційного процесу, стану захисних сил організму і в середньому коливається від 5-7 до 14-21 дня. Вважається, що лікування препаратом проводиться до одужання хворого і ще приблизно протягом 3 днів після цього для профілактики рецидиву захворювання. При тифоїдних захворюваннях, інфекційному ендокардиті, туберкульозі лікування триває значно довше, так як вони можуть рецидивувати через значний проміжок часу після клінічного одужання. Одноразове введення антибіотика з метою профілактики при більшості хірургічних втручань є цілком достатнім. Пересічна тривалість курсів антибактеріального лікування при різних інфекційних процесах наведена у додатку 8.
VI. Контроль за виліковуванням.
При деяких інфекціях (наприклад, сечовивідних шляхів, туберкульозному процесі тощо) після проведеного курсу лікування необхідно проводити бактеріологічний контроль санації організму (його звільнення від збудника).
VII. Моніторинг і Профілактика негативних побічних реакцій і ускладнень.
VIII. Вирішення питання про доцільність комбінованої антибіотикотерапії з урахуванням явищ синергізму та антагонізму між препаратами.
Максимально об’єктивізувати результати бактеріологічного дослідження допомагають сучасні Методи забору біологічного матеріалу. Але навіть при їх застосуванні у 30-50 % випадків не вдається ідентифікувати причинний мікроорганізм. Крім того, рутинні мікробіологічні дослідження не дають можливості визначати більшість збудників, які є актуальними в наш час.
Тому значного поширення в Україні й за кордоном отримала Емпірична антибактеріальна терапія.
Сучасна Класифікація хіміотерапевтичних препаратів, яка враховує особливості хімічної будови, механізму та спектра дії, включає такі групи цих засобів:
Антибіотики
I. Бета-лактамні антибіотики:
A. Пеніциліни.
Б. Інгібітори бета-лактамаз і комбіновані препарати, до складу яких вони входять.
B. Цефалоспорини.
Г. Монобактами.
Д. Тієнаміцини (карбапенеми).
II. Макроліди, азаліди, стрептограміни, пристинаміцини.
III. Лінкозаміди.
IV. Тетрацикліни.
V. Аміноглікозиди.
VI. Хлорамфеніколи.
VII. Глікопептиди.
VIII. Циклічні поліпептиди (поліміксини).
IX. Фторхінолони.
X. Інші антибіотики.
XI. Протипухлинні антибіотики.
Нітроімідазоли
Нітрофурани
Сульфаніламіди
Диамінопіримідини
Антимікобактеріальні препарати
Протигрибкові препарати
Противірусні препарати
У даному посібнику ми обмежимося розглядом антибактеріальних антибіотиків (I-X групи вищевказаних препаратів).
Бета-лактамні антибіотики (бета-лактами) - найбільша група антимікробних препаратів, які об’єднує наявність в їх хімічній структурі бета-лактамного кільця, яке відповідальне за антимікробну активність. При руйнуванні бета-лактамного кільця антимікробна дія зникає. Залежно від будови другої частини біциклічного кільця бета-лактами поділяються на пеніциліни, цефалоспорини, карбапенеми і монобактами (рис. 1).
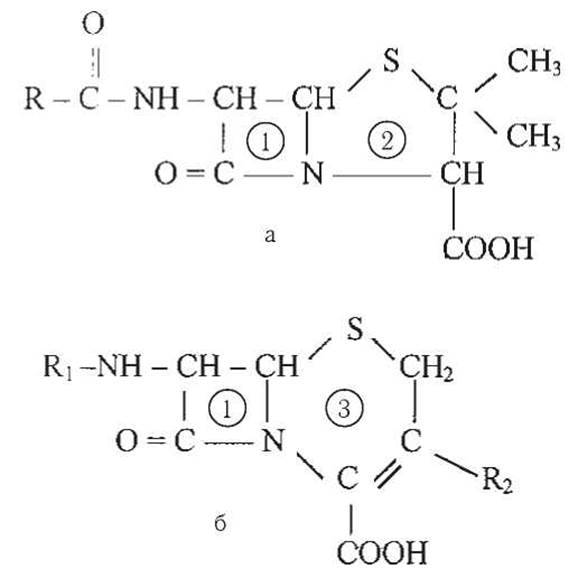
Puc. 1. Хімічна структура пеніцилінів (а) і цефалоспоринів (б)
1 - бета-лактамне кільце; 2 - тіазолідинове кільце; 3 - дигідротіазинове кільце.
Последнее обновление: 05/02/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.