Медична радіологія - Лазар А.П. 2008
Променеве терапія
Джерела іонізуючих випромінювань
Методи променевої терапії поділяють на дві основні групи: дистанційні та контактні.
При дистанційному опроміненні джерело випромінювання знаходиться на відстані від хворого. До дистанційних методів опромінення належать: дистанційна гамма-терапія, рентгенотерапія, терапія гальмівним випромінюванням високої енергії, терапія швидкими електронами (бета-терапія), протонна терапія.
При контактній променевій терапії (або брахітерапія, brachytherapy) джерело випромінювання прилягає до патологічного вогнища. Це здійснюється шляхом розміщення радіоактивних препаратів на поверхні ділянки, яку опромінюють (аплікаційний метод), Введення їх у порожнину органа (внутрішньопорожнинний метод), безпосередньо у тканину пухлини (внутрішньотканинний метод), в Організм хворого з наступним накопиченням в ураженому органі (метод вибіркового накопичення).
Для Лікування деяких захворювань поєднують одночасно або послідовно дистанційне і контактне опромінення. Така Методика дістала назву поєднаної променевої терапії.
У медичній практиці у якості джерел іонізуючих випромінювань застосовуються природні та штучні радіоактивні елементи, рентгенівські апарати і прискорювачі різних видів іонізуючих випромінювань.
Їх можна класифікувати таким чином.
I. Радіоактивні речовини.
1. Закриті.
А. Гамма-терапевтичні установки.
Б. Радіоактивні препарати (трубочки, кульки, голки, дроти).
2. Відкриті (розчини, суспензії, порошки).
II. Прискорювачі заряджених часток.
1. Лінійні.
2. Циклічні (бетатрони, циклотрони, синхрофазотрони).
III. Рентгенівські апарати.
1. Далекодистанційні.
2. Короткодистанційні.
Радіоактивні елементи при своєму розпаді випромінюють альфа- і бета-частинки. Альфа- і бета-розпад, як правило, супроводжується випромінюванням гамма-квантів. Залежно від поставленої мети в практичній медицині для діагностики або для променевої терапії використовуються випромінювання бета-часток або гамма-випромінювання.
Радіоактивні речовини за характером застосування в медичній практиці поділяються на дві групи: відкриті та закриті радіоактивні препарати.
Відкриті радіоактивні препарати являють собою розчини, суспензії та порошки радіоактивних елементів у різних хімічних сполуках. Як відкриті радіоактивні препарати в медицині набули великого поширення штучні радіоактивні ізотопи йоду (131I), фосфору (32P), золота (198Au). Відкриті радіопрепарати можуть розлитися, випаритися, розсипатися, осісти на поверхні. Тому захист від них складніший, необхідні жорсткіші умови зберігання, транспортування та застосування.
Закриті радіоактивні препарати являють собою радіоактивні елементи, вміщені в металеві оболонки у вигляді трубочок, голок, гранул, дисків, дротів та ін. Металеві оболонки закритих радіоактивних препаратів виконують роль фільтрів для відсіювання м’якого випромінювання даного елемента. Кожний радіоактивний препарат має оболонку з певного металу: радій міститься в платинових оболонках, кобальт - у трубочках з нержавіючої сталі.
Для закритих радіоактивних препаратів використовують природні і штучні елементи: радій, кобальт, цезій та ін. До закритих радіоактивних препаратів належать і гамма-терапевтичні стаціонарні установки, де застосовуються штучні радіоактивні ізотопи кобальту або цезію, радіоактивний розпад яких супроводиться гамма-випромінюванням.
Найрозповсюдженіше джерело гамма-випромінювання - радіоактивний ізотоп кобальту, період напіврозпаду якого 5,24 роки, енергія випромінювання - 1,17 і 1,33 (в середньому - 1,25) МеВ. Для отримання джерела заготовку зі стабільного ізотопу 59Со поміщають у гарячу зону реактора, де під впливом теплових нейтронів відбувається накопичення радіоактивного 60Со. Потім з цих заготовок набирають джерела необхідної сумарної активності і розміру, поміщають в ампули з нержавіючої сталі і запаюють. Радіоактивний кобальт може бути застосований у вигляді гранул діаметром 0,7 мм, завдовжки 3 мм, з активністю кожної 0,3-0,5 мг-екв радію. Для поглинання бета- випромінювання гранули покривають шаром неактивного золота товщиною 0,05 мм. Відрізками 60Со заповнюють нейлонові трубочки із зовнішнім діаметром 1,3мм і внутрішнім 0,8мм; вони застосовуються при внутрішньотканинному методі лікування. У вигляді джерел великої активності 60Со використовують для дистанційної гамма-терапії.
Інші радіоактивні джерела мають як переваги, так і недоліки. Так, 137С8 характеризується тривалим періодом напіврозпаду (30 років), але низькою питомою активністю. Навпаки, 192Ir, що широко застосовують для контактного опромінення, має високу активність (3-5 мг-экв радію), що дозволяє виготовляти джерела у вигляді тонкого (діаметром 0,6 мм) дроту та голок, але короткий період напіврозпаду (74 дні), внаслідок чого необхідно часто змінювати джерела. Розпад радіоактивного золота 198 Аu (Т=2,69 дні) супроводжується переважно бета-випромінюванням із максимальною енергією 0,96 МеВ і гамма-випроміненням з енергією 0,41 МеВ. Радіоактивне золото застосовується у вигляді колоїдного розчину або гранул, вкритих шаром платини товщиною 0,1 мм для поглинання бета-випромінювання.
Порівнювальний аналіз ізодозних карт різних радіотерапевтичних апаратів, що продукують випромінювання різної природи та енергії (мал.314), дозволяє зробити низку важливих для Планування променевої терапії висновків.
Рентгенівське випромінювання (Х-проміння), яке генерується при анодній напрузі 30-200 кВ, обумовлює максимум поглинутої дози на поверхні тіла людини, тому найсильніше опромінюється Шкіра. На глибині тканин доза значно зменшується. При анодній напрузі 40 кВ доза на глибині 3 см складає всього 10% від дози на поверхні. При анодній напрузі 200 кВ випромінення проникає глибше, але й тут на глибині 10 см залишається тільки 20% від поверхневої дози. Тому рентгенівські установки використовують тільки для опромінення пухлин, що знаходяться на поверхні.

Мал. 314. Дозовий розподіл у тканинах різних видів іонізуючого випромінювання:
Х - рентгенівського;
Y - гамма;
Г - гальмівного;
Е - електронного;
П - протонного;
Н - нейтронного.
Змінюючи показники напруги та фільтри рентгенівського апарату можна генерувати випромінювання різної проникаючої здатності. Далекодистанційну рентгенотерапію здійснюють на відстані джерело- поверхня шкіри більше 30 см (мал.315). Сила струму при цьому не змінюється і становить близько 10 мА. Поверхнева рентгенотерапія застосовується при розташуванні патологічного вогнища на глибині до 1 см від поверхні шкіри; використовується напруга на трубці 100-120 кВ, алюмінієвий фільтр завтовшки 3 мм, ВДП - 30 см. Напівглибока рентгенотерапія застосовується при розташуванні патологічного вогнища на глибині до 3 см від поверхні шкіри; використовується напруга 140-160 кВ, мідний фільтр завтовшки 0,5 мм та алюмінієвий фільтр завтовшки 3 мм, ВДП - 40-50 см. Глибока рентгенотерапія застосовується при розташуванні патологічного вогнища на глибині до 5 см від поверхні шкіри; використовується напруга 180-230 кВ, мідний фільтр завтовшки 1,0 мм та алюмінієвий фільтр завтовшки 5,0 мм, ВДП - 40-50 см. Для обмеження поля опромінення необхідних розмірів та форми у вихідному вікні рентгенівської трубки встановлюють спеціальні тубуси зі свинцевими стінками (мал. 316).

Мал.315. Рентгено-терапевтичний апарат РУМ-11.
Для короткодистанційної рентгенотерапії використовуються рентгенотерапевтичні апарати з виносним анодом у вигляді циліндричного стрижня. Виносний анод може використовуватися також для внутрішньопорожнинної терапії. Відстань від джерела до поверхні при короткодистанційній рентгенотерапії становить від 1,5 до 30 см (найчастіше - 10 см), напруга на трубці регулюється від 8 до 100 кВ. Застосовується короткодистанційна рентгенотерапія при розташуванні патологічного вогнища на глибині до 0,5-0,7 см від поверхні шкіри. Різновидом короткодистанційної рентгенотерапії є ультрам’яка рентгенотерапія, коли при напрузі від 10 до 20 кВ генеруються так звані промені Буккі. Проникна здатність променів Буккі в Тканини тіла людини не перевищує 1,5 мм. Ці промені застосовують при лікуванні гіперкератозу та поверхнево розташованих запальних процесів - дерматитів, блефаритів, кон’юктивітів.
Гамма-терапевтичні установки, заряджені 60Со активністю 20004000 Кu, випромінюють майже однорідний пучок фотонів великої енергії (1,25 МеВ). Максимум поглинання знаходиться на 0,5 см вглиб, що зменшує опромінення шкіри. На глибині 10 см залишається не менш 50% поверхневої дози. Тому глибинні дози вищі, ніж при використанні рентгенотерапевтичних установок.

Мал. 316. Набір фільтрів та тубусів для рентгенотерапії.

Мал. 317. Гамма-терапевтичний апарат.
А - зовнішній вигляд; Б - будова радіаційної головки;
1 - затвор;
2 - діафрагма;
3 - джерело 60Со.
Апарати для дистанційної гамма-терапії типу «АГАТ-Р», «Рокус», «Theratron» мають радіаційну головку з коліматором, що регулює розмір поля опромінення, і світловий центратор. Радіаційна головка апарата може обертатися навколо хворого, що полегшує укладання хворого і центрацію пучка (мал. 317). До апаратів додається комплект знімних частин, що включає набір захисних та клиноподібних блоків з поворотним пристроєм, решітчасті фільтри та растри з різним співвідношенням закритих і відкритих ділянок, додаткові коліматори, що дозволяють широко варіювати способи у-опромінення при різних злоякісних новоутвореннях (мал. 318, 319).

Мал. 318. Клиноподібні блоки. 1 - різні види блоків; 2 - дистанційна гамма-терапія раку стравоходу:
А - без застосування блоків;
Б - з клиноподібними блоками.

Мал. 319. Додаткові фільтри та блоки для дистанційної гамма-терапії.
А - решітчасті фільтри;
Б - захисні блоки.

Мал. 320. Лінійний прискорювач.
Лінійні прискорювачі електронів (ЛПЕ) і циклічні прискорювачі (бетатрони і мікротрони) з виведенням пучків гальмівного й електронного випромінювання усе ширше застосовують для опромінення хворих зі злоякісними пухлинами (мал. 320). Серед переваг прискорювачів перед у-апаратами можна назвати такі: можливість вибору виду випромінювання (квантове чи електронне), регулювання енергії випромінювання та невеликі розміри пучка електронів (до 0,5мм).
У бетатронах гальмування потоку електронів призводить до формування гальмівного випромінення з енергією від 4 до 40 МеВ. При енергії фотонів 25 МеВ максимум поглинутої дози знаходиться на глибині 4-6 см від поверхні тіла хворого. Тканини, що розташовані на цьому рівні, отримують не більше половини максимальної дози. Але гальмівне випромінювання має недолік - порівняно повільний спад дози за максимумом. Це означає, що здорова тканина позаду пухлини сильно опромінюється.
При отриманні у бетатроні потоку електронів високої енергії максимум поглиненої дози визначається на глибині 1-3 см, після чого доза швидко знижується, і на глибині 10 см тканина практично не опромінюється. Це вигідно для лікування неглибоко розташованих новоутворень. Але для опромінення пухлин, які залягають у глибині тіла, найкраще користуватися пучками важких заряджених часточок (протонів та альфа-часток).
Протонне випромінювання - іонізуюче випромінювання, що складається з важких заряджених часток - протонів. Для медичних цілей використовують протонні пучки, які отримують у великих фізичних прискорювачах. Енергія протонного пучка, що використовується для променевої терапії, коливається від 50 до 1000 МеВ. Основна перевага протонного випромінювання перед гамма-, електронним і гальмівним випромінюваннями полягає в тому, що при проходженні через тканини протони високої енергії мало розсіюються, і це дозволяє використовувати його для селективного ураження пухлин, розташованих у безпосередній близькості від життєво важливих органів. Зазвичай для опромінення застосовуються протони з енергією 70-200 МеВ. Протони високих енергій до моменту «зупинки» в тканинах рухаються практично прямолінійно, при цьому лінійна втрата енергії (ЛВЕ) збільшується, доходячи до максимуму в кінці пробігу (пік Брегга).
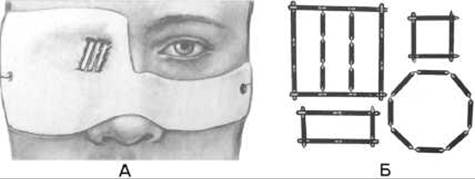
Мал. 321. Аплікаціний метод опромінення.
А - аплікація на обличчі з лінійними радіоактивними джерелами;
Б - схеми розташування у муляжі лінійних радіоактивних джерел.
Медичний протонний комплекс складається з протонного тракту, зали опромінення, де розташована частина магнітних фокусуючих елементів, системи контролю пучка, а також установки для протонної стереотаксичної терапії. Оптимальна ділянка застосування методу - радіонейрохірургія, тобто проведення безкровних операцій на різних ділянках головного мозку. Завдяки можливості формування тонкого пучка з великою дозою опромінення (100-200 Гр) вдається вибірково руйнувати всередині мозку ділянки об’ємом до 1 см і більше, наприклад, пухлину гіпофізу.
До контактних методів променевої терапії належать аплікаційний, внутрішньопорожнинний, внутрішньотканинний, та внутрішній (або метод вибіркового накопичення).
Під час аплікаційного методу променевої терапії використовують аплікатори (від лат. «applicare» - приєднувати). У якості аплікаторів використовують пластмаси, поліетиленові плівки, іонообмінні смоли, в яких розміщуються радіонукліди (мал. 321). Вони моделюються і прикладаються до патологічного осередку. Розрізняють бета- і гамма- аплікатори. Бета-аплікатори застосовуються в офтальмології, вони містять радіонукліди Sr90і Y90. Опромінення відбувається через робочу поверхню аплікаторів, що прикладаються до патологічного осередку в амбулаторних умовах, або фіксуються на визначений час за допомогою операції.
Якщо джерела випромінювання поміщають у порожнину, що знаходиться всередині тіла хворого (Стравохід, Сечовий міхур, Піхва, Матка, пряма кишка та ін.), то спосіб опромінення називають внутрішньопорожнинним (мал. 322). Широке поширення при лікуванні пухлин шиики та тіла матки отримали джерела гамма-випромінення високої активності 60Со, 137Cs, 192Іr. Для проведення внутріпорожнинного опромінення існують спеціальні апарати із програмним керуванням для внутріпорожнинного й аплікаційного опромінення типу «АГАТ-ВУ » (заряд 60Со), «Селектрон» (заряд 137Сs), «Гаммамед» (заряд 192Ir), що дозволяють дистанційно по шлангах переміщати джерела випромінювання в ендостати, заздалегідь поміщені в порожнину (мал. 323). Такий спосіб опромінення називають методом дистанційного послідовного введення ендостата і джерела (англійською - remote after-loading).

Мал. 322. Внутрішньопорожнинне опромінення.
А - лінійні джерела випромінювання у порожнині матки;
Б - дозовий розподіл при використанні лінійного джерела.

Мал. 323. Апарат GammaMed.
Внутрішньотканинне опромінення з використанням закритих джерел здійснюють, вводячи в пухлину провідники у вигляді дроту, голок чи трубочок, в які потім поміщають джерела випромінювання, найчастіше 60Со (мал. 324). Зазвичай під час операції роблять візуальний розподіл провідників, в які потім уводяться за допомогою спеціальної апаратури («Мікроселектрон») радіоактивні джерела. Радіоактивне джерело 125І, активністю 0,8224 мС, може знаходитись у пухлині протягом 6 місяців.
Радіохірургічний метод, як різновид внутрішньотканинного методу, полягає в хірургічному видаленні пухлини з наступним введенням радіоактивних препаратів у тканини ложа пухлини. Радіоактивні препарати, голки або нейлонові трубочки розташовують у м’яких тканинах рани рядами. Щоби препарати не зміщувалися, кожний із них підшивають одним кетгутовим швом. Нейлонові нитки не потребують додаткової фіксації, тому що тканини прошивають ними. Після введення радіоактивних препаратів рану зашивають, а нитки від кожного препарату або кінця нейлонових трубочок виводять у проміжки між швами. По закінченні експозиції, через 5-7 днів препарати видаляють. Загальна доза може варіювати, в залежності від радикальності операції, від 45 до 60 Гр. Під час операції можна застосовувати також інтраопераційне опромінення пучком електронів (Intraoperative Electron Beam Radiotherapy - IOERT) (мал. 325).
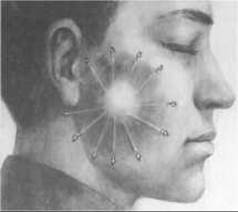
Мал. 324. Внутрішньотканинне опромінення пухлини привушної залози.

Мал. 325. Інтраопераційне бета-опромінення.
1, 3 - проведення опромінення; 2 - схема опромінення на комп’ютерній томограмі.
Опромінення відкритими рідкими радіонуклідами (внутрішній метод) проводять шляхом безпосереднього введення радіоактивної речовини в організм у вигляді справжнього чи колоїдного розчину перорально, у порожнину, пухлину чи судину (мал. 326). Застосування водних розчинів солей 32Р і 131І основане на їхній здатності вибірково накопичуватися переважно у визначених тканинах (фосфор - у кістковому мозку, йод - у щитоподібній залозі) незалежно від шляху введення, тому ці радіонукліди застосовують для лікування захворювань крові, раку щитоподібної залози з метастазами. Колоїдні розчини 198Аu частіше використовують для внутрішньопорожнинного, внутрішньопухлинного і внутрішньолімфатичного введення. Для введення радіоактивного золота в ділянку операційного рубця попередньо вводять порожнисті довгі голки, після чого до голки приєднують канюлю шприца з розчином колоїдного золота. Розчин уводять при одночасному поступовому витягу голки.
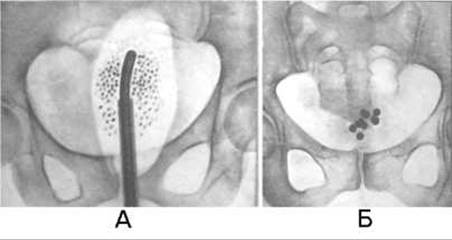
Мал. 326. Внутрішньо-порожнинне опромінення на рентгенограмах.
А - балон з макросуспензією радіоактивного препарату у прямій кишці;
Б - кульки з радіоактивного кобальту у сечовому міхурі.

Мал. 327. Стереотаксичний прилад.
Последнее обновление: 05/02/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.