Медична генетика - В. М. Запорожан 2005
Методи діагностики спадкових хвороб
Молекулярно-генетичні методи (методи ДНК-діагностики)
Етапи ДНК-діагностики з використанням полімеразної ланцюгової реакції
Сьогодні одним з основних методів ДНК-діагностики є Полімеразна ланцюгова реакція (ПЛР). Метод було розроблено в 1983 р. К. Мюллісом (США). За розробку цього методу в 1993 р. йому було присуджено Нобелівську премію в галузі хімії.
Метод грунтується на ампліфікації (тобто багатократній редуплікації) in vitro певної ділянки ДНК завдовжки від кількох десятків до тисячі та більше пар нуклеотидів. Це дозволяє протягом 35 год одержати велику кількість копій потрібної послідовності ДНК. Ідентифікація такої великої кількості копій ДНК надалі не є дуже складною. Як матриця придатна будь-яка ДНК, виділена з різних джерел. Головними перевагами методу ПЛР є таке:
— ампліфікація потрібної ділянки ДНК, навіть якщо аналізований препарат недостатньо очищений або є складною сумішшю молекул. Саме такими препаратами є зразки крові, сечі, ексудатів, мокротиння та інших середовищ організму, а також бактерійні культури;
— ампліфікація ДНК, що міститься в зразку в дуже малих кількостях. По суті, як стартовий матеріал для ПЛР достатньо взяти не тільки одну клітину, але й одну молекулу. Це важливо при дослідженні проб повітря, води тощо на наявність патогенних збудників захворювань, фрагментів тканин людини для судово-медичних досліджень;
— можливість довгострокового зберігання матеріалу для дослідження у зв’язку зі стійкістю молекули ДНК.
Розрізняють такі етапи ДНК-діагностики з використанням полімеразної ланцюгової реакції.
1. Виділення ДНК. Для проведення ампліфікації не потрібна велика кількість матричної ДНК, придатні навіть невеликі фрагменти слабоочищеної ДНК, в принципі може бути достатньо навіть однієї молекули. Як правило, ДНК із біологічного матеріалу виділяють методами лізису клітин з подальшим очищенням від білкових компонентів. Для підвищення чутливості реакції ДНК можна сорбувати на іонообмінних смолах.
2. Полімеразна ланцюгова реакція, яка дозволяє вибірково ампліфікувати (багатократно редуплікувати) потрібну ділянку ДНК у мільйони разів.
Необхідною умовою для проведення ПЛР є знання нуклеотидної послідовності ампліфікованої ділянки ДНК, оскільки специфічний вибір цієї ділянки здійснюється шляхом гібридизації матричної ДНК з двома штучно синтезованими праймерами. Праймери — олігонуклеотидні послідовності ДНК завдовжки від 15 до 30 п. н., комплементарні 3'-кінцям ампліфікованої ділянки на змістовому й антизмістовому ланцюгах ДНК відповідно. Таким чином, відстань між праймерами визначає довжину синтезованих фрагментів ДНК.
По суті, метод ПЛР імітує природний процес редуплікації ДНК у клітинах. До складу реакційного розчину вводять ДНК обстежуваної людини, чотири види нуклеотидів ДНК (dNTP — дезоксирибонуклеотид-трифосфати), а також термостабільну ДНК-полімеразу (Taq-полімеразу), яка зберігає свою активність при високій температурі. Цей фермент було виділено з бактерій, які живуть у гарячих джерелах (Thermus aquaticus). Оптимум роботи ферменту — при температурі +72 °С.
Реакція відбувається у спеціальній буферній суміші з певними концентраціями іонів калію, хлору, магнію і точним значенням рН.
Полімеразна ланцюгова реакція відбувається циклічно. Кожен цикл має три фази (рис. 10.7):
1) денатурація (плавлення) — суміш нагрівають до 90-95 °С. При цьому відбувається розрив водневих зв’язків, що з’єднують два ланцюги ДНК, і ДНК перетворюється на однониткову форму;
2) гібридизація (відпал) — суміш охолоджують до 45-60 °С, праймери з’єднуються з комплементарними ділянками ДНК;
3) синтез — суміш знову нагрівають до 72 °С, починає працювати термостабільна ДНК-полімераза, і синтезується дочірній ланцюг ДНК. ДНК-полімераза добудовує нитку нуклеотидів комплементарно матричній ДНК, причому Синтез ДНК йде від місця гібридизації праймера у напрямі 3'5'. При цьому праймер включається до складу щойно синтезованої ділянки нуклеїнової кислоти. У подальших циклах нові синтезовані молекули ДНК стають, у свою чергу, матрицею для аналогічного синтезу нових копій. Оскільки синтез кожного з двох антипаралельних ланцюгів ДНК розпочинається від місця гібридизації праймера, це місце і стає межею синтезованої ділянки.
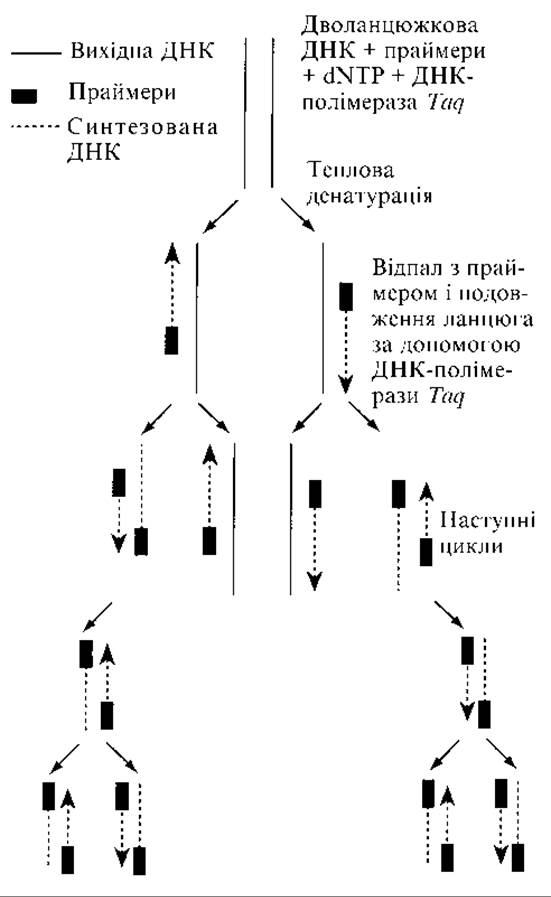
Рис. 10.7. Полімеразна ланцюгова реакція (збільшення кількості копій ДНК у геометричній прогресії)
Якщо уявити собі, що в реакційній суміші знаходилася одна молекула ДНК з ділянкою, яку необхідно редуплікувати, то після першого циклу одержують 2 молекули, після другого циклу — 4 і т. ін. Тобто кількість копій ДНК збільшується в геометричній прогресії.
Кількість вказаних циклів у ПЛР становить зазвичай від 25 до 30. У результаті кількість копій ДНК збільшується в мільйони разів.
Суміш ставлять у спеціальний прилад — термоциклер (ампліфікатор). У ньому автоматично відбувається зміна температур, необхідних для реакції.
Переваги ПЛР:
— значне (у 2-10 разів) скорочення витрат праці та часу;
— висока точність, принципова неможливість отримання хибнопозитивних результатів;
— можливість проведення дослідження на вкрай малому (кілька мікролітрів) об’ємі матеріалу;
— простота підготовки матеріалу до дослідження; може використовуватися практично будь-яка тканина або рідина організму.
Проведення ПЛР-діагностики вимагає ретельного дотримання всіх санітарно-гігієнічних норм для уникнення забруднення зразків чужорідною ДНК, спеціально обладнаних лабораторій і навченого персоналу.
3. Аналіз одержаних результатів. Подальший аналіз ампліфікованих фрагментів ДНК передбачає дослідження конкретних особливостей ампліфікованого фрагмента. Фрагменти з нормальною і мутантною послідовностями можуть відрізнятися за електрофоретичною рухливістю, тому часто проводиться електрофорез ампліфікованих фрагментів у гелі (10.4.5.2). Водночас проводять електрофорез контрольних фрагментів ДНК. У гель додають бромистий етидій (барвник, який забарвлює ДНК). Фрагменти ДНК переміщаються на певну відстань. Ділянки гелю, в яких знаходяться фрагменти ДНК, даватимуть оранжеве світіння при ультрафіолетовому освітленні. Збіг смуг контрольного і дослідного фрагментів дозволить діагностувати наявність шуканого гена. Гель можна сфотографувати або його зображення перенести на екран комп’ютера (рис. 10.8).
Для ідентифікації ампліфікованих фрагментів можна використати Методи секвенування, а також метод алель-специфічних олігонуклеотидів. Він грунтується на гібридизації ампліфікованих фрагментів ДНК з міченими олігонуклеотидами, комплементарними нормальній або мутантній послідовності ДНК. Прикладом такого підходу є застосування ДНК-чіпів.
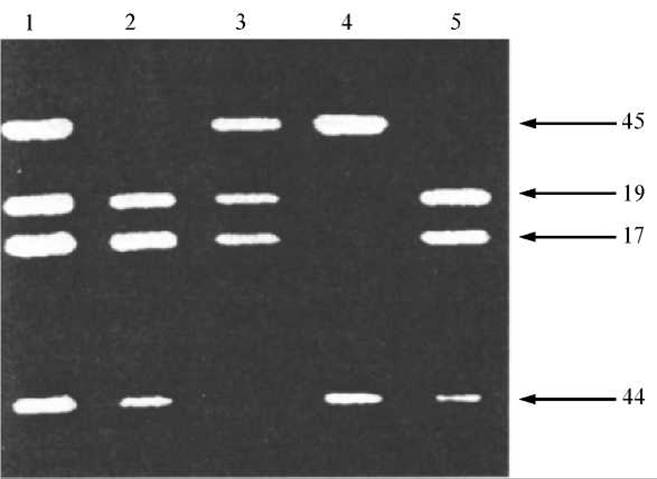
Рис. 10.8. Пряма ДНК-Діагностика м’язової дистрофії Дюшенна за допомогою мультиплексної полімеразної ланцюгової реакції. У кожної з обстежуваних осіб одночасно ампліфіковано 4 екзони гена дистрофіну. Екзони 17, 19, 44 і 45 відмічено стрілками. Доріжка 1 — контроль, видно всі чотири екзони. Доріжки 25 — хворі на м’язову дистрофію Дюшенна з різними делеціями гена дистрофіну (доріжки 2 і 5 — делеція екзона 45, доріжка 3 — делеція екзона 44, доріжка 4 — делеція екзонів 17 і 19)
Последнее обновление: 05/02/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.