Фізіологія рослин - Мусієнко М.М. 2001
Дихання
Каталітичні системи дихання
Оксидоредуктази
Окислювальний апарат рослин характеризується своїми специфічними особливостями. Насамперед, на відміну від тварин, для нього характерна делокалізація дихального апарату (Мітохондрії, пероксисома, Цитоплазма та ін.). По-друге, для нього характерна поліфункціо- нальність, тобто наявність каталізаторів, що характеризуються багатьма властивостями. Нарешті, для окислювального апарата рослин характерний принцип, коли в організмі знаходяться не один, а кілька ферментів, які каталізують ті самі, або близькі реакції. Як відомо, біологічне окислення будь-якої речовини передбачає втрату нею електронів або електронів разом з протонами. В рослинній клітині відбуваються окислювальні реакції трьох типів.
І. Реакції, в яких спостерігається безпосередня втрата електрона в результаті зміни його валентності. Такі реакції каталізують Ферменти оксидази, в активних центрах яких є метали:
![]()
II. За рахунок відняття від окислюваної речовини водневих іонів за допомогою ферментів гідроксилаз. Роль акцепторів протонів в таких реакціях часто виконує сам кисень:
![]()
III. Пряме окислення молекулярним киснем за допомогою оксигеназ або трансфераз:
![]()
У біологічних системах всі ці шляхи взаємопов’язані, причому втрата електрона при окисленні супроводжується, як правило втратою і водню. Саме тому процес окислення певної речовини в живих системах поєднується з відновленням іншої.
Щоб знати напрямок руху електронів, введено поняття стандартного відновного потенціалу (Ео). За нуль потенціалу умовно прийнято відновний потенціал реакції:
![]()
Мірою електрон-донорної та електрон-акцепторної здатності оечовини є величина окислювально-відновного потенціалу, вираженого у вольтах (табл. 9). Всі біологічні окислю-
Таблиця 9. Стандартні окислювально-відновні потенціали біохімічних систем
|
Система |
Е0’ (pH 7,0), В |
Система |
Е0’ (pH 7,0), В |
|
Кисень/Вода |
0,81 |
ФМН/ФМН Н2 |
-0,12 |
|
Цитохром a (Fe +3/Fe+2) |
0,29 |
Оксалацетат/малат |
-0,17 |
|
Цитохром c (Fe +3/Fe+2) |
0,22 |
Рибофлавін (окисл./відн.) |
-0,21 |
|
Цитохром b (Fe +3/Fe+2) |
0,12 |
над+/надн+н + |
-0,32 |
|
Убіхінон (окисл./відн.) |
0,10 |
ГІіруват/малат |
-0,33 |
|
Дегідроаскорбат/аскорбат |
0,08 |
Н/1/2Н2 |
-0,42 |
|
Фумарат/сукцинат |
0,03 |
Фередоксин (окисл./відн.) |
-0,43 |
|
Сукцинат/ α-кетоглутарат |
-0,67 |
вально-відновні системи можуть бути розміщені в певний ряд за величиною їх окислювально- відновного потенціалу.
Знання стандартних окислювально-відновних потенціалів різних біологічних систем дозволяє передбачити напрямок потоків електронів від однієї окислювально-відновної системи до іншої. Звичайно, перенесення електронів здійснюється від системи з більш від’ємним окислювально-відновним потенціалом до системи з більш позитивним потенціалом. Для перенесення електронів у зворотному напрямку необхідно затратити енергію.
Системи з більш високим еле*ктровід'ємним потенціалом характеризуються більшим запасом енергії. Відновлення речовини поєднується із зміною положення енергетичних рівнів її. При відновленні, одночасно з набуттям електрону, проходитть збільшення енергії системи. Повністю окислені сполуки характеризуються мінімальним вмістом вільної енергії. Кількість вільної енергії, яка може запасатися або звільнятися, прямо пропорційна різниці окислювально-відновних потенціалів двох систем, що беруть участь в перенесенні електронів.
Чим більш від’ємна величина відновного потенціалу, тим більша здатність даної речовини віддавати електрони (окислюватися) тобто бути відновником. Навпаки, чим більш позитивний відновний потенціал певної речовини, тим вище її здатність приймати електрони (відновлюватися, тобто бути окислювачем).
Універсальним окислювачем є О2, який має максимальний позитивний потенціал (+0,817 В), а роль донорів виконують різні речовини. Всі електрони транспортуються до Ог через багатокомпонентну окислювально-відновну систему. Перелічені особливості лежать в основі функціонування всіх без винятку груп ферментів, які каталізують процеси аеробного Дихання (рис. 85). Так як окислення донора електрону і протонів поєднується із відновленням їх акцептора, ферменти, що каталізують ці реакції, називають оксидоредуктазами. Оксидази здатні передавати електрони тільки до кисню.
Дегідрогенази. Окислення органічних речовин в рослинній клітині здійснюється за участю дегідрогеназ та оксидаз. Роль дегідрогеназ — активування і передача водню (електронів) субстратів дихання. За характером дії їх ділять на аеробні та анаеробні. Аеробні переносять водень безпосередньо на О2, а анаеробні — на певний акцептор, в ролі якого часте виступає інша дегідрогеназа, але не О2.
![]()
В рослинних мітохондріях НАД знаходиться у великій кількості, наприклад, порівняно з цитохромом с його більше майже в 40 разів.
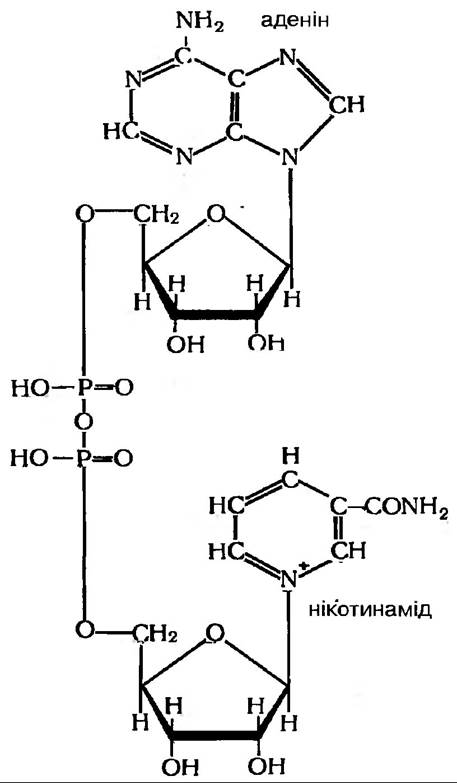
Анаеробні дегідрогенази — це протеїди, двокомпонентні ферменти, коферментами яких виступають НАД+ або НАДФ+. Залежно від білкового носія, до якого приєднується кофермент НАД або НАДФ, розрізняють більше 150 піридинових дегідрогеназ. Субстратна специфічність ферменту визначається білковим компонентом його. В основі дії цих ферментів лежить здатність піридинового ядра, що входить до складу коферментів цих дегідрогеназ у вигляді аміду нікотинової кислоти, приймати та віддавати водень.
Така дегідрогеназа, приймаючи чи віддаючи водень або електрони здатна до окислювально-відновних перетворень. Окислена дегідрогеназа має максимум поглинання в області 260 нм, а відновлена характеризується появою другого максимуму при 340 нм, редокспотенціал НАД×Н (-0,32 В).
Анаеробна дегідрогеназа каталізує перенесення атома водню разом із зв’язаними з ним електронами у вигляді гідрид-іону Н' від молекули субстрату (АН2) до позитивно зарядженого атому четвертого вуглецю НАД(Ф)+, утворюючи внаслідок цього НАД(Ф)Н; електронна пара Н+ стає зв’язуючою парою заново утвореного ковалентного зв’язку С4 → Н. Субстрат, який втратив Н від одного із своїх атомів стає позитивно зарядженим АН+, який стабілізується, віддаючи FT в навколишнє водне середовище:
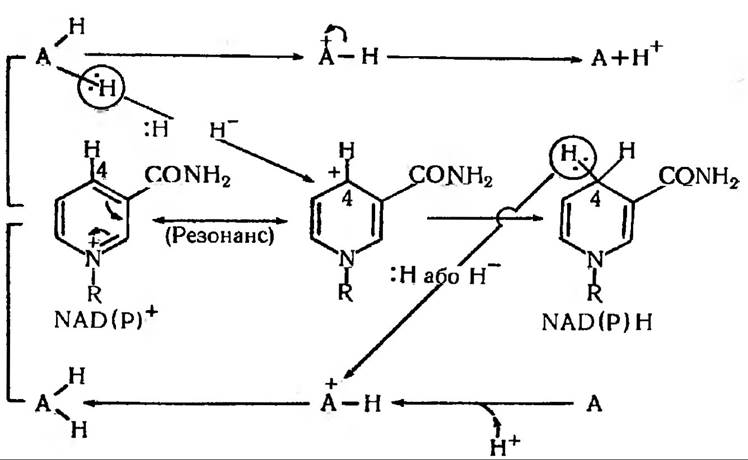
Таким чином, НАД(Ф)+ та НАД(Ф)×Н+ відрізняються наявністю або відсутністю одного гідрид-іону, який еквівалентний двом електронам та одному протону Н+. Звідси легко зрозуміти, чому НАД та НАДФ відносять до переносників водню та двохелектронних окислювально-відновних сполук. Необхідно враховувати, що НАД і НАДФ можуть приймати водень і електрони лише у тих випадках, коли субстрат має більш від’ємне значення потенціалу в порівнянні з ними.
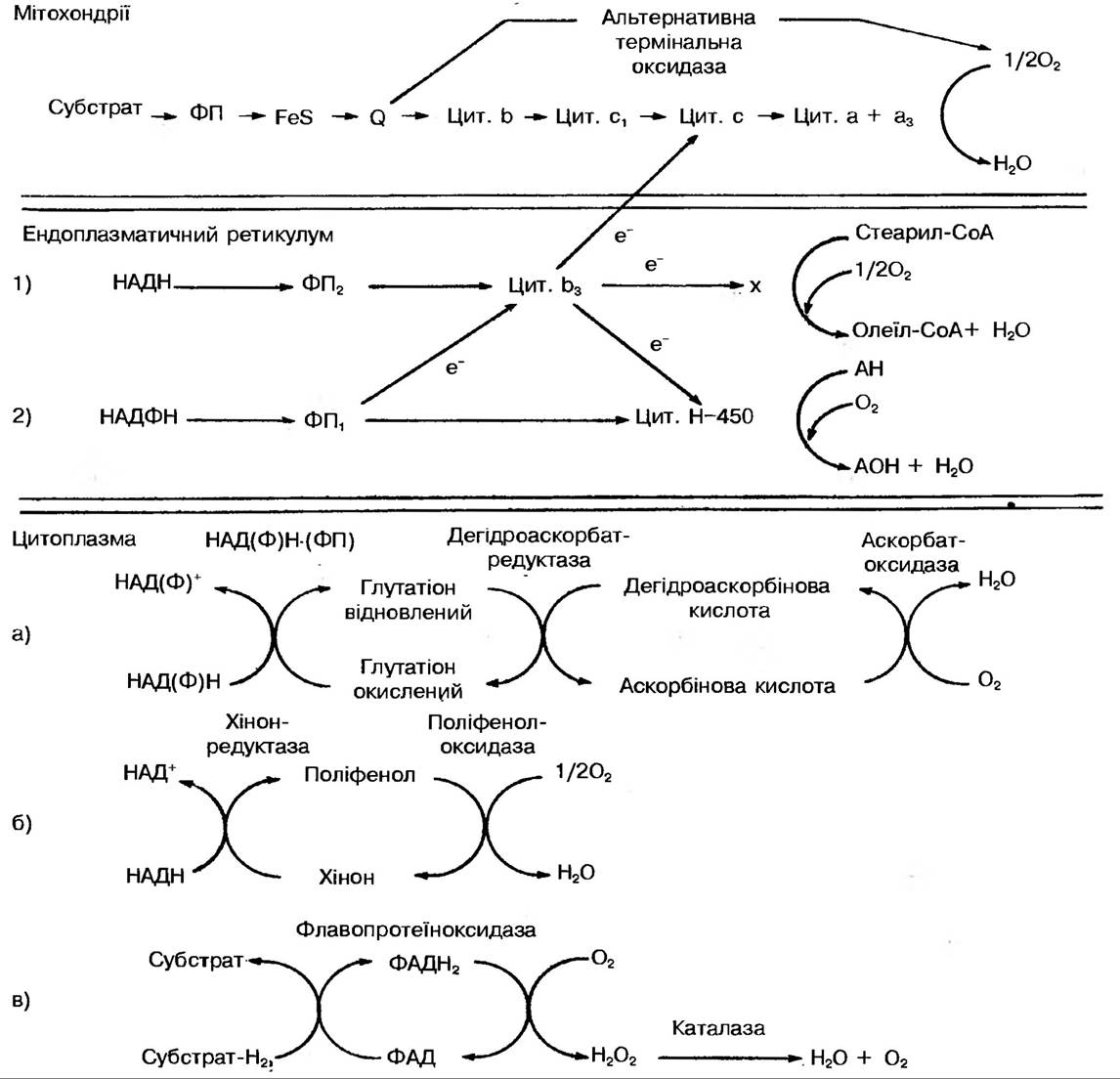
Рис. 85. Редокс-системи рослинних клітин
Піридинові дегідрогенази досить широко розповсюджені як у рослинних, так і в тваринних організмах.
Для багатьох НАД- та НАДФ-залежних дегідрогеназ необхідна присутність іонів двовалентних металів. Наприклад, фермент алкогольдегідрогеназа містить в своєму складі іони цинку. Окислені та відновлені форми коферментів їх здатні до взаємоперетворень за участю фермента НАДФ-трансгідрогенази.
Незважаючи на структурну подібність, НАД- і НАДФ-дегідрогенази не можуть заміщати один одного: до НАД-дегідрогеназ належать дегідрогенази яблучної, молочної кислот, етилового спирту, а до НАДФ-дегідрогеназ — дегідрогеназа глюкозо-6-фосфату, ізоцитратдегідрогеназа та ін. Слід зазначити існування обмеженої групи дегідрогеназ, які активні і за відсутності коферментів.
Аеробні дегідрогенази — це також двокомпонентні ферменти, їх ще називають флавінови- ми дегідрогеназами (флавопротеїни). їх функціональна роль — проміжне транспортування протонів, віднятих від окислювального субстрату або відновленої форми анаеробної дегідрогенази, на О2 або до оксидаз — поліфенолоксидазної чи цитохромної систем.
В ролі простетичної групи в них виступає похідне вітаміну В2 (рибофлавіну) — флавінаде- ніннуклеотид (ФАД) і флавінмононуклеотид (ФМН). Активною частиною флавінових дегідрогеназ є ізоалоксазинове кільце, до якого і приєднуються 2Н (2Н++2е-):
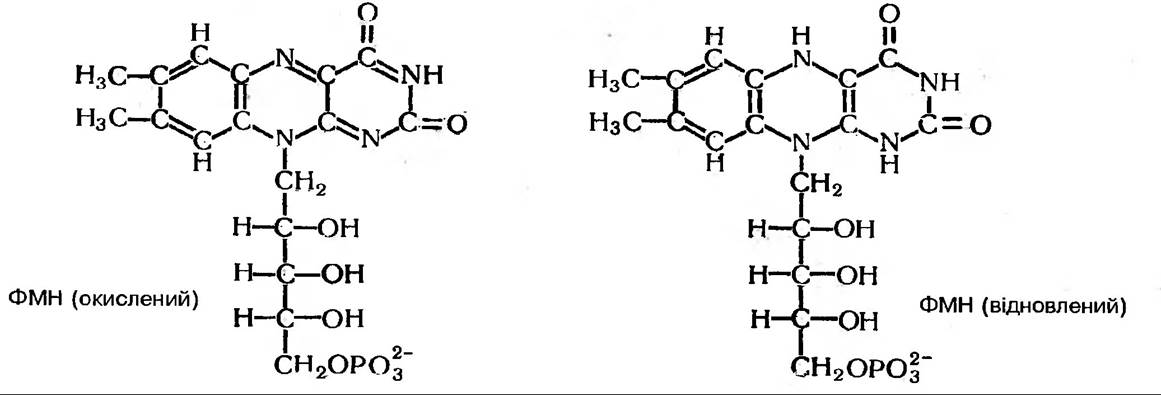
Простетичні групи у флавінових дегідрогеназ міцно приєднані до білкового носія.
Майже всі флавопротеїни (ФП) мають в своєму складі метали (Fe, Сu, Мо, Мn). Прикладом дегідрогенази, до складу якої входить ФАД є сукцинатдегідрогеназа. Флавопротеїни переносять водень від НАД×Н2 (зрідка від НАДФ×Н2) ДО коферменту Q, при цьому ФМН та ФАД як проміжні акцептори приймають обидва протони та обидва електрони:
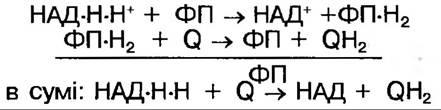
У відновленій формі ФМН×Н2 та ФАД×Н2 безбарвні.
Деякі субстрати окислюються безпосередньо флавопротеїновими ферментами, минаючи піридиннуклеотиди, наприклад янтарна кислота. Е’о для ФМН та ФАД становить (-0,21 В). Залежно від зв’язку з іншими апоферментами воно може змінюватись (від + 0,19 до -0,12 В), а інколи навіть досягає (-0,34 В). Донори електронів для аеробних дегідрогеназ — анаеробні дегідрогенази, тоді як акцепторами виступають Хінони, цитохроми, кисень.
Отже, основна функція дегідрогеназ — передача активованого ними водню або електрона якоїсь сполуки іншому акцептору, який має більш високий окислювальний потенціал.
Поряд з безпосереднім дегідруванням молекули субстрату часто спостерігається додаткове попереднє фосфорилування та гідратація тих сполук, які окислюються. Досить часто багато дегідрогеназ поєднуються між собою за допомогою проміжних компонентів електрон-транспортного ланцюга (ЕТЛ).
Оксидази. Це група ферментів, які активують кисень, іншими словами, це аеробні дегідрогенази, які здатні транспортувати електрони від окислювального субстрату лише на О2. При цьому утворюється Н2О, Н2О2 або супероксидний аніон кисню. В першому випадку на О2 переноситься 4е-, у другому — 2е-, в третьому 1е-. Прикладом оксидаз першої групи є цито- хромоксидаза, поліфенолоксидаза, другої групи — флавопротеїнові оксидази, зокрема оксидази амінокислот, третьої — ферменти типу ксантиноксидази. Для Введення молекулярного кисню в окислювальний процес в рослинній клітині існує три механізми:
І — відновлення кисню одно- або двовалентними донорами. Ферменти, що каталізують такого типу реакції, — оксидази. До складу активних центрів їх, як правило, входять залізо або мідь, тобто вони мають гемінову або флавінову групу.
II — відновлення молекулярного кисню двовалентними донорами, що поєднується з включенням утвореного при цьому продукту відновлення в молекулу, яка окислюється. Ферменти, що каталізують ці реакції, відносять до групи оксидаз із змішаними функціями і називають гідроксилазами.
Ill — безпосереднє включення кисню в молекулу тієї сполуки, яка окислюється. Ферменти називають трансферазами, або оксигеназами. Слід нагадати, що всі названі раніше механізми включення кисню в окислювальні процеси були постульовані пероксидною теорією Баха-Палладіна.
Отже, група ферментів-активаторів кисню досить численна. Однак основну роль в цій групі відіграють ферменти, до складу яких входять атоми заліза. Це — двокомпонентні системи, в ролі простетичної групи яких знаходяться залізо-порфірини.
Цитохроми
У 1925 р. Д. Кейлін відкрив групу сполук в рослинній клітині, які дістали назву цитохромів. За своїм складом вони належать до похідних геміну, який містить у собі залізо. Залізо- порфіринова група (гем) в цитохромах міцно зв’язана з білком через атоми сірки амінокислоти цистеїну. (Між іншим, вперше цитохроми в тваринних клітинах відкрив Мак-Мун ще в 1886 р.). Д. Кейлін вважав, що цитохроми переносять електрони від молекули субстрату до О2. У цито- хромі залізо може легко перетворюватися з двовалентного на тривалентне і навпаки. Цитохром добре забарвлений і, отже, характеризується відповідним спектром поглинання. Існує щонайменше 4 класи цитохромів: a, b, с, d, які відрізняються між собою природою простетичної групи,наприклад, цитохроми а мають в своєму складі залізоформілпорфірини, цитохроми б — залізопротопорфірини, d — залізогідропорфірини (рис. 86).
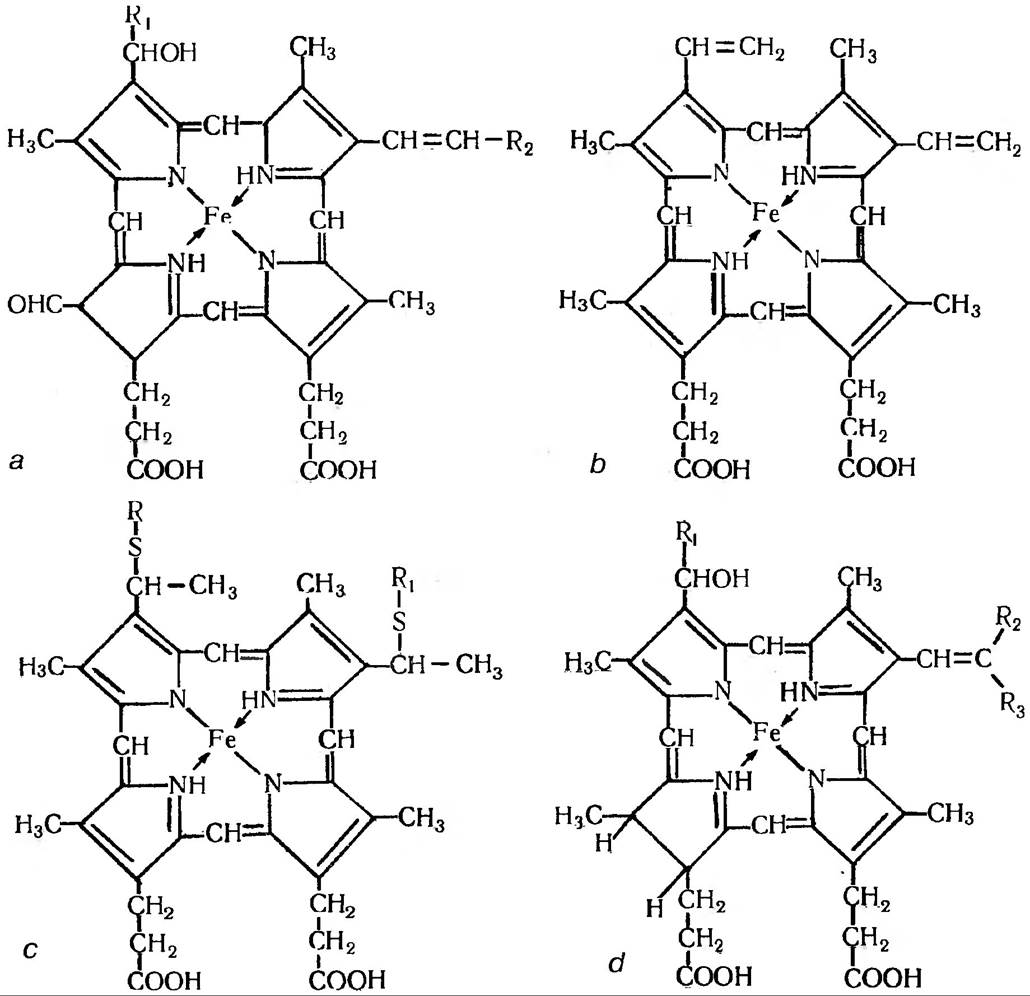
Рис. 86. Будова порфіринів цитохромів а, Ь, с і d
Цитохроми (їх відомо до 20) мають досить широкий окислювально-відновний потенціал від 0 до 0,6 В. Величина окислювально-відновного потенціалу залежить від структури простетичної групи, структури апобілку та способу зв’язку апоферменту з простетичною групою. Найдетальніше вивчено структуру цитохрому с тваринних організмів. В рослинній клітині в мітохондріях виявлено два типи цитохромів с — с547 та С549 з E0 + 0,235 В. Дані про цитохроми групи b в мітохондріях рослин досить суперечливі. До середини 80-х років вважалось, що в рослинних мітохондріях знаходилось три цитохроми b-типу: b557(E0 + 0,075В), b560 (E0 + 0,045 В) та b566 (Е0 + 0,070 В). Потім було одержано дані про наявність в мітохондріях ще двох цитохромів b з максимумами поглинання близько 558 нм.
Відновлені цитохроми окислюються за участю ферменту цитохромоксидази (це цитохром а3, що виступає в ролі кінцевої ланки перед О2). Відновлення окислених цитохромів відбувається в живій клітині за рахунок електронів, що переносяться дегідрогеназами. Послідовність передачі електрона від одного цитохрому до іншого така:
![]()
Каталаза та пероксидаза
До групи залізопорфіринів належать також каталаза та пероксидаза, дія яких направлена на перетворення пероксиду водню. Каталаза розкладає її на воду та молекулярний кисень
![]()
а пероксидаза розкладає пероксид водню з виділенням активного атомарного кисню:
![]()
Поряд із здатністю проводити окислення за рахунок пероксидного кисню очищені препарати рослинних пероксидаз здатні функціонувати як специфічні оксидази .Доведено також зростання активності пероксидаз в тканинах рослин, що знаходяться в несприятливих умовах існування. Це ще раз заставляє нас по-новому поглянути на біологічну роль даного ферменту.
Мідь-протеїди
У тканинах рослин знайдено також окислювальні ферменти, що мають в складі простетич- ної групи мідь, це так звані мідь-протеїди, наприклад, поліфенолоксидаза, аскорбатоксидаза:
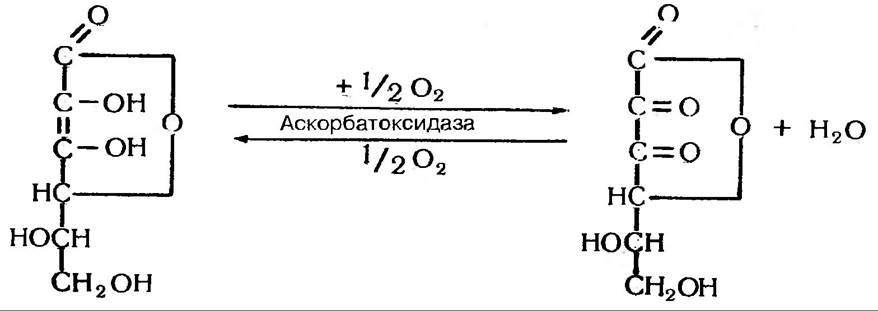
Це група ферментів, які при наявності молекулярного кисню окислюють різноманітні феноли з утворенням хінонів, тобто вони каталізують перенесення протонів і електронів від фенолів (гідрохінон, пірокатехін, пірогалол та ін.) на молекулярний кисень.
Поліфеноли — це, по суті ті ж дихальні хромогени, існування яких передбачав В.І. Палладій. (До речі, при механічному пошкодженні тканин — розрізані яблука, картопля, порушується координація між окислювальною та відновною фазами: в результаті нагромаджуються стійкоза- барвлені пігменти — м’якуш чорніє).
Вона належить до строго специфічних фенолоксидаз і окислює в основному аскорбінову кислоту та деякі сполуки, що мають подвійну фенольну групу. До мідьпротеїдних ферментів належить також пластоціанін.
Оксигенази
Крім оксидаз, які використовують О2 як акцептор електронів, в рослинній клітині локалізовані також оксигенази, які здатні активувати О2, внаслідок чого він може приєднуватися до органічних сполук. В активованому стані він безпосередньо приєднується до органічних сполук. Причому одночасно можуть приєднуватись, як два атоми (діоксигенази), так і один атом кисню (гідроксилази). Донорами електронів для них виступають НАДФ×Н, ФАД×Н2 та інші сполуки. Вони забезпечують процеси гідроксилування амінокислот, фенолів, стеринів та інших ендогенних сполук, а також детоксикацію ксенобіотиків (чужорідні для організмів сполуки, наприклад, пестициди). Гідроксилази функціонують за схемою:
![]()
де АН — органічна сполука, ДН2 — донор водню.
Діоксигенази можуть приєднувати кисень до різноманітних органічних сполук, як наприклад:
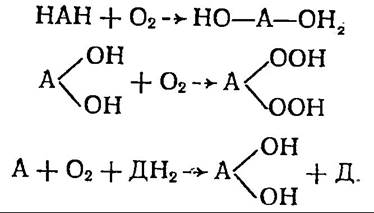
Отже, оксигеназами називають ферменти, що активують кисень з наступним включенням його в молекулу субстрату. На відміну від інших груп окислювальних ферментів оксигенази каталізують безпосередньо взаємодію атомів кисню не з воднем, а з атомами вуглецю ароматичних кілець. Флавінові ж та інші оксидази відновлюють молекули кисню з утворенням пероксидів. Існування оксидаз із змішаними функціями є ще одним вагомим доказом альтернативних шляхів активування кисню.
Слід також запам’ятати, що останнім часом все більшої ваги набуває ствердження того факту, що можливе пряме включення кисню в органічні молекули. Це один з дуже поширених можливих шляхів включення в загальний метаболізм таких речовин, як феноли, лізин, лактати та ін.
Ферменти — проміжні переносники водню (електрона). Це досить численна група ферментів, яка за хімічною природою належить до флавінових похідних. Специфіка даної групи ферментів полягає в здатності передавати електрони безпосередньо кисню. В цьому вони функціонально наближаються до оксидаз. Як простетична група в них виступає ФМН — флавінмононуклеотид, або ж ФАД — флавінаденіннуклеотид. Деякі з флавопротеїдів акцептують водень від того ж субстрату, який окислюється (приклад — специфічна сукциндегідрогена- за), тоді як інші тільки від відновленого НАД.
Основна функція флавопротеїдів — окислення відновлених піридинових (НАД та НАД×Ф- дегідрогеназ) і передача електронів у ЕТЛ в напрямку до кисню. Акцепторами, які можуть приймати від них електрони, служать інші дегідрогенази, або окислений цитохром, або нарешті сам О2. Отже, флавопротеїди здатні також переносити електрони на кисень, тому по суті їх також слід розглядати як оксидази. Адже в результаті їхньої дії утворюється пероксид водню, кисень якого використовується потім пероксидазою (приклад такого ферменту — глюкооксидаза). Саме тому флавінові ферменти та пероксидази являють собою спарену систему.
Досі ще немає єдиної думки відносно того, які з флавопротеїнів, що ідентифіковані в міто- хондріях вищих рослин, беруть участь в перенесенні електронів та локалізація їх в електротранспортному ланцюгу. В рослинних та тваринних об’єктах також виявлено фередоксини.
Частина з них безпосередньо взаємодіє з флавіновими дегідрогеназами, а частина з анаеробною НАД-дегідрогеназою.
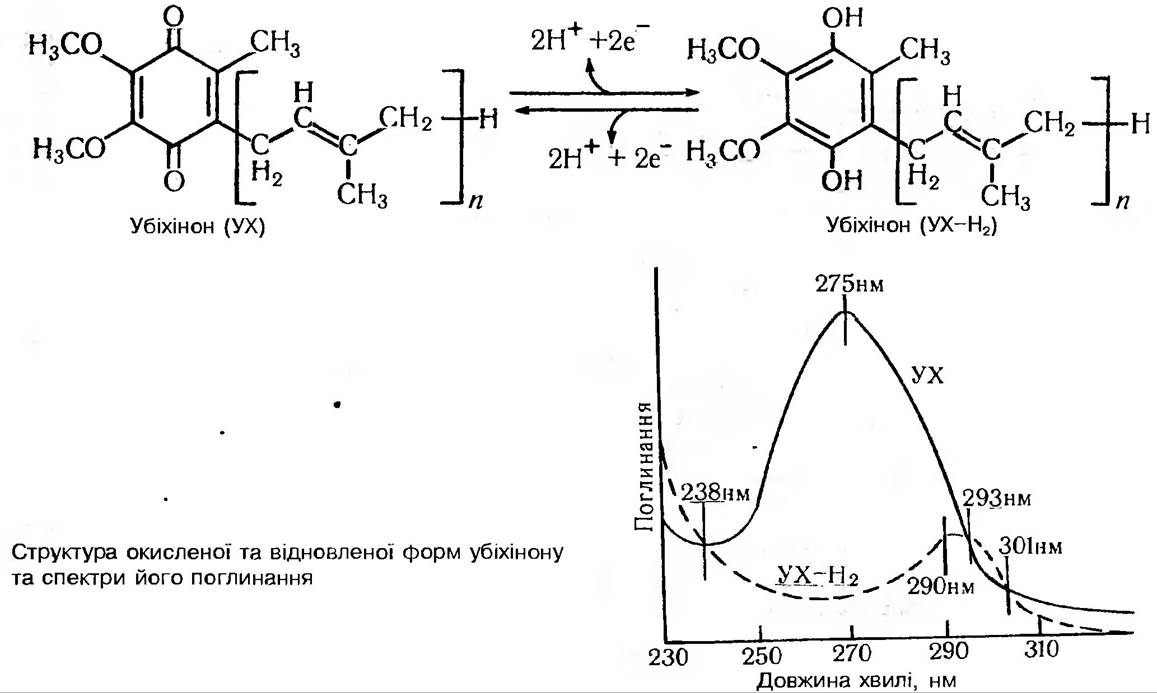
До проміжних переносників водню (електронів) належить також кофермент Q, або убіхінон.
Цей термін вживають для позначення групи сполук, що мають те саме хіноїдне Ядро, але відрізняються кількістю ізопротеїдних залишків у складі бічної ліпофільної ланки вуглецевого ланцюга. Убіхінон відновлюється до убіхінолу, приєднуючи одночасно по два електрони та два протони. Саме тому убіхінон є «двохелектронною окислювально-відновною сполукою» та «переносником» Н2. Убіхінон — невелика молекула порівняно з білковими компонентами термінальної ланки ЕТЛ. До того ж, будучи ліпідом, він легко розчиняється і тому має змогу переміщатися в ліпідному матриксі мітохондріальної мембрани. Вміст його в мембрані відносно високий порівняно з цитохромами (5:1). Цими властивостями, можливо, і пояснюється його роль як колектора електронів ЕТЛ. Сюди стікаються всі електрони від різних донорів, щоб потім, в разі потреби, постачати їх в ланцюг цитохромам. Крім названих ферментів в перенесенні електронів беруть участь і залізо-сірчані білки. В їх склад входить комплекс Fe-S; залізо якого зворотно окислюється і відновлюється.
Допоміжні ферменти
До ферментних систем, які беруть участь у диханні, слід віднести також ряд допоміжних ферментів, наприклад карбоксилази. Вони каталізують відщеплення СО2 від різних органічних кислот (кетокислот, амінокислот), в результаті чого утворюються сполуки з укороченим вуглецевим ланцюгом. Наприклад, таким чином при декарбоксилуванні пірувату утворюється оцтовий альдегід і т. д.
Слід також згадати ще одну групу ферментних систем, які не беруть безпосередньої участі в окисленні субстратів та перенесенні електронів, але беруть активну участь в підготовці субстратів дихання. Нагадаємо, що здатність ферментів дегідрогеназ здійснювати окислення поширюється лише на сполуки з невеликою, досить простої структури молекулою (органічні кислоти, спирти, цукри). Однак при диханні використовуються досить складні Органічні сполуки типу поліцукрів, білків, жирів. Саме тому використанню їх передує перетворення їхньої структури з допомогою ферментів гідролітичного комплексу. Потім в дію вступають ферменти, діяльність яких направлена на активування молекул мономерів, шляхом утворення їх фосфорних ефірів. Дальше активування досягається перетворенням хімічної структури молекули за допомогою ізомераз. Слід назвати також групу трансфераз, які каталізують відщеплення та перенесення окремих фрагментів вуглецевого ланцюга (трансальдолази та транскетолази).
Переносники електронів та водню ЕТЛ організовані в функціональні комплекси всередині внутрішньої мітохондріальної мембрани, а отже знаходяться в самому тісному контакті з компонентами ліпідного бішару. Не беручи участі в безпосередньому перенесенні електронів, ліпіди, створюючи ідеальне оточення для компонентів ЕТЛ, суттєво впливають на функціонування його. Цей висновок підтверджується таким спостереженням: якщо виділити фосфоліпіди з мітохондрій, активність електронного транспортування значно знижувалась, особливо на рівні цитохромоксидаз. При внесенні ззовні екстрагованих ліпідів активність поновлювалась до початкового рівня. Більше того, як виявилось, ліпідний склад внутрішньої мітохондріальної мембрани значно відрізняється від такої зовнішньої мембрани, наприклад, дифосфатдигліцерол локалізований виключно у внутрішній мембрані.
Шлях перенесення електронів і водню від однієї молекули переносника до іншої — це окислювально-відновний процес. Рушійною силою їх перенесення є різниця потенціалів. В зв’язку з цим, розташування окремих переносників ЕТЛ, як і при фотосинтезі, визначається величиною їх окислювально-відновного потенціалу. На початку ланцюга (рис. 87) розташований НАД> який володіє найбільш від'ємним потенціалом (-О,32 B), а в кінці — кисень з найбільш позитивним потенціалом (+0,82 В).
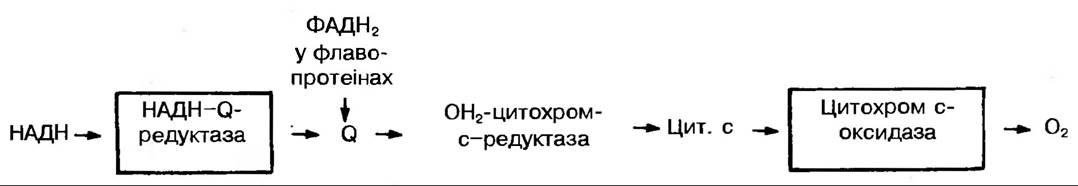
Рис. 87. Послідовність транспортування електронів у дихальному ланцюгу
Ферменти резистентного дихання
Мітохондрії рослин відрізняються від мітохондрій тварин тим, що в них можуть функціонувати два різних шляхи перенесенні електронів від субстрату типу НАД×Н та сукцинату до О2. Якщо один з цих шляхів пригнічується з допомогою (KCN-ціанідів), що блокують цитохромоксидазу, то інший шлях не блокується ціанідом, а тому його називають ціанідрезистентним ланцюгом перенесення електронів. Аналогічно сам окислювальний процес, що приводить до утворення такого термінального ланцюга, має назву ціанідрезистентного дихання, або дихання, стійкого до ціаніду.
Слід підкреслити, що ці два ланцюги не зовсім незалежні. Справа в тому, що в обох випадках введення в ланцюг електронних пар здійснюється внутрішньою та зовнішньою НАД×Н- дегідрогеназою та сукцинатдегідрогеназою і далі вони передаються на убіхінон. Тільки потім, після убіхінону, спостерігається розділення їх подальших шляхів. В нормальному ланцюгу електрони поступово переносяться через ФП, цитохроми b- і с-типу та цитохромооксидазу до О2, тоді як в ціанідрезистентному ланцюгу електрони переносяться від убіхінону на ФП, а потім через ціанцідрезистентну термінальну оксидазу теж на О2.
Природу термінальної оксидази поки що не вивчено. Вважають, що це залізосірчаний білок, що не є гемопротеїном. Фізіологічне значення ціанідрезистентного дихання не зрозуміле. Вважають, що воно відповідає за клімактерій у плодів, тобто посилення дихання в процесі перед дозріванням плодів. Є дані, що клімактерій індукується етиленом, тому вважають, що Етилен стимулятор ціанідрезистентного дихання. Доведено, що у деяких проростків цей тип дихання функціонує на його ранніх етапах, зокрема бубнявіння насіння.
Последнее обновление: 23/05/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.