Фізіологія рослин - Мусієнко М.М. 2001
Фотосинтез: фізіолого-біохімічні та екологічні аспекти
Фотосистема ІI
Це функціональне та структурне утворення фотосинтетичної одиниці, яке здатне поглинати світло, окислювати воду, відновлювати пластохінон та забезпечувати асиметричний трансмембранний розподіл електричних зарядів і генерувати хімічний потенціал іонів водню.
Незважаючи на те що в останні роки дослідження в напрямку з’ясування кількісного та якісного складу поліпептидів СЗК II, компонентів водоокислювального комплексу й учасників індукованого світлом транспортування електронів розвиваються досить швидкими темпами, все ж залишається досить не з’ясованих питань про склад комплексу фотосистеми II.
Вважають, що Ядро комплексу ФС II містить 5 гідрофобних поліпептидів. Крім того, воно містить до 50 молекул хлорофілу а, які зв’язані з білками масою 47 та 43 кД. Передбачають, що реакційний центр фотосистеми II (Р680 та феофітин), а також акцептори хінонової природи, локалізовані в комплексі з двох поліпептидів з відповідними масами 30 і 34 кД.
Доведено, що найменший поліпептид ядра ФС II масою 10 кД зв’язаний з цитохромом b559. Можливо, це тетрамер. Припускають, що він пронизує, незважаючи на малі розміри, весь бішар тилакоїдної мембрани. В цілому роль цитохрому b559 залишається не з’ясованою.
Виявлено в ФС II наявність ще трьох поліпептидів з масами 33 кД. Два з них входять до складу ядра ФС II, причому один виступає в ролі апопротеїну для вторинного хінонового акцептора Q, а другий бере певну участь в окисленні води. Третій виявився периферійним мембранним білком, який теж має відношення до окислення води. З процесом водоокислення пов’язані ще два периферійні мембранні білки комплексу ФС II з масами 23 та 17 кД.
Крім того, до складу ФС II входять поліпептиди з масами 29, 27, 26 та 25 кД, які становлять нативний світлозбираючий комплекс з хлорофілами а та каротиноїдами. В більшості хлоропластів вищих рослин поліпептид 26 кД найпоширеніший
Первинні процеси перенесення електронів у фотосистемі II пов’язані з одноелектронним перенесенням в РЦ II, чотириелектронною реакцією окислення двох молекул води та двоеле- ктронним відновленням пластохінону. В ролі первинного донора виступає хлорофіл а (Р680). Залишається дискусійним питання, де локалізується окислений стан Р+680, на одній чи на двох молекулах хлорофілу а. Первинний розподіл заряду в РЦ II — це надзвичайно швидке, індуковане світлом перенесення електронів між Р680 та феофітином. Акцептором виступає молекула пластохінону QА, який зв’язаний з поліпептидом масою 47 кД. При відновленні акцептора QА утворюється аніон семихінону.
В комплексі ФС II є два різних пластохінони, які виступають в ролі послідовно діючих акцепторів електронів: QА, ймовірно, зв’язаний з поліпептидом 47 кД та Qв, який поєднаний з поліпептидом центрального ядра ФС II масою 33 кД.
Вторинний акцептор поєднує одноелектронні процеси перенесення зарядів в РЦ з відновленням вільного пластохінону таким чином, що електрони переносяться попарно. Пігмент Р680 розміщений ближче до внутрішньої сторони мембрани, а акцептор QA, навпаки, ближче до зовнішньої. За рахунок такого асиметричного розміщення при фотохімічному розподілі зарядів в РЦ на мембрані може виникати трансмембранна різниця електрохімічних потенціалів.
Особливо важливі реакції відбуваються на донорній стороні ФС II. Насамперед розглянемо відновлення Р680 В ролі проміжного донора електронів для нього виступає компонент Z. Він являє собою одноелектронний переносник, який поєднує РЦ II з водоокислювальним комплексом. Невідомо поки що, чи він поодинці зв’язує РЦ, чи їх існує кілька, як вони тоді взаємодіють — послідовно чи паралельно? Передбачають, що за хімічною природою — Z -катіон пластосемихінону (PQH+).
Більш важка субодиниця СР 47 фотосистеми II володіє фотохімічною активністю не лише в складі всього комплексу, а навіть в ізольованому вигляді. В цілому вона містить Р680 реакційного центра, компонент Z, а також феофітин — первинний акцептор ФС II та молекулу зв’язаного пластохінону QA — вторинний акцептор ФС II. Встановлено амінокислотну послідовність даної субодиниці. Цей білок містить сім α-спіральних ділянок, які наскрізь пронизують тилакоїдну мембрану. Із них чотири ділянки містять пари гістидинів, які відповідальні за зв’язування молекул хлорофілів. Значна частина цього поліпептиду, що налічує 200 амінокислот, формує по-
лярну область, яка відповідає за взаємодію з функціональними комплексами — первинними та вторинними донорами електронів для Р680 (рис. 54, 55).
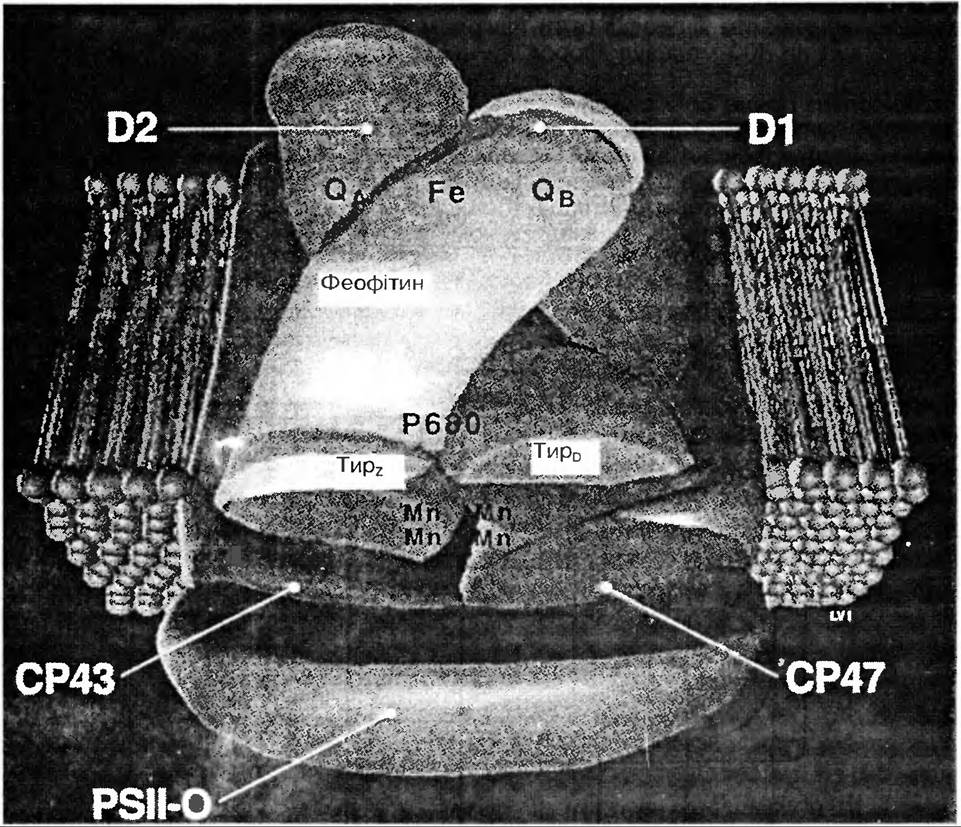
Рис. 54. Модель центрального комплексу ФС II (D1, D2 — поліпептиди які зв’язують хлорофільні комплекси СР47 та СР43
Більш легка субодиниця ФС II СР43 в ізольованому вигляді не проявляє фотохімічної активності. В основному вона виконує функції внутрішньої антени СЗК II. Саме тому, вона знахо
диться в тісному контакті з попередньою субодиницею СР47, щоб забезпечити високу ефективність Міграції енергії до РЦ ФС II.
Водоокислювальний комплекс фотосистем и II.
Мінімальний кисневидільний комплекс ФС II вперше виділено в 1985 р. (I. Kenchi et al., 1985). Він містив, крім поліпептидів 47, 43, 32, 30 кД і цитохрому b6, ще зовнішній мембранний білок 33 кД, 3-4 атоми марганцю та 2 молекули пластохінону.
Вважають, що саме центральний комплекс ФС II, що містить поліпептид 33 кД та іони марганцю, і є місцем локалізації розкладання води. Два зовнішніх мембранних білки 23 і 16 кД утворюють відповідне оточення, щоб забезпечити міцне зв’язування іонів кальцію та хлору. Доведено, що при наявності білка 23 кД в кілька разів зменшується кількість іонів хлору, яка потрібна для виділення кисню. Якщо достовірне припущення, що хлор та кальцій зв’язуються з протеїном 33 кД то, очевидно, білки 23 і 16 кД забезпечують потрібну конформацію білка 33 кД, щоб утримати ці іони.
Процеси виділення кисню найтісніше пов’язані з наявністю марганцю в водо окислювальному комплексі. Як допускають, існує не менше двох пулів марганцю: один з них слабо зв’язаний з мембраною, який саме забезпечує формування молекули О2, та пул, міцно зв’язаний з мембраною. Функції останнього ще повністю не виявлені, хоча є дані про його зв’язок із світлозбираючим хлорофіл (а/b)-білковим комплексом.
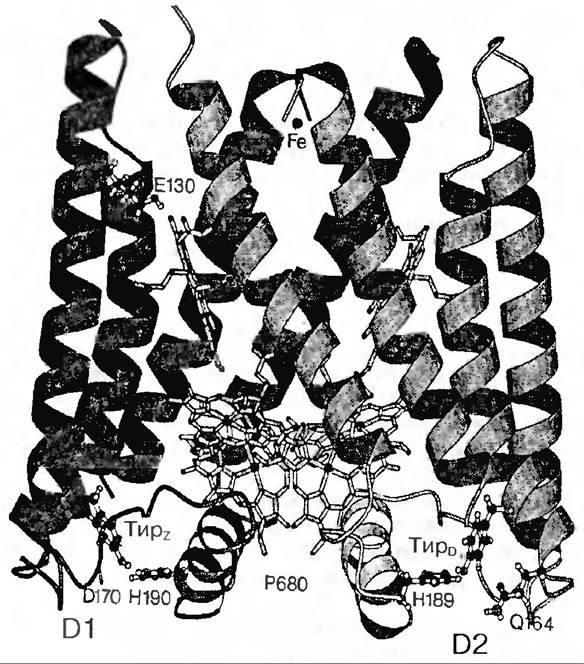
Рис. 55. Структурна модель реакційного центру ФС II
Знайдено, що на 400 молекул хлорофілу, іншими словами, на одиницю фотосистеми II припадає 4 атоми марганцю. Екстрагуванням марганцю із тилакоїдів за допомогою трис-буферу була встановлена пряма кількісна залежність між кількістю виділеного кисню та втратою іонів марганцю. Тому була запропонована модель, згідно з якою кожен центр по виділенню кисню функціонально з’єднується з 4 атомами марганцю. У виділених фрагментах тилакоїдів, які несуть компоненти ФС II, саме в їх донорній частині дійсно розташований Mn-вмісний центр, де знаходиться якраз чотири атоми марганцю. Послідовно віддаючи 4 електрони, вони здатні досягати високого ступеня окислення, завдяки чому відбувається і окислення води, завершуване виділенням молекулярного кисню:
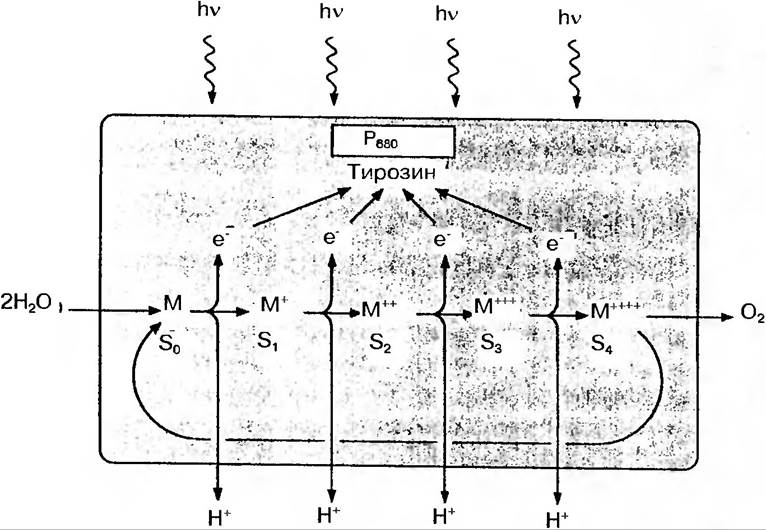
Таким чином, молекула пігменту Р+680 реакційного центру ФС II як сильний окислювач забирає електрон, тобто окислює донор Z та запускає цикл перетворення системи S, яка і розщеплює воду (рис. 56).
Система S, ймовірно, і є тим Mn-вмісним білковим комплексом, який здатний нагромаджувати чотири позитивні заряди.
В ролі проміжних компонентів, які переносять електрони від водоокислювального комплексу до Р680, виступають Z та цитохром b559, який наскрізь пронизує мембрану. Його центр, можливо знаходиться ближче до внутрішньої сторони мембрани, за рахунок чого забезпечується активне транспортування електронів до акцепторних груп Z та Р680. Виявлено дві форми цитохрому b559 — низькопотенціальну та високопотенціальну, які відрізняються функціонально. Така гетерогенність може бути зумовлена різницею в мікрооточенні двох однакових молекул цитохрому b559.
В цілому мінімальна модельна схема фотосистеми II може бути представлена у вигляді:
![]()
де М — специфічний для системи виділення кисню проміжний компонент, який здатний нагромаджувати до чотирьох зарядів, тобто Мn+; Мn+2, Мn+3, Мn+4 Р680 — специфічна молекула хлорофілу а РЦ II, яка окислюється під дією світла; Q — перший стабільний акцептор електронів, який є молекулою хінону; Z — донор електронів для Р680; В — вторинний акцептор електронів, який також є молекулою хінонового типу і позначається QB; він зв’язує ФС II з пулом пластохінону PQ та ФС І.
Отже, макромолекулярний комплекс ФС II містить не менше семи різних поліпептидних субодиниць, узгоджена дія яких забезпечує міграцію квантів поглинутого світла у вигляді нейтрального збудження до реакційного центру Р680, розділення зарядів та стабілізацію їх, відновлення пластохінону, розкладання молекул води з виділенням кисню та виділенням протонів всередину тилакоїда.
Відновлення НАДФ. Фередоксин є однією з найголовніших ланок в електрон-транспортній системі фотосинтезу. Під час послідовних реакцій, які ведуть до відновлення НАДФ+, електрони спочатку поступають на проміжний фермент фередоксин-НАДФ-редуктазу. Лише цей хлоро пластний флавопротеїновий фермент відновлює НАДФ+. Наявність двох каталітичних центрів дозволяє цьому ферментові реагувати як з фередоксином, так і з НАДФ+.
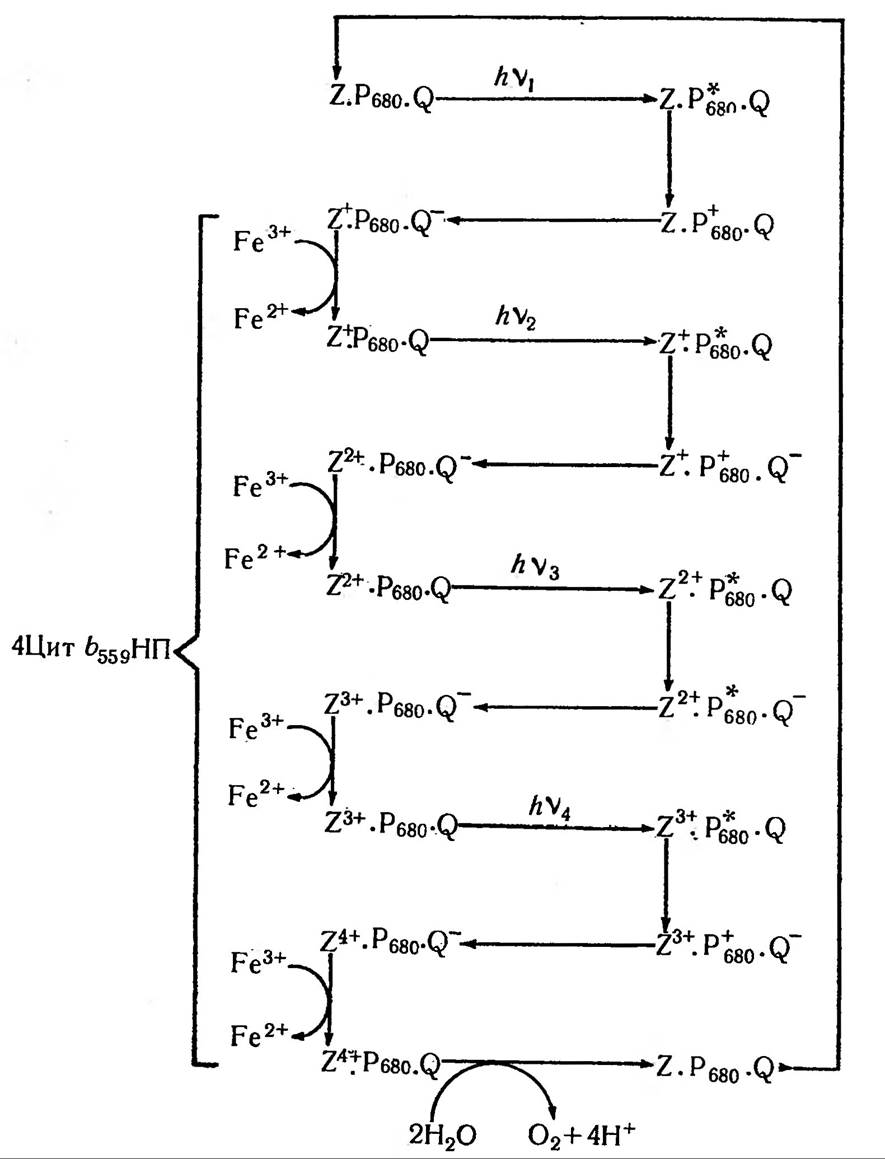
Рис. 56. Система виділення кисню яка функціонує в ФС II. На переноснику Z, який віддає електрони на Р680 повинні нагромадитись чотири позитивні заряди, перш ніж відбудеться виділення молекули кисню
Последнее обновление: 23/05/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.