Фізіологія рослин - Мусієнко М.М. 2001
Загальні принципи регуляції росту та морфогенезу рослин
Мембранна регуляція
В основі мембранної регуляції лежить той незрівноважений стан, який забезпечується різноманітними хемо-, фото- та механорецепторами мембран. Вони досить чутливі до кількісних та якісних змін зовнішнього і внутрішнього середовища і забезпечують відповідну реакцію мембрани.
. В основі мембранної регуляції знаходиться той стан динамічної нерівноваги, який підтримується в кожній клітині на певному стаціонарному рівні завдяки роботі іонних насосів, локалізованих в мембранах. Особливу роль відіграють протонні помпи, які функціонують на базі мембранних Н+ — АТФ-аз або редоксланцюгів, створюючи електрохімічний потенціал іонів Н+(ΔμН+). Він включає в себе два компоненти: електричний, або мембранний потенціал (Δу) і хімічний, або концентраційний потенціал (ΔрН), тобто ΔμН+ =Δψ+ΔрН. Значення мембранного потенціалу на плазмалемі, досягає 100-200 мВ, причому внутрішня сторона мембрани має від’ємний заряд. Енергія даного потенціалу використовується для поглинання клітиною катіонів, аніонів, цукрів і інших сполук. Підтримка на стаціонарному рівні значення мембранного потенціалу є найважливішою складовою частиною гомеостазу. При зниженні мембранного потенціалу на плазмалемі його величина відновлюється внаслідок відкриття калієвих каналів і виходу іонів К+ або активацією протонного насосу (Польовий, Саламатова, 1991).
Мембранна регуляція має вирішальний вплив на зміну концентрацій внутрішньоклітинного кальцію. Останній входить в клітину за електрохімічним градієнтом через кальцієві канали, а викачується за участю Са2+-АТФ-ази або шляхом антипорту з іонами водню. Кальцій може акумулюватися у вакуолях, в ендоплазматичному ретикулумі та звільнятися з них. Його концентрація в цитоплазмі підтримується на досить низькому рівні (10-7М). Незначне підвищення його концентрації до (10-6М) впливає на активність Са2+-залежних протеїнкіназ, фосфорилування білків, стан цитоскелету, секреторну, мітотичну активність та інше. Кальцій регулює всі ці процеси через зв’язок із кальмодуліном та іншими кальцій-зв’язуючими білками.
Крім того, в рослинних клітинах, так же як і у тварин, в ролі регуляторної системи функціонує фосфоінозитольний цикл. Фосфатидилінозитол-4,5-дифосфат плазмалеми розщеплюється з допомогою мембранної фосфоліпази С на інозитол-1,4,5-трифосфат та діацилгліцерол. Перший із них сприяє звільненню Са2+ із ендоплазматичного ретикулуму, а другий активує за участю Са2+ протеїнкіназу С в плазмалемі. Активована протеїнкіназа С фосфорилює білки іонних каналів, регулюючи їх роботу (дивись стор. 212).
Зовсім недавно (Kaufman, 1994) виявлено, що в мембранній регуляції у вищих рослин значну роль відіграють ГТФ-зв’язуючі сигнальні білки. Це так звані великі, або гетеротримерні ГТФ-зв'язуючі регуляторні протеїни та малі G-протеїни. Великі G-протеїни складаються із трьох (а, β і γ) субодиниць, але взаємодіють лише з одним рецептором та однією ефекторною системою (elicitor system).
Перша α-субодиниця, з молекулярною масою між 35 і 55 кДа, містить ГДФ-зв'язуючу ділянку, яка має здатність гідролізувати ГТФ. Наступні β-субодиниця (≈40 кДа) і у-субодиниця (≈10 кДа) є стійким димером. В неактивному стані α-субодиниця зв'язана з ГДФ, який після взаємодії із збудженим рецептором звільняється і залишається на ГТФ. Далі α-субодиниця відокремлюється від (β/γ-субодиниць), і в такому дисоційованому стані вони здатні активувати специфічну мішень ефекторної системи відповіді на збудження (рис. 169).
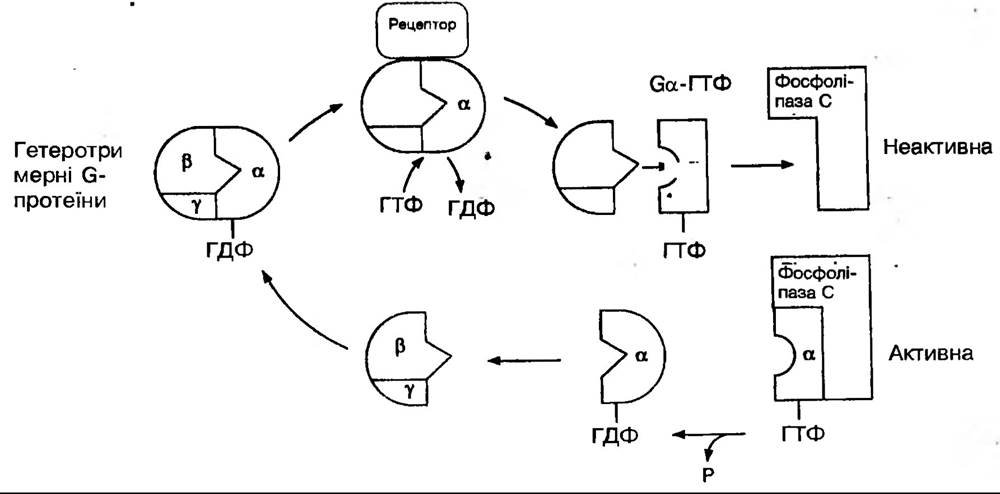
Рис. 169. Схема функціонування G-протеїнів
Цікаво, що α-субодиниця залишається активною до закінчення гідролізу ГТФ, тоді як димер (β/γ-субодиниць) проявляє активність доти, доки не з’єднається з інактивованою α-субодиницею. Вважають, що вони передають сигнали від семисегментних трансмембранних рецепторів до специфічних клітинно-ефекторних систем, таких як циклічний аденозинмонофосфат (цАМФ) — або інозитолтрифосфат генеруючих систем. Відомо, що аденілциклазна система, яка включає 3’,5’-АМФ та цАМФ-залежні протеїнкінази і регуляторними субодиницями яких є цАМФ-зв’язуючі білки, є універсальним механізмом передачі зовнішніх сигналів та їх реалізації на молекулярному рівні у евкаріот.
Малі G-протеїни є мономерами з молекулярною масою між 20 і 30 кДа. Вони також здатні зв’язувати ГТФ під час активації та переходити в неактивну форму у процесі гідролізу ГТФ.
Виявлено три підкласи малих G-протеїнів із різноманітними регуляторними функціями — від транспортування білків, везикул, до регуляції клітинного циклу, росту клітин, їх диференціації, організації мікрофіламенгних структур цитоскелету.
Практично всі функції мембран — бар’єрна, транспортна, енергетична, осмотична, структурна, біосинтетична, електрична, рецепторна — відіграють певну роль в регуляторних процесах. Причому особливо важливе значення має система мембранних хемо-, фото- та механоре- цепторів, які дозволяють клітині відповідно оцінювати якісні і кількісні зміни внутрішнього, зовнішнього середовища та відповідно на них реагувати.
Последнее обновление: 23/05/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.