Фізіологія рослин - Мусієнко М.М. 2001
Фізіологія росту та розвитку рослин
Біогенез клітинних структур та онтогенез рослинної клітини
Процес біогенезу клітинних структур багатоступеневий: ДНК → РНК → білки → самозбирання надмолекулярних функціонально активних блоків → функціональна активність метаболічних циклів → клітинні органоїди.
Воду, всі поживні речовини, Органічні сполуки, мінеральні катіони та аніони рослини використовують для нових синтезів різноманітних речовин, з яких складається сама Клітина: НУКЛЕЇНОВІ КИСЛОТИ, білки, Ліпіди, вторинні метаболіти, фітогормони та ін. Основним принципом біогенезу вторинних структур є самозбирання надмолекулярних комплексів. В цих процесах найважливішу роль відіграють нуклеїнові кислоти та білки (рис. 147). Кожна рослинна клітина має ДНК та РНК. У еукаріот ДНК локалізована в ядрі і є основним компонентом хромосом. В органелах (мітохондріях та хлоропластах) є ДНК кільцевого типу. Всі клітини мають також три типи РНК, які синтезуються на матриці ДНК і це називають транскрипцією. РНК є матрична (мРНК), рибосомальна (рРНК) та транспортна (тРНК). Білки синтезуються за участю всіх форм РНК, які є в складі полісом. Цей процес називають трансляцією. Коефіцієнти седиментації РНК, цитоплазми, мітохондрій та хлоропластів 80S, 78S та 70S (Сведберг) відповідно. Запис інформації в ДНК зберігається у вигляді відповідних сполучень чотирьох нуклеотидів. Інформація записується вздовж ланцюга спіралі ДНК (триплетний код) у формі специфічної для кожного організму послідовності азотистих основ. Інформація від ДНК кодує амінокислотну послідовність білків, які синтезуються. В свою чергу, послідовність амінокислот в білках визначає специфічність структури та функції білків. Інформація в білках записана кодом із 20 амінокислот. Переведення інформації з коду ДНК на код білків здійснюється за допомогою РНК.
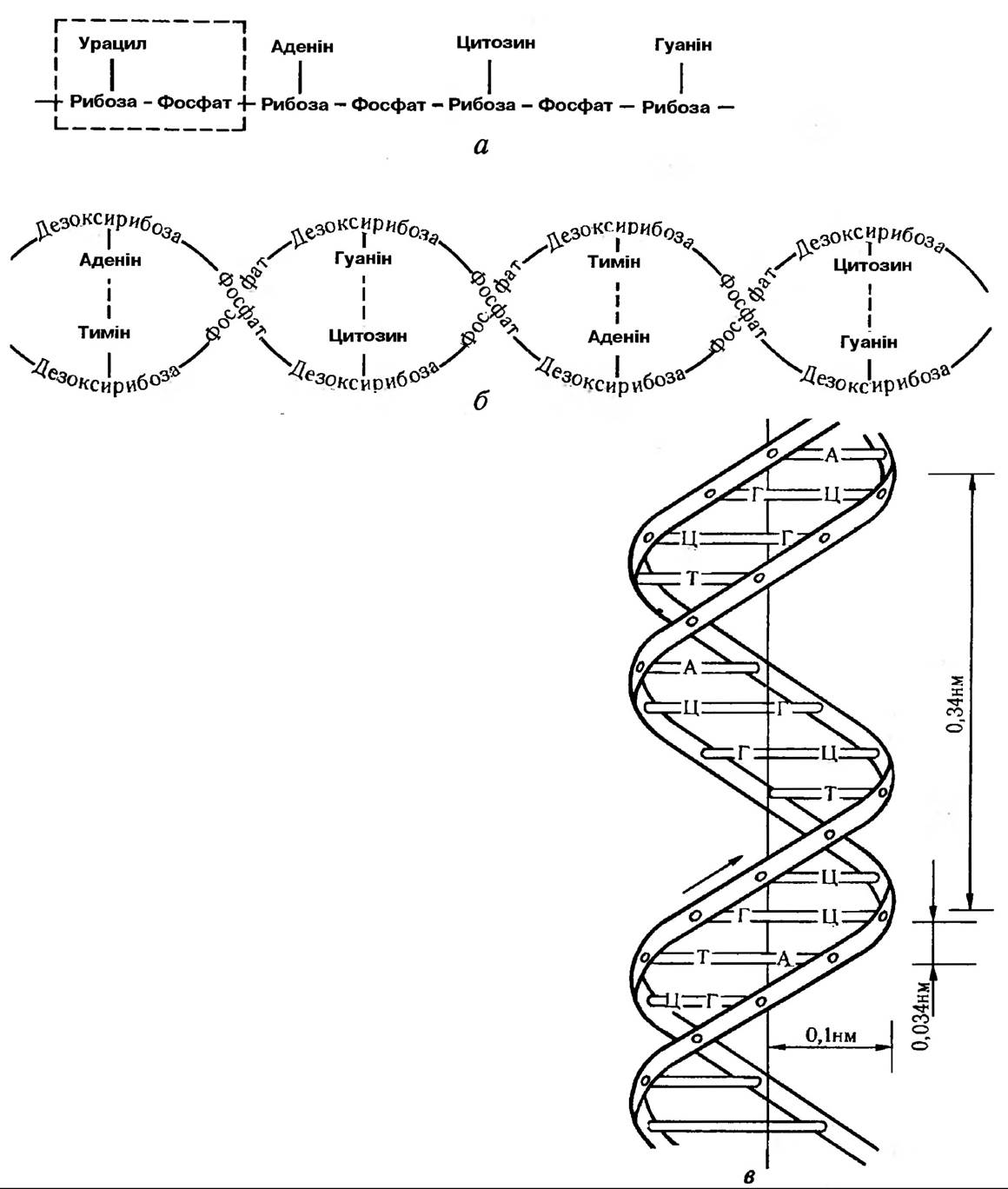
Рис. 147. Схема будови нуклеїнових кислот: а — молекула РНК (виділений один нуклеотид); б — молекула ДНК; в — модель молекули ДНК за Уотсоном і Кріком. Буквами позначені азотисті основи (аденін, тимін, гуанін, цитозин)
Подвійна спіраль ДНК та гістони становлять нуклеосоми. Нуклеосомою називають комплекс, що складається з 8 молекул гістонових білків, на які "намотані» петлі ДНК, кожна з яких має 140-200 пар нуклеотидів. Діаметр нуклеосом 10 нм. Між нуклеосомами локалізовані ділянки ДНК із 30-50 пар нуклеотидів довжиною до 10-20 нм, які зв’язані з гістонами. Така організація ДНК в Хроматин дозволяє її молекулі складатися в петлі та більш складні структури. ДНК в нуклеосомах менш доступна до впливу нуклеаз, тому нуклеази легше розщеплюють міжнуклеосомні ділянки молекули. Гени (цистрони), які кодують функціонально зв’язані білки, розміщуються по різних ділянках хромосом, а не об’єднані в оперони, як це спостерігається у прокаріот.
Більшість молекул РНК синтезується у вигляді її попередників (про-РНК). Після утворення первинного транскрипту відбувається його процесинг (дозрівання),
що складається із сукупності реакцій, які ведуть до перетворення первинних продуктів транскрипції в функціонуючі молекули, Напівперіод життя більшості молекул матричної РНК еукаріот становить від 3 до 48 год (рис. 148).
В ДНК еукаріот крім унікальних послідовностей нуклеотидів є велика кількість повторів, тобто послідовностей, які повторюються. Кількість їх може досягати 10е разів на Геном. У вищих рослин доля унікальних ділянок геному становить лише 20-30%. Велика кількість повторів необхідна для синтезу рРНК та гістонів. Однак все ж більшість повторів використовується для регуляції експресії генів.
Більшу частину геному займають інтрони — послідовності в середині структурного гена, які не беруть участі в кодуванні білкового продукту гена. Після транскрипції гена послідовності, які відповідають інтронам, виділяються з мРНК в процесі сплайсингу.
Сплайсинг — це ферментативне видалення інтронів та зрощування двох кінців екзонів при синтезі мРНК. Екзони — ті ділянки структурного гена, які кодують амінокислотну послідовність
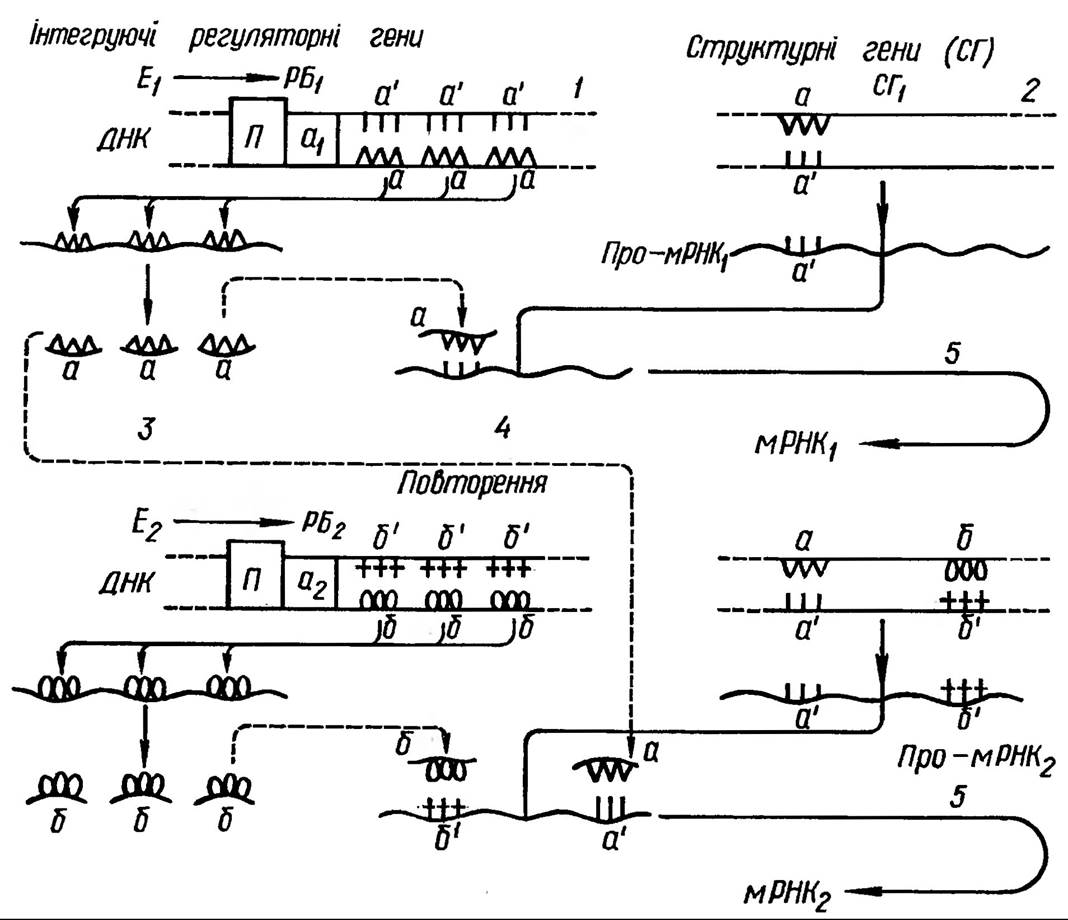
Рис. 148. Гіпотетична схема регуляції експресії генів мРНК у еукарют: Ел, Е2 — ефектори; ЗБ1т РБ2 — рецепторні білки ефекторів; а,, а2 — акцепторні зони, П — промотор
білкового продукту. В склад генів входять спейсери (прокладки), які або не вичитуються взагалі, або транскрибуються, після чого руйнуються.
Структура та Синтез ДНК. ДНК — це полімер, що складається з 4 нуклеотидів: пуринових (аденін-гуанін) та піримідинових (цитозин-тимін), а також дезоксирибози та залишку фосфорної кислоти. Це подвійна спіраль, в кожній із яких НУКЛЕОТИДИ ковалентно зв’язані через залишки фосфорної кислоти. Між собою ланцюги взаємодіють за допомогою водневих зв’язків, які виникають в середині спіралі між пуриновими та піримідиновими основами, причому аденін завжди взаємодіє з тиміном А-Т, Т-А, а гуанін з цитозином Г-Ц, Ц-Г (див. рис. 147). Це явище (комплементарність) лежить в основі відтворення самої ДНК, а також ДНК-залежних синтезів всіх РНК та синтезу білка в клітині. Молекули ДНК евкаріот налічують 109—10» пар таких основ.
Цей процес відбувається в певний період мітотичного циклу при наявності тріозофосфатів всіх чотирьох дезоксинуклеотидів, іонів магнію, ДНК-затравки та ДНК-полімерази і має назву реплікації, тобто копіювання. Він здійснюється напівконсервативним способом, який полягає в тому, що молекула ДНК подвоюється шляхом реплікації кожного з двох його ланцюгів. Саме тому кожна подвійна спіраль ДНК має в своєму складі «старий» та "новий» полінуклеотидний ланцюги. V.процесі реплікації двоспіральна Структура ДНК локально розплітається в кількох місцях одночасно. Звідси реплікація йде в обох напрямках до зустрічі між подібними ділянками. Новий ланцюг синтезується ДНК-полімеразою, причому на всіх ділянках зберігається полярність збирання полімеру.
В процесі реплікації ДНК взаємодіє комплекс факторів, який включає ДНК-полімеразу, фактори початку реплікації та компонент, який відповідає за локальне розплетення подвійного ланцюга ДНК.
Структура, форми РНК та синтез їх. Всі РНК також побудовані з нуклеотидів чотирьох основ: аденіну, цитозину, гуаніну та урацилу. Піримідин урацил в РНК замінює тимін ДНК. Як цукор використовується рибоза, а не дезоксирибоза. Розміри РНК досить різноманітні. Матрична РНК займає до 3% загальної суми РНК в клітині і включає в себе до 10-40 тисяч нуклеотидних послідовностей. До складу рибосом входять також рибосомальні РНК (рРНК) з коефіцієнтами седиментації I8S, 28S (синтезуються в ядерції 5,8S та 5S деяких (синтезується в деяких
хромосомах). Транспортна РНК містить 75-80 нуклеотидів і таких тРНК в клітині близько 20 різних форм (для кожної амінокислоти своя транспортна РНК).
Молекули РНК не мають подвійної спіралі, але в різних ділянках можуть сполучатися між собою, що призводить до утворення петель і формування вторинної структури молекули. Наприклад, молекули тРНК можуть мати вторинну структуру у вигляді трилисника (листок конюшини). Характерно, що до складу тРНК входять різноманітні метильовані та інші незвичайні нуклеотиди.
Синтез РНК здійснюється на матриці ДНК за участю РНК-полімераз (рис. 149).
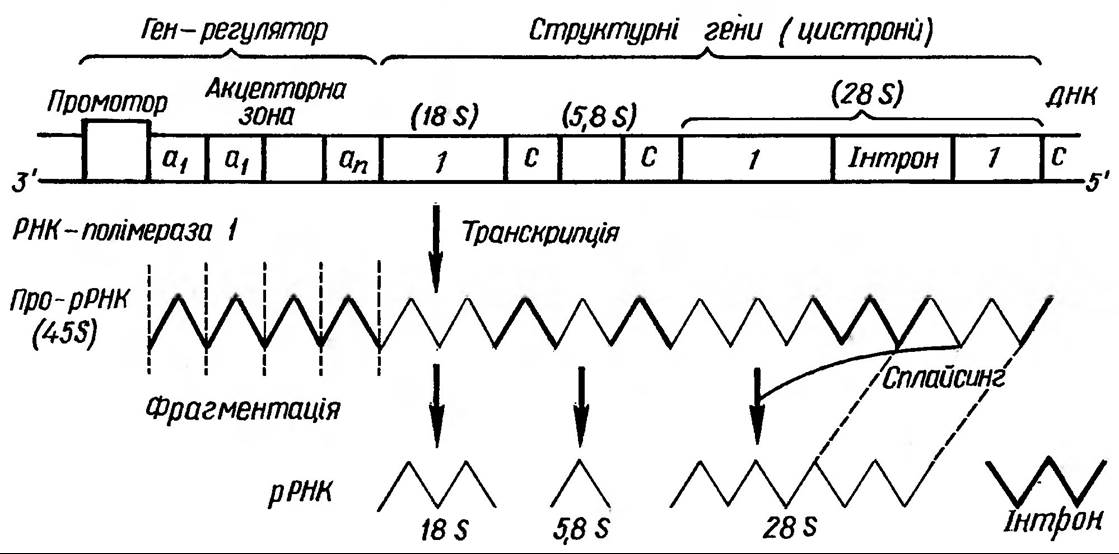
Рис. 149. Структурні гени рРНК, еукаріот, їхня Транскрипція та процесинг: С — спейсер, 1 — екзон
Причому, в ядрах еукаріот функціонують три РНК-полімерази:
·РНК-полімераза, яка забезпечує синтез рибосомальної РНК і локалізована в ядерці;
·РНК-полімераза, яка здійснює синтез матричної РНК;
·РНК-полімераза, яка здійснює транскрипцію тРНК і 5S рРНК.
Останні дві полімерази локалізовані в хроматині та нуклеоплазмі.
Синтез РНК здійснюється на матриці ДНК. Регуляція процесів транскрипції здійснюється на різних рівнях: шляхом роздріблення хроматину за рахунок модифікації структури гістонів (метилювання їх, фосфорилування та ін.), зміною активності та локалізації РНК-полімераз, через контроль всіх етапів процесингу, а також зв’язуванням матричних РНК в рибонуклеопро- теїнові комплекси (інформосоми) та звільненням їх. Істотну роль в регуляції процесів транскрипції відіграють специфічні негістонові білки, які виступають у ролі активаторів і репресорів, рецепторів фізіологічно активних речовин, фітогормонів, ферментів.
Структура та синтез білка
Білки складають основу цитоплазми. До складу їх входять 20 амінокислот, хоч небілкових амінокислот відомо значно більше. Амінокислоти з’єднуються в білку за допомогою пептидного зв’язку —NH—CO—. Поліпептиди в рослинному організмі можуть зустрічатися у вільному стані, наприклад глутатіон. Крім пептидних зв’язків, є ще один тип ковалентних зв’язків — дисульфідні (-S-S-), які об’єднують окремі ділянки молекули, або поліпептидні ланцюги. В молекулі білка зустрічаються і різноманітні більш слабкі зв’язки, наприклад, водневі, іонні.
Розрізняють первинну і вторинну структури білків. Спеціальна послідовність амінокислот, які зв’язані ковалентними пептидними зв’язками, становить первинну структуру білка. Водневі зв’язки між певними ділянками зумовлюють згортання молекули, а отже α-спіральну структуру її. Це так званні α-структури, які можуть зустрічатися на певних ділянках молекули. Зустрічається також β-структура, яка також зумовлена водневими зв’язками, але не в середині одного ланцюга, а між сусідніми двома ланцюгами, α- і β-структури визначають вторинну структуру білка. Різноманітні просторові розміщення спіральної молекули білка створюють специфічну конфігурацію її і це є третинною структурою білка.
Білки досить часто складаються з різних субодиниць, які поєднуються нековалентними зв’язками. Ці комплекси утворюють четвертинну структуру білків. За формою розрізняють фібрилярні та глобулярні білки. До складу їх входять амінокислоти, які містять як карбоксильні, так і амінні групи, тому білки є амфотерними сполуками. В лужному розчині вони дисоціюють як кислоти і будуть заряджені від’ємно, а в кислому середовищі білки дисоціюють як луги, тому заряджені позитивно. Реакцію середовища, при якій встановлюється рівновага позитивних та негативних зарядів білка, називають ізоелектричною точкою. В такому стані білок найменше
розчинний і легко випадає в осад. Гідроксильні групи та амінні групи — гідрофільні, тому вони зв’язують молекули води. В певних умовах білки набувають структури гелю — це пов’язано з утворенням з білкових молекул сітчастих структур, всередині яких знаходяться відповідно орієнтовані молекули води. При руйнуванні такої сітчастоподібної структури весь комплекс переходить в більш оводнений стан золю. Переходи гель — золь відіграють важливу роль в життєдіяльності цитоплазми.
інформація про структуру білка знаходиться в матричній РНК у формі кодонів, кожен з яких складається з трьох основ — триплетів, які еквівалентні конкретній амінокислоті. У зв’язку з тим. що до складу нуклеотидів РНК входить чотири азотисті основи, для амінокислот можливі 64 кодони, тому кожній амінокислоті належить більше ніж один кодон. Синтез білка здійснюється на матриці мРНК в цитоплазмі в процесі трансляції (рис 150).
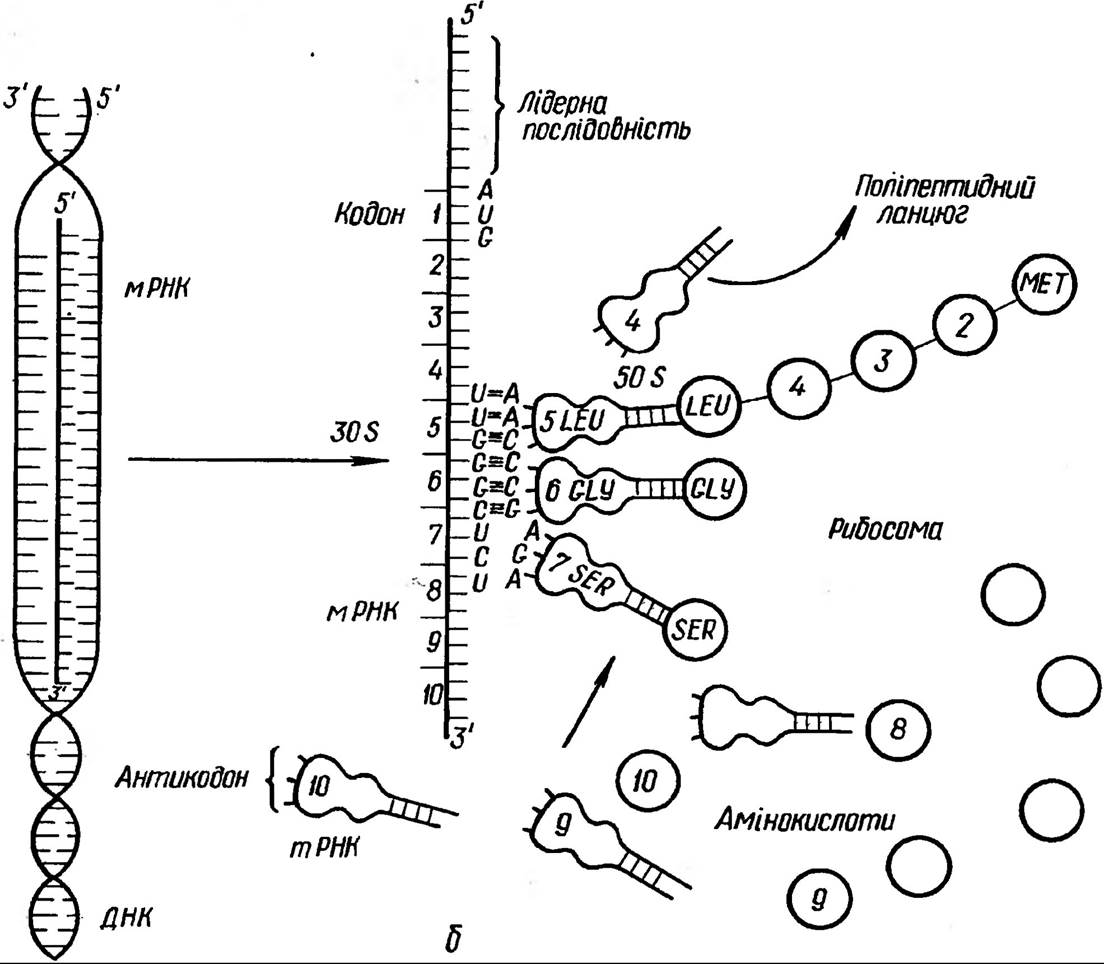
Рис. 150. Схематичне зображення процесів транскрипції (а) і трансляції (б)
Механізми трансляції значно складніші за процеси транскрипції. Якщо транскрипцію забезпечує близько двох десятків білків, то для трансляції потрібно до 50 спеціалізованих білків. Процес синтезу поліпептиду крім ініціації включає фази елонгації та термінацїї.
Для включення в поліпептид амінокислоти попередньо активуються, перетворюючись за участю АТФ та аміноацил — тРНК-синтетази в аміноациладенілати, які потім під дією тих же ферментів приєднуються до відповідних тРНК (рис. 151). Для кожної амінокислоти існує одна специфічна тРНК та одна аміноацил-тРНК-синтетаза. Синтез поліпептидного ланцюга в рибосомному комплексі здійснюється доти, доки не буде досягнуто термінального кодону мРНК. З даним кодоном зв’язується білковий фактор термінацїї, який не лише розпізнає потрібний кодон, а й забезпечує відрив поліпептиду від тРНК. Після відривання поліпептиду відбувається роз’єднання деацильованих тРНК і мРНК. Процес завершується дисоціацією Рибосоми на субодиниці.
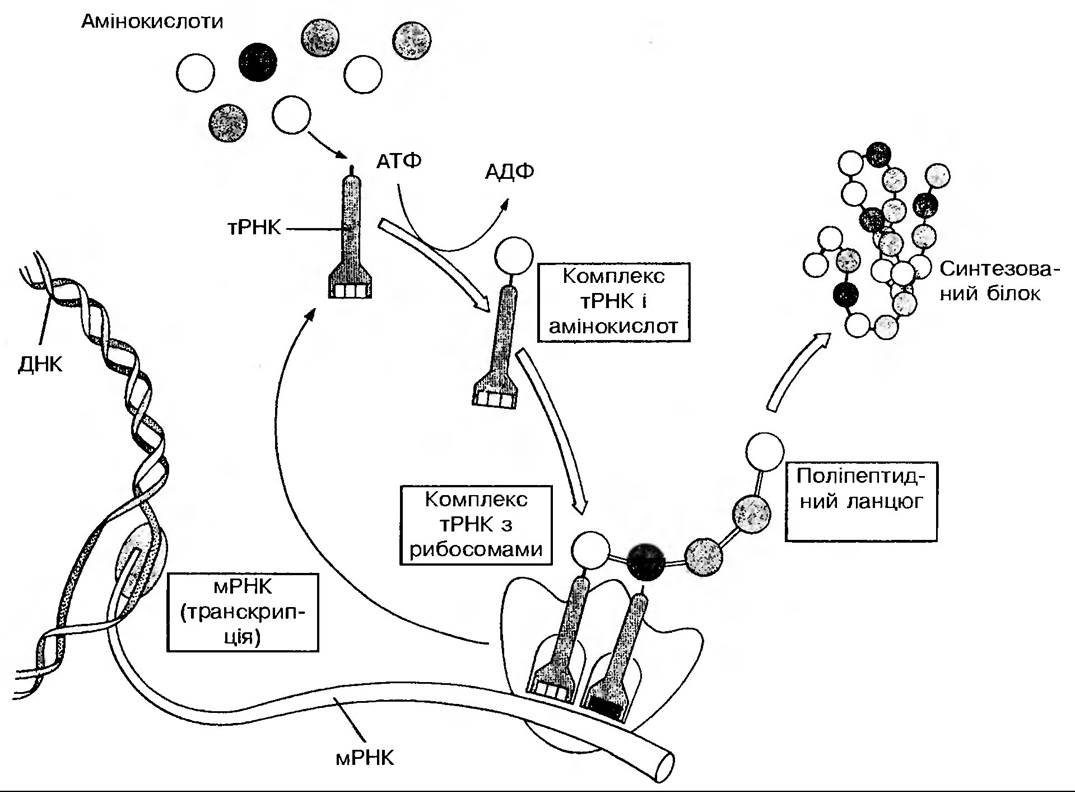
Рис. 151. Схема синтезу білку
Характерно, що кожна молекула матричної мРНК може бути зчитаною багатократно. Слід зазначити, що для синтезу білка важливу роль відіграє певне фізико-хімічне середовище (на-
явність іонів магнію, калію, марганцю, pH і т. д.). У клітині в певний відрізок часу синтез білка забезпечує виконання певної фізіологічної програми, тому активація і зчитування великої кількості матричної мРНК, які кодують новоутворені білки, повинні бути строго координовані. При зміні фізіологічного стану клітини змінюється практично стан усіх компонентів апарата трансляції. Зниження інтенсивності синтезу білків, у свою чергу, гальмує транспортування мРНК із ядра в цитоплазму. Отже, в рослинній клітині функціонують системи регуляції, які координують транскрипцію різних класів РНК і трансляцію різних білків, а також забезпечують тісну взаємодію всіх цих процесів.
Самозбирання та біогенез клітинних структур
Процеси транскрипції та трансляції — це перший етап на шляху формування внутрішньоклітинних структур. Наступні етапи — це збирання надмолекулярних комплексів та доставка їх до конкретних ділянок клітин. Всі етапи перетворень білкової молекули, починаючи від синтезу її рибонуклеїнової матриці до входження в склад певних компонентів клітини, пов’язані з процесами самозбирання. Саме вони і лежать в основі формування та біогенезу клітинних структур.
Самозбирання — це процес спонтанної агрегації однорідних або різних молекул, що спричинює впорядкування їх та ріст багатокомпонентних структур. Якщо відразу за самозбиранням виникають ковалентні зв’язки, то такий процес називають полімеризацією. Сам механізм цих процесів базується на слабких взаємодіях: електростатичні сили (на відстань 0,7 нм), водневі зв’язки (0,1 нм), ван-дерваальсові та гідрофобні взаємодії.
Вибірковість механізму самозбирання забезпечується наявністю у молекулі біополімерів ділянок пізнавання до відповідних молекул-партнерів. Слід пам’ятати, що самозбирання молекул може бути зворотним процесом, бо в ньому беруть участь лише слабкі зв’язки. Характер самозбирання визначається особливостями первинної структури полімеру, а також залежить від фізико-хімічних умов середовища наявності спеціалізованих молекул-регуляторів та інших факторів. Наприклад, самозбирання в біологічних системах проявляється в двошаровому розміщенні фосфоліпідів у мембранах, певній послідовності азотистих основ у нуклеїнових кислотах, у взаємодії ферменту і субстрату білка-рецептора і ефектора (наприклад, фітогормони), в формуванні ферментативних комплексів і т. д.
Слід пам’ятати, що у водному середовищі, а значить і в цитоплазмі, агрегація речовин спричинює утворення рідинно-кристалічного стану компонентів системи. Цей стан можна розглядати як четвертий стан речовини (рідинні кристали). Білки, нуклеїнові кислоти, поліцукри, ліпіди у воді утворюють такі структури, які реагують на різноманітні впливи навколишнього середовища — світло, електричне і магнітне поле, pH, тобто характеризуються властивостями, характерними і для живих клітин.
Синтезовані білки, ліпіди беруть участь в самозбиранні клітинних мембран, рибосом, мікротрубочок, мікрофіламентів, пластид та інших клітинних компонентів. Провідна роль в біогенезі клітинних мембран належить ендоплазматичному ретикулуму, який є основним місцем синтезу як мембранних білків, так і ліпідів, зокрема фосфоліпідів та гліколіпідів. Тут же відбувається біосинтез стероїдів, всіх ненасичених кислот. Саме тут синтезуються властиві рослинам Жирні кислоти — лінолева, ліноленова, арахідонова. Похідними мембран ендоплазматичного ретикулуму є мембрани вакуолі, сферосом, мікротілець і т. д. Ендоплазматичний ретикулум пов’язаний безпосередньо з ядерною оболонкою, бере участь в синтезі плазмалеми. Перехід мембрани в різні види органел дістав назву «потік мембрани». Існує уявлення про взаємодію мембранних компонентів клітини як концепцію «ендомембранної системи», згідно з якою саме потік мембран пояснює функціональну неперервність їх та участь в життєдіяльності всіх органел клітини.
Последнее обновление: 23/05/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.