БІОФІЗИКА РОСЛИН - Ю. І. Посудін - 2004
І. ФІЗИЧНІ ВЛАСТИВОСТІ РОСЛИННИХ КЛІТИН ТА ТКАНИН
4. ЕЛЕКТРОФІЗИЧНІ ВЛАСТИВОСТІ РОСЛИН
4.1. МЕМБРАННИЙ ТРАНСПОРТ
4.1.1. Види транспорту
Розрізняють такі типи транспорту (переносу) речовин крізь мембрани:
✵ пасивний транспорт, обумовлений градієнтом хімічного потенціалу (для незаряджених молекул або частинок) або градієнтом електрохімічного потенціалу (для іонів або заряджених частинок); цей вид транспорту здійснюється внаслідок дифузії через ліпідний бішар (переміщення молекул з області високої концентрації в область низької за рахунок самочинного руху) або полегшеної дифузії (транспорту, що здійснюється за допомогою переносників або каналів) і не потребує затрат хімічної енергії;
✵ активний транспорт передбачає перенос незаряджених молекул або частинок та іонів проти градієнта хімічного або електрохімічного потенціалу. Цей вид транспорту пов'язаний з енергетичними затратами.
Якщо пасивний транспорт призводить до вирівнювання градієнтів, то активний транспорт відновлює ці градієнти. Транспортні системи, що утворюють необхідний концентраційний градієнт, називаються насосами або АТФазами.
4.1.2. Осмотична рівновага
Різниця у концентраціях розчинених речовин у розчині має тенденцію зменшуватися у часі; такий тип переносу речовини, рушійною силою якого є концентраційний градієнт або градієнт хімічного потенціалу, відповідає дифузії, а кінцевий стан системи, при якому концентрація речовини однакова у всіх частинах об'єму, називається дифузійною рівновагою. Дифузія речовини (звичайно розчинника) через напівпроникну мембрану, що розділяє розчин та чистий розчинник, відповідає осмосу, а вирівнювання концентрацій по обидва боки мембрани внаслідок осмосу називається осмотичною рівновагою. Розглянемо процеси дифузії незаряджених частинок через мембрану.
Біологічна мембрана являє собою бар’єр, який характеризується селективною вибірковістю для певних іонів. Розглянемо мембрану, яка розділяє два відсіки - І та II. У відсіку І знаходиться розчинник S, а у відсіку ІІ - речовина А, розчинена у розчиннику S. Уявімо, що мембрана є проникною лише для розчинника. В такій ситуації молекули розчинника рухаються з відсіку I до відсіку II за рахунок концентраційного градієнта. Сумарному руху молекул розчиненої речовини протидіє тиск, який встановився у відсіку II. Розглянемо цей процес з позицій термодинаміки.
При переміщенні одного моля розчинника через мембрану зміна вільної енергії буде дорівнювати:
![]()
де μsII та μsI - хімічні потенціали розчинника у відсіках I і II відповідно. При рівновазі ΔG = 0.
Якщо прийняти за Xs відношення числа молів розчинника ns до загального числа молів розчинника і розчиненої речовини ns + nA, то рівняння (4.1) може бути приведене до такого вигляду:
![]()
або
![]()
оскільки XsI = 1 (розчинена речовина відсутня у відсіку І). Слід зауважити, що μs0 залежить лише від тиску. Використовуючи вираз dμg = Vdp, можна записати:
![]()
де vs -молярний об’єм розчинника.
Інтегруючи останній вираз, отримаємо:
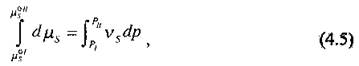
звідки:
![]()
Після підстановки рівняння (4.3) у (4.6) маємо:
![]()
де росм - осмотичний тиск.
Виразимо осмотичний тиск через концентрацію шляхом використання виразу XS = 1 - XA, де ХА - загальна молярна частка розчиненої речовини. Для розведених розчинів ХА < ХS, звідки:
![]()
З урахуванням того, що ns · vs є об’єм V розчинника, можна записати:
![]()
де CA — концентрація розчиненої речовини.
Логарифм у правій частині виразу (4.7) можна розкласти в такий ряд:
![]()
який для розведених розчинів приймає вигляд:
![]()
Таким чином, осмотичний тиск визначається виразом, який називається рівнянням Вант-Гоффа:
![]()
Завдяки концентраційному градієнту рух незаряджених частинок через мембрану супроводжується зміною вільної енергії ΔG. Якщо мембрана розділяє розчини з концентраціями СI та СIIвідповідно, то перенесення 1 моля частинок з одного розчину в інший визначається за виразом:
![]()
Осмотична рівновага настає, коли при переході одного моля цих частинок з відсіку I у відсік II зміна вільної енергії дорівнює нулю:
![]()
де μс - хімічний потенціал.
4.1.3. Іонна рівновага
Розглянемо рух заряджених частинок (іонів) через мембрану, яка розділяє два відсіки і проникна тільки для певних іонів. Якщо концентрація розчинів в обох відсіках однакова, то кількість іонів, що переходять з відсіку I у відсік II і навпаки, буде однаковою. Через це різниця потенціалів, що встановлюється на мембрані, дорівнює нулю.
Якщо концентрація розчину у відсіку I перевищує концентрацію у відсіку II, буде мати місце дифузія іонів, внаслідок якої кількість позитивних зарядів у відсіку II збільшиться. Таким чином, на мембрані встановлюється різниця потенціалів.
Отже, якщо різниця концентрацій іонів між відсіками являє собою хімічний градієнт (або хімічну різницю потенціалів), який призводить до дифузійного потоку іонів крізь мембрану з відсіку I у відсік II, то накопичення позитивних зарядів у відсіку II сприяє утворенню електричного градієнта (або електричної різниці потенціалів), який примушує іони рухатися у протилежному напрямку - з відсіку II у відсік I.
У цілому, наявність концентраційного (хімічного) і електричного градієнтів обумовлює стан електрохімічної рівноваги іонів. Різниця потенціалів, що виникає на мембрані при такому стані, називається електрохімічним (рівноважним) потенціалом.
Осмотичний тиск обумовлений зниженням хімічного потенціалу розчинника за присутності розчиненої речовини. Аналогічна ситуація має місце, коли мембрана розділяє заряджені частинки — іони. Розглянемо мембрану, що поділяє два відсіки І та II з різною концентрацією електроліту С+А- і характеризується однобічною проникністю для катіонів С+.
Перенесення 1 моля іонів з одного розчину в інший завдяки електричному градієнту за умови, що концентраційний градієнт відсутній, супроводжується зміною вільної енергії:
![]()
де z - валентність іона, F- число Фарадея (9,64846·104 Кл·моль), Δφ - різниця потенціалів на мембрані.
Для системи з двох відсіків, розділених мембраною, хімічна різниця потенціалів Δμ = μI — μII ≠ 0, якщо концентрації розчинів у відсіках різні. Втім, Δμ = 0, якщо концентрації однакові. В загальному випадку рух іонів через мембрану визначається двома градієнтами - концентраційним та електричним. Зміну вільної енергії в цьому разі подають як різницю електрохімічних потенціалів μCII — μCI.
Рівновага настає, коли при переході одного моля цих катіонів з відсіку І у відсік II зміна вільної енергії дорівнює нулю.
![]()
де μс — електрохімічний потенціал.
Електрохімічний потенціал μ враховує хімічний потенціал а та електричну роботу Аел = zFφ по перенесенню заряджених частинок:
![]()
Для випадку перенесення іонів або незаряджених частинок з відсіку І у відсік ІІ крізь мембрану зміна електрохімічного потенціалу визначається за виразом:
![]()
Умова рівноваги має вигляд:
![]()
звідки:
![]()
Припускаючи, що хімічні потенціали за відсутності розчиненої речовини та електричного поля рівні (μІ0 = μІІ0), отримуємо вираз:
![]()
Для клітинної мембрани, яка розділяє зовнішнє (Се) і внутрішнє (Сі) середовища, останній вираз можна переписати так:
![]()
Цей вираз отримав назву рівняння Нернста.
Зазвичай, різниця потенціалів між внутрішнім середовищем рослинної клітини та зовнішнім розчином, що омиває клітину, знаходяться у межах від -50 до -250 мВ (наприклад, різниця потенціалів для клітин кореневої системи Pea sativum та Avena sativa дорівнює —110 мВ та —84 мВ відповідно).
Приклад. У рослинних клітинах встановилася рівновага потоків із зовнішнім розчином, який містить по 10-3 моля іонів К+, Na- та Сl-. Внутрішня їхня концентрація становить 89·10-3, 10·10-3 та 24·10-3 моля відповідно. Визначити потенціал Нернста для кожного іона.
Розв’язання. Рівноважний потенціал визначимо за допомогою рівняння Нернста (вираз (4.22)). Підставляємо в це рівняння числові дані, враховуючи, що RT/F = 25,3 мВ (див. Додаток):

4.1.4. Мембранний потенціал
Внутрішнє і зовнішнє середовища клітини характеризуються нерівномірним розподілом певних іонів. Так, основними іонами рослинної клітини є К+ та Сl-. Завдяки різним концентраціям іонів на клітинній мембрані установлюється концентраційний градієнт. Крім того, клітинна мембрана характеризується селективною іонною проникністю, обумовленою наявністю іонних каналів. Оскільки іони несуть електричний заряд, на мембрані виникає електричний градієнт. Врешті-решт, на клітинній мембрані утворюється так званий потенціал спокою. Величина його коливається для різних клітин від - 60 до -90 мВ. Про клітину у стані спокою кажуть, що вона поляризована.
Під час дії на мембрану зовнішнього стимулу (наприклад, механічної, хімічної або електричної природи) електричний баланс порушується, що супроводжується виникненням швидкої зміни мембранного потенціалу. На мембрані встановлюється позитивний потенціал дії (близько 20-30 мВ). Цей потенціал виникає не на всій мембрані, а лише в тій ділянці, до якої був прикладений зовнішній стимул. Процес збудження мембрани, що супроводжується появою потенціалу дії, називається деполяризацією. Послідовність подій, що супроводжують появу потенціалу дії в клітині (на прикладі харових водоростей) після триразового подразнення така (рис. 4.1): точці а відповідає подразнення і швидке зростання електропровідності мембрани для іонів Сl-, яке викликає різке збільшення направленого усередину електричного струму ICl за рахунок виходу іонів Сl- і деполяризації мембрани, проміжок (а - b) характеризує продовження деполяризації мембрани з подальшим зростанням електропровідності мембрани для іонів Сl-; проміжок (b - с) означає спонтанне зменшення електропровідності мембрани для іонів К+ та струму ICl; протягом проміжку часу (а - с) відзначається вихід іонів К+ та напрямок електричного струму ІK назовні; максимум деполяризації (точка с) спостерігається, коли —ICl = +IK; після точки с ситуація повертається у вихідний стан.
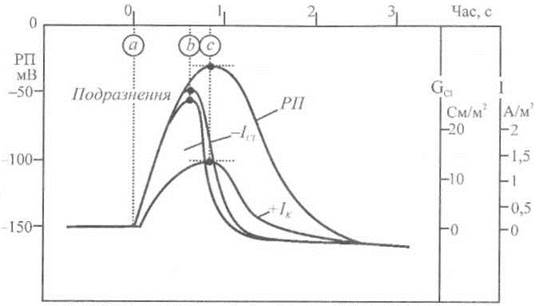
Рис. 4.1. Послідовність подій, що супроводжують появу потенціалу дії в клітині (на прикладі харових водоростей) після триразового подразнення (пояснення в тексті).
Основними властивостями мембранного потенціалу рослинних клітин є: 1) величина амплітуди у деяких рослин може досягати -170 мВ і не залежить від амплітуди зовнішнього стимулу; тривалість потенціалу дії 0,2-1 с; 2) полярність потенціалу дії протилежна полярності потенціалу спокою; 3) під час деполяризації і на початку фази реполяризації відповідна ділянка мембрани тимчасово стає незбуджуваною, несприйнятливою (рефрактерною); 4) потенціал дії поширюється по клітинній мембрані від місця збудження наче біжуча хвиля зі швидкістю від 10 м·с-1 до 170 м·с-1. Основні параметри потенціалу дії рослинних систем наведено у табл. 4.1.
Таблиця 4.1. Параметри потенціалу дії рослинних систем [Люттге, Хігінботам, 1984]
Рослинна система |
Тривалість вихідної фази, с |
Швидкість поширення, м·с-1 |
Тривалість рефрактерного стану, с |
Харові водорості, клітини міжвузля |
1 |
10-20 |
4-40 |
Mimosa |
0,5 |
20-30 |
- |
Dionaea |
0,1-0,2 |
60-170 |
0,6 |
4.1.5. Техніка вимірювання мембранних потенціалів
Електричні мембранні потенціали вимірюють за допомогою скляних мікроелектродів, виконаних з витягнутих тонких скляних трубок із зовнішнім діаметром близько 1 мкм для невеликих клітин та 2-20 мкм - для великих. Один із електродів безпосередньо занурюють у клітину за допомогою мікроманіпулятора, а інший, електрод порівняння, розташовують зовні (рис. 4.2) так, щоб можна було вимірювати різницю потенціалів. Електроди заповнені розчином КСl і являють собою сольові містки. Іони, які пересуваються через мембрану, несуть електричний заряд, завдяки чому через мембрану проходять електричні струми величиною близько 10-12 А, а на мембрані утворюється електричний потенціал. Обидва електроди з'єднані з чутливим вольтметром, який має високий вхідний опір.
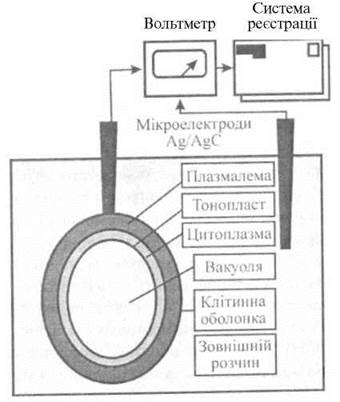
Рис. 4.2. Метод вимірювання трансмембранного потенціалу за допомогою скляних мікроелектродів.
Типові значення мембранного потенціалу клітин водоростей наведено у табл. 4.2.
Таблиця 4.2. Мембранний потенціал клітин водоростей [McRobbie, 1970]
Об’єкт |
Потенціал між вакуолею та зовнішнім розчином Евo |
Потенціал між цитоплазмою та зовнішнім розчином Ецо |
Потенціал між вакуолею та цитоплазмою Евц |
Прісноводні водорості Nitella translucens Nitella flexilis Chara corallina Hydrodictyon africanum |
-122 -155 -152 -90 |
-140 -170 -170 -116 |
+18 +15 +18 +26 |
Морські водорості Halicystis ovalis Valonia ventricosa Chaetomorpha darwinii Griffithsia Acetabularia Mediterranea |
-80 +17 +10 -55 -174 |
-80 -71 -70 -80 -174 |
±0 +88 +80 +25 ±0 |
Для більшості рослинних клітин різниця потенціалів на плазмалемі характеризується значною від'ємною величиною. На тонопласті ця різниця дорівнює нулю, або має невелике додатне значення, отже, загальний електричний потенціал між вакуолею та зовнішнім розчином - від'ємний. Техніка мікроелектродів може застосовуватися лише для великих клітин; крім того, мікроелектрод перетинає і плазматичну, і вакуолярну мембрани, що ускладнює вимірювання завдяки впливу струмів через обидві мембрани.
Ці проблеми були успішно розв'язані за допомогою петч-клемп-методу, який полягає в установленні тісного контакту відполірованого скляного мікроелектрода (мікропіпетки) діаметром 0,5-1 мкм з мембраною, що оточує ізольований протопласт (клітину, яка позбавлена клітинної оболонки). Такий тісний контакт досягався завдяки легкому всмоктуванню. Назва цієї техніки походить від англійських слів "patch" - латка, пластир (невелика область у зоні контакту мікропіпетки з мембраною) та "clamp" - скріпляти [Taiz and Zeiger, 1998]. Вимірювання проводять або з прикріпленою цілою клітиною, або лише з тією її частиною, яка залишається в отворі мікропіпетки (рис. 4.3). В останньому випадку латка розміщується у фізіологічному розчині, який оточує її ззовні та подається через піпетку. Малі діаметри мікропіпетки дозволяють вимірювати струми через окремі іонні канали. Оскільки протопласт має сферичну форму, можна виміряти його об'єм і оцінити потік зарядів через одиницю площі мембрани. Ще одна перевага методу полягає в можливості відрізняти електричні події, що відбуваються на плазматичній і вакуолярній мембранах, та контролювати склад зовнішнього і
внутрішнього середовищ.
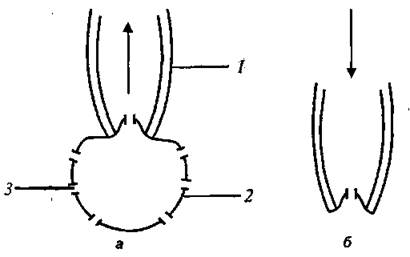
Рис. 4.3. Суть петч-клемп-методу, який полягає в установленні тісного контакту відполірованого скляного мікроелектродаз мембраною, що оточує ізольований протопласт (клітину, яка позбавлена клітинної оболонки): 1 - мікропіпетка, 2 - протопласт, 3 - іонні канали. Тут а - процес усмоктування, б - процес відриву фрагмента протопласта.
Последнее обновление: 05/02/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.