МИКРОБИОЛОГИЯ БИОЛОГИЯ ПРОКАРИОТОВ ТОМ III - А. В. ПИНЕВИЧ - 2009
ГЛАВА 18. РЕГУЛЯЦИЯ
18.4. Регуляция поведения
Термином «поведение» обозначается интегральная адаптивная реакция особи (индивидуальное поведение) или группы особей (коллективное поведение). Поскольку особью у прокариотов является клетка или трихом, все формы поведения у них так или иначе реализуются на клеточном уровне.
Регуляцию индивидуального или коллективного поведения (которое обычно узко интерпретируют как активную подвижность) принято обсуждать отдельно не только от регуляции метаболизма, но и отдельно от регуляции дифференциации и регуляции вирулентности. Мы же поступим иначе и распространим понятие «поведение» на дифференциацию и вирулентность, поскольку последние определяются условиями питания и связаны с интегративным изменением состояния клетки.
Контроль клеточной дифференциации мы уже рассматривали в разделе 17.5. Теперь остановимся на других формах регулируемого поведения, прежде всего на таксисах.
18.4.1. Индивидуальное поведение и таксисы
Общебиологический термин «таксис» (греч. taxis — расположение) означает целесообразное миграционное поведение организма по отношению к односторонне ориентированному стимулу. Иными словами, стимул может привлекать объект или вызывать у него реакцию отторжения.
Привлечение или отторжение, применительно к прокариотам, означает поиски условий, более благоприятных для роста или, во всяком случае, не угрожающих целостности клеточных структур и процессам жизнедеятельности.
Локомоторная основа такисов у прокариотов. Таксис у прокариотов носит интегративный характер и связан с самостоятельным перемещением особи (клетки или трихома), что приводит к изменению дистанции между ней и источником стимула.
Следует уточнить, что активный таксис отличается от пассивной ориентации по вектору стимула, и поэтому такой термин, как «магнитотаксис» (см. I том учебника) некорректен.
Движение при таксисах осуществляется при помощи жгутиков (у бактерий и архей) или путем скольжения (только у бактерий). Хотя у бактерий существует ряд других механизмов подвижности, например, твитчинг с помощью фимбрий IV типа (см. I том учебника), достоверными данными об их участии в таксисах мы не располагаем.
Классификация таксисов. По традиции таксисы классифицируются в соответствии со спецификой внешнего стимула. Соответственно, различают хемотаксис (таксис к химическим веществам), фототаксис (таксис к свету), осмотаксис (таксис к осмомолярности среды), гальванотаксис (таксис к источнику электрического заряда) и термотаксис (таксис к температуре). Одни из них изучены на уровне клеточных механизмов, другие только феноменологически.
Современная классификация исходит из более глубоких соображений, и таксисы подразделяются на два основных типа: не зависящие от. метаболизма (англ. metabolism-independenttaxis) и зависящие от метаболизма (англ. metabolism-dependent taxis). В первом случае внешний стимул используется только как регуляторный сигнал, который отражает состояние окружающей среды и вызывает миграционный ответ, но не влияет на метаболизм и не участвует в нем в качестве источника энергии или конструктивного субстрата. Во втором случае клетка воспринимает не стимул как таковой, а вызванное им изменение метаболизма.
Существует и третий тип таксиса, который уникален и поэтому рассматривается обособленно — это таксис, зависящий от транспорта (англ. transport-dependent taxis).
Примерами таксисов, не зависящих от метаболизма, служит хемотаксис и фототаксис.
18.4.1.1. Таксис, не зависящий от метаболизма: хемотаксис
Первооткрывателем хемотаксиса был немецкий физиолог Вильгельм Пфеффер (W. Pfeifer), который в 1883 г. обнаружил, что одни и те же химические вещества могут привлекать или отпугивать разные хемотрофные бактерии.
Начало современным исследованиям хемотаксиса у прокариотов положили пионерские работы Юлиуса Адлера (J. Adler), выполненные в конце 1960-х гг. на Е. coli К-12. В них впервые было показано, что хемотаксис непосредственно не связан с метаболизмом хемоэффектора.
Общий механизм хемотаксиса (рис. 265). Основа механизма хемотаксиса едина для бактерий и архей, независимо от типа аппарата, обеспечивающего активную подвижность, и независимо от характера стимула.
Рис. 265. Механизм хемотаксиса. Объяснение в тексте. LF — свободный лиганд; LB — связанный лиганд.
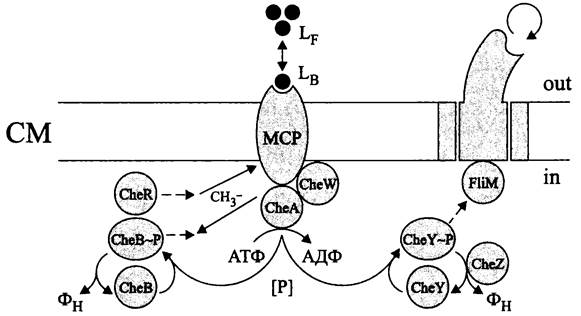
Систему хемотаксиса, наиболее изученную на примере Е. coli, кодируют шесть незаменимых генов универсальной сигнальной системы — cheA, cheB, cheR, cheW, cheY и cheZ, а также пять дополнительных генов хеморецепторов - tsr, tar, trg, tap и aer. Опероны хемотаксиса входят в состав регулона fia (сокр. англ. flagellar — жгутиковый), кодирующего и регулирующего подвижность при помощи жгутиков.
Хемотаксис позволяет сменить текущие условия роста на условия, более благоприятные. Эта цель достигается путем активного перемещения клетки либо в область с повышенной концентрацией аттрактанта, т. е. привлекающего вещества (англ. attractant; от лат. attrecto — прикасаться), либо в область с пониженной концентрацией репеллента, т. е. отпугивающего вещества (англ. repellent; от лат. repello — отталкивать).
Клетка Е. coli снабжена 6-7 жгутиковыми моторами, равномерно распределенными по оболочке. В изотропной среде роторы этих моторов периодически изменяют направление своего вращения, что делается с присущей данной бактерии базовой частотой. При вращении против часовой стрелки нити жгутиков сплетаются и вращаются вместе, в результате клетка движется поступательно. При вращении по часовой стрелке нити жгутиков расплетаются, и в результате этого клетка кувыркается на месте. При новом переходе к плаванию велика вероятность изменения ориентации продольной оси клетки по сравнению с ориентацией при последнем заплыве (см. I том учебника).
Мониторинг концентрации хемоэффекторов позволяет адаптивно изменить базовую частоту переключений мотора. При увеличении концентрации аттрактанта или уменьшении концентрации репеллента она понижается. В свою очередь, при уменьшении концентрации аттрактанта или увеличении концентрации репеллента она повышается. В итоге клетка перемещается зигзагами и дольше плывет в благоприятном направлении. Такой тип движения называется клинокинезом (англ. klinokinesis; от греч. klino — наклонять и kineo — двигать; буквально — двигаться под уклон).
Частота переключений ротора контролируется двухкомпонентной сигнальной системой, которая имеет два принципиальных отличия от классических двухкомпо нентных сигнальных систем (см. раздел 18.1.1.3).
Во-первых, регулятор не содержит ДНК-связывающего домена, а взаимодействует с мотором жгутика.
Во-вторых, гистидинкиназа не содержит сенсорного модуля, а получает сигнал от первичного сенсора — метилакцепторного белка хемотаксиса (англ. methyl-accepting chemotaxisprotein, МСР), обладающего периилазматическим сенсорным доменом для связывания лиганда-хемоэффектора, а также цитоплазматическим сигнальным доменом, который обратимо метилируется по 4-6 остаткам Glu. Таким образом, функции сенсора и гистидинкиназы выполняет не одна, а две разные молекулы, что позволяет давать унифицированный адаптивный ответ на разные стимулы.
Сигнальный домен МСР образует тройственный комплекс с гистидинкиназой CheA и «адапторным» белком-посредником CheW (рис. 265). Гистидинкиназа СhеА активируется или дезактивируется — в зависимости от баланса между' загруженностью хеморецептора и уровнем его метилирования.
Взаимодействие рецептора с лигандом приводит к быстрому ответу (~ 100 мс) на уровне жгутикового мотора. Более медленная обратная связь (~10 с) осуществляется путем деметилирования хеморецептора под контролем гистидинкиназы CheA. Этим достигается привыкание рецептора, и активность гистидинкиназы CheA возвращается на уровень, предшествовавший стимулированию. Запаздывание сенсорной адаптации по отношению к двигательному акту — не что иное, как своеобразная кратковременная память, позволяющая клетке отслеживать изменение концентрации хемоэффектора во времени, хотя она плывет в пространственном градиенте.
В центре каскада реакций фосфорилирования/дефосфорилирования находится двухкомпонентная сигнальная система CheA/CheY.
В результате связывания лиганда с рецептором цитоплазматическая гистидинкиназа CheA автофосфорилируется по остаткам His (CheA+ АТФ —> CheA~P+АДФ). За счет CheA~Pцитоплазматические регуляторы CheY и CheB трансфосфорили- руются по остаткам Asp.
Активированная форма регулятора CheY (CheY~P) теряет сродство к гистидин- киназе CheA и диффундирует к базальному телу жгутика. Там она аллостерически
активирует белок FliM, отвечающий за устойчивое вращение ротора жгутикового мотора по часовой стрелке. Нефосфорилированная форма CheY не взаимодействует с ротором.
В свою очередь, активированная форма регулятора CheB (CheB~P) играет роль метилэстеразы. Деметилированный ею хеморецептор МСР перестает активировать гистидинкиназу CheA; регулятор CheY дефосфорилируется и в такой форме уже не способен активировать белок FliM. В результате ротор жгутика начинает вращаться против часовой стрелки. Антагонистом метилэстеразы CheB~P служит метилтрансфераза CheR. Она метилирует МСР за счет универсального донора (S- аденозилметионина; см. рис. 196), и ее активность не зависит от стимула.
Чтобы быть готовыми к новому восприятию стимула, регуляторы CheY~P и CheB~P подвергаются автокаталитическому дефосфорилированию. Для ускорения дефосфорилирования более долгоживущего регулятора CheY~P дополнительно используется протеинфосфатаза CheZ, а у некоторых бактерий, например, Sinorhizobium meliloti,фосфорильная группа CheY~P сбрасывается на второй белок CheY- типа, не выполняющий функцию регулятора мотора.
Хемоэффекторы. В результате связывания аттрактанта с хеморецептором активность гистидинкиназы CheA ингибируется, а при связывании с репеллентом она стимулируется (рис. 265).
Одни лиганды напрямую взаимодействуют с сенсорными доменами МСР. Другие лиганды презентируются этим доменам периплазматическими связывающими белками, «позаимствованными» у АВС-пермеазной системы (см. II том учебника). Эти белки связывают дипептиды (англ. dipeptide binding protein; DBP), глюкозу/галактозу (англ. glucose/galactose binding protein; GBP), мальтозу/мальтодекстрины (англ. maltose/maltodextrin binding protein; MBP), рибозу (англ. ribose-binding protein; RBP) или такой репеллент, как катион Ni2+ (англ. Ni-binding protein; NiBP).
Хеморецепторы (рис. 266). Как уже отмечалось, хеморецепторы МСР, или трансдукторы (англ. transducer) состоят из двух модулей. Вариабельный N-конце- вой сенсорный модуль расположен в периплазматическом компартменте и реагирует на изменение концентрации хемоэффекторов. Консервативный С-концевой сигнальный модуль обеспечивает адаптивный ответ, сообщаясь со жгутиковым мотором через двухкомпонентную сигнальную систему CheA/CheY и адапторный белок CheW.
Рис. 266. Доменная структура хеморецептора МСР и гистидинкиназы CheА. Объяснение в тексте.
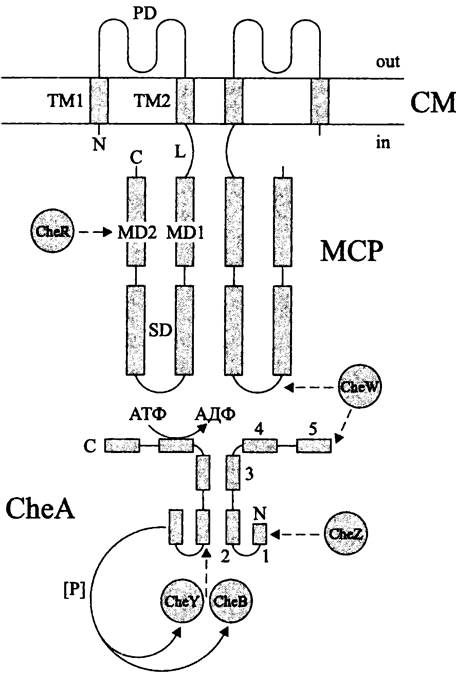
Разные объекты имеют разные наборы хеморецепторов МСР, общее число которых, согласно базам данных, достигает нескольких сотен. У отдельного объекта число генов, кодирующих хеморецепторы, варьирует в пределах от двух (Archaeoglobus fulgidus) до >20 (Pseudomonas aeruginosa), причем многие из них —это гены-пара- логи. Геномы прокариотов, неспособных к плаванию (примером служат цианобактерии), также содержат гены хеморецепторов; по-видимому, их продукты участвуют в регуляции скольжения.
Е. coli К-12 обладает простой системой хемотаксиса и использует всего лишь пять хеморецепторов: Tsr (сокр. англ. transducer for serine and repellents); Tar (сокр. англ. transducer foraspartate); Tap (сокр. англ. transducer for peptides); Trg (сокр. англ. transducer for ribose and galactose) и Aer (сокр. англ. aerotaxis and energy responses). Ее ближайший родственник, Salmonella entérica серовар Typhimurium имеет шесть хеморецепторов: Tsr, Tar, Trg, Aer, Tip (от англ. hairpin tip of Tsr — концевая шпилька цитоплазматического домена белка Tsr) и Тср (сокр. англ. taxis for citrate and phenol).
Хеморецепторы Tsr и Tip воспринимают аланин, аминоизобутират, глицин, кислород, протоны и серин (аттрактанты); Таг — аспартат, глутамат и мальтозу (аттрактанты), а также двухвалентные катионы (репелленты); Тар — дипептиды (аттрактанты); Trg — рибозу, галактозу и глюкозу (аттрактанты); Тср цитрат (аттрактант) и фенол (репеллент); Аег является сенсором редокс-состояния электрон-транспортной цепи.
Если энтеробактерии используют сравнительно узкий набор хеморецепторов, то у других прокариотов их может быть гораздо больше. В частности, у экстремально галофильного археота Halobacterium salinarium их 11 (Htrl-XI; сокр. англ. Halobacterium transducer), а у бактерии Vibrio cholerae свыше 40.
Большинство МСР имеет стандартную доменную структуру (рис. 266). На N-конце находится короткий цитоплазматический сегмент. Далее следуют первый трансмембранный домен (ТМ1), большой периплазматический сенсорный домен (PD), второй трансмембранный домен (ТМ2), линкер (L), первый домен для метилиро-
вания (MD1), высококонсервативный сигнальный домен (SD), второй домен для метилирования (MD2) и короткий С-концевой сегмент. Исключением является хеморецептор Аег, у которого сенсорный домен не периплазматический, а цитоплазматический (см. раздел 18.4.1.3). Во всех случаях сигнальный домен обеспечивает взаимодействие между первичным сенсором (хеморецептром) и вторичным сенсором (гистидинкиназой CheА).
Интересно, что взаимно гомологичные сенсорные модули хеморецепторов энтеробактерий Tsr, Таг, Тар и Trg не имеют гомологов среди других белков, в то время как сенсорный модуль хеморецептора Аег содержит широко распространенный домен PAS (см. разделы 18.3.1.1 и 18.4.1.3).
Согласно классической модели, хеморецепторы образуют димеры, в результате чего на цитоплазматической стороне мембраны образуется пучок из четырех попарно антипараллельных α-спиралей (рис. 266). С димером МСР связаны два других димера — димер адапторного белка CheW и димер вторичного сенсора, протеинки- назы CheA.
Однако, согласно последним данным, МСР объединяются в кластеры размером до 103 мономеров. По-видимому, это происходит за счет взаимодействия МСР друг с другом, а затем уже к ним присоединяются белки CheW и CheA. В неделягцихся клетках Е. coli кластеры, состоящие из смеси рецепторов, занимают терминальное положение, а в делящихся клетках — латеральное положение, с интервалом в 1/8 длины продольной оси (благодаря этому после деления они оказываются на полюсах). Физиологический смысл анизотропной сегрегации кластеров МСР еще не ясен.
Консервативные компоненты сигнальной системы. Белки CheW, CheY и CheZ содержат только по одному домену. Белок CheB имеет два домена, один из которых гомологичен CheY и получает сигнал от гистидинкиназы CheA, а другой обладает метилэстеразной активностью.
Протеинкиназа CheA состоит из доменов Р1 — Р5 (рис. 266):
— N-концевой домен Р1 обладает фосфотрансферазной активностью;
— домен Р2 используется для связывания регуляторов CheY и CheB;
— домен Р3 обеспечивает димеризацию;
— домен Р4 автофосфорилируется по остаткам Bis;
— домен Р5 является гомологом белка CheW, через него взаимодействует с сенсорным доменом хеморецептора МСР и играет роль проводника сигнала.
Домен Р1 существует в двух вариантах: основном и модифицированном. Модифицированный вариант служит для связывания протеинфосфатазы CheZ (рис. 266). Он синтезируется от альтернативного старта трансляции и имеет N-конец, укороченный на 97 а. о.
18.4.1.2. Таксис, не зависящий от метаболизма: фототаксис
Как уже отмечалось, живые организмы могут использовать свет в качестве источника энергии или в качестве стимула, дающего информацию о состоянии окружающей среды. В первом случае речь идет о фототрофии, а во втором случае — о фототаксисе.
Фототаксисом называется самостоятельное перемещение организма, ориентированное относительно пути распространения света. Различают положительный фототаксис, или движение по направлению к источнику света и отрицательный фототаксис, или движение в противоположную сторону от источника света.
В отличие от ядерных организмов с их фоторецепторными органеллами или органами, прокариоты лишены механизма, который позволил бы им определять направление на источник света. Поэтому ориентация бактерий и архей по отношению к источнику света имеет поисковый характер, т. е. осуществляется путем проб и ошибок (хотя трихомы цианобактерии Phormidium sp. каким-то образом различают «передний» и «задний» свет).
Как любой внешний стимул, видимый свет может быть не только полезным, но и вредным, в зависимости от его интенсивности и спектрального состава. Напомним, что после поглощения кванта света фотосинтетическим пигментом возбужденное состояние дезактивируется либо путем ассимиляции энергии, либо за счет флуоресценции. В противном случае избыточная энергия рассеивается в виде тепла (и тогда локальная среда вокруг молекулы пигмента за ~10-9 с нагревается до ~200°С, что может вызвать температурную денатурацию) или передается триплетному кислороду (что приводит к окислительному стрессу; см. раздел 19.1.6). Напомним и о вредном, преимущественно мутагенном воздействии дальнего ультрафиолетового света, которое благодаря фотореактивации купируется близким ультрафиолетовым светом или коротковолновым видимым светом (см. раздел 16.5.1.1). Поэтому фототаксис не обязательно связан с поисками более благоприятного светового режима и иногда наблюдается у некоторых хемогетеротрофных бактерий, в частности Isosphaera pallida.
Отрицательный фототаксис имеет не меньшее приспособительное значение, чем положительный фототаксис. В особенности важен таксис по отношению к синему свету, который поглощается соответствующими фоторецепторами. С одной стороны, это позволяет реагировать на общую интенсивность светового потока, т. е. на его потенциальную опасность. С другой стороны, обитатели водоемов, особенно глубоководные, преимущественно имеют дело с синими квантами (характерно, что наземные формы используют в качестве фоторецепторов фитохромы, поглощающие красные кванты).
Фототаксис, как и хемотаксис, позволяет сменить текущие условия роста на условия, более благоприятные. По характеру распределения стимула в пространстве градиент интенсивности света аналогичен градиенту концентрации хемоэффектора. Соответственно, прокариоты ведут мониторинг светового стимула во времени и, пользуясь фоторецепторной сигнальной системой, перемещаются путем клинокинеза.
Однако в целом влияние света на характер движения бактерий сложнее, чем влияние хемоэффекторов.
Индуцированные светом миграционные ответы клетки или популяции бывают трех типов.
Первый тип ответа — фототаксис, когда световой стимул порождает сигнал, который через двухкомпонентную сигнальную систему влияет на направление движения.
Второй тип ответа — фотокинез (от греч. kinesis — движение), когда свет, независимо от его направления, влияет на скорость движения посредством изменения активности фотосинтетического аппарата; при этом эффект может быть положительным или отрицательным. Показательно, что Теодор Энгельман (Т. W. Engelmann) считается первооткрывателем фототаксиса, поскольку он в 1883 г. описал свойство пурпурных бактерий р. Chromatium избирательно скапливаться в полосах разложенного солнечного спектра соответственно максимуму поглощения бактериохлорофилла. Однако такое поведение объясняется не фототаксисом, а фотокинезом, и оно не требует участия сигнальных фоторецепторов.
Третий тип ответа — фотофобическая реакция (от греч. phobos — страх) при внезапном увеличении или уменьшении интенсивности освещения; по-видимому, это также вызвано изменением активности фотосинтетического аппарата. В зависимости от объекта, фотофобическая реакция выражается во временной остановке движения или в изменении направления движения под углом <90° или >90°. Фотофобическая реакция может быть связана с внезапным изменением интенсивности света не только во времени, но и в пространстве, т. е. когда движущийся объект пересекает границу света и темноты. При особой форме фотофобической реакции, скотофобическом ответе (от греч. skotos — темнота и phobos — страх), объект, выйдя из освещенной зоны, резко останавливается и поворачивает назад.
В отличие от фототаксиса, второй и третий типы миграционных ответов изучены только на феноменологическом уровне; в частности, неизвестно, существуют ли фоторецепторы для фотофобической реакции.
Отличить истинный фототаксис от других миграционных ответов легче в том случае, когда сенсорная и метаболическая системы используют свет разных участков спектра. В качестве примера рассмотрим отрицательный фототаксис у экстремально галофильных архей и пурпурных бактерий.
Фототаксис у экстремально галофильных архей. Экстремально галофильный археот H. salinarium обладает способностью к положительному и отрицательному фототаксису. Для этого он использует два разных фоторецептора, которые называются сенсорными родопсинами SRI и SRII (сокр. англ. sensory rhodopsin) и в качестве хромофора содержат ретиналь.
Фоторецептор SRI (максимум поглощения в основном состоянии ~600 нм) выполняет двойственную функцию. При слабом освещении он участвует в положительном фототаксисе к зеленому свету (587 нм), а при сильном освещении - еще и в отрицательном фототаксисе к синему свету (373 нм). Фоторецептор SRII (максимум поглощения в основном состоянии ~500 нм) участвует только в отрицательном фототаксисе к синему свету.
Благодаря отрицательному фототаксису Я. salinarium покидает поверхность ярко освещенных водоемов, где высок уровень вредного ультрафиолетового излучения, и сосредоточивается в зоне доминирования зеленого света, который стимулирует биосинтез бактериородопсина.
Напомним, что помимо сенсорных родопсинов H. salinarium образует два «метаболических» ретинопротеина, создающих градиент концентрации простых неорганических ионов на уровне СМ (см. II том учебника):
— бактериородопсин (англ. bacteriorhodopsin, BR), который осуществляет светозависимый экспорт Н+ и используется как протонофорный мембранный биотрансформатор;
— галородопсин (англ. halorhodopsin), который осуществляет светозависимый импорт анионов СI-.
Наряду с фоторецепторами SRI и SRII Я. salinarium образует третий фоторецептор, батородопсин (англ. bathorhodopsin; Bat; от греч. bathis — глубокий). Его функция, а также тип его хромофора окончательно не выяснены.
Мембранный фоторецептор SRI (SRII) взаимодействует с мембранным трансдуктором HtrI (HtrII), который независимо от этого может использоваться в качестве хеморецептора при хемотаксисе.
Трансдуктор HTRI (HtrII) образует с гистидинкиназой CheA двухкомпонентную сигнальную систему, которая через регулятор ответа CheY контролирует направление вращения ротора жгутикового мотора.
При поглощении фотона фоторецептор вступает в фотоцикл продолжительностью порядка секунды, переходя из основного состояния в состояние долгоживущего интермедиата (максимум поглощения 373 нм в случае SRI и 350 нм в случае SRII). В ходе фотоцикла хромофор фоторецептора претерпевает trans-cis изомеризацию
(см. II том учебника), что приводит к изменению конформации апопротеина, а тот уже передает сигнал трансдуктору.
Фототаксис у пурпурных бактерий. Экстремально галофильные пурпурные бактерии Chromatium, salexigens, Ectothiorhospira halophila и Rhodospirillum salexigens проявляют отрицательный фототаксис к синему свету.
Фоторецептором служит растворимый фотоактивный желтый пигмент (англ, photoactive yellow pigment of E. halophila, E-PYP), который относится к группе ксан- топсинов (англ, xanthopsin; название выбрано неудачно, поскольку между растворимым E-PYP и мембранными опсинами нет структурного сходства). Апопроте- ин E-PYP (14 кДа; 125 а.о.) имеет смешанную α/β-складчатую структуру с гидрофобным карманом, в котором находится сенсорный N-концевой домен из ~50 а. о., связывающий хромофор. Согласно данным молекулярного секвенирования и рентгеноструктурного анализа с уровнем разрешения МА, этот консервативный домен можно рассматривать в качестве эволюционного прототипа сенсорных доменов суперсемейства PAS (см. раздел 18.3.1.1).
Хромофор E-PYP уникален — это 3-n-гидроксибензилпропеновая кислота (тривиальные названия: n-гидроксикоричная, n-кумаровая), которая через тиоэфирную связь присоединяется к остатку Cys-69 (рис. 267).
Рис. 267. Хромофор фотоактивного желтого пигмента РУР (3-n-гид- роксибензилпропеновая кислота) и его связь с апопротеином.
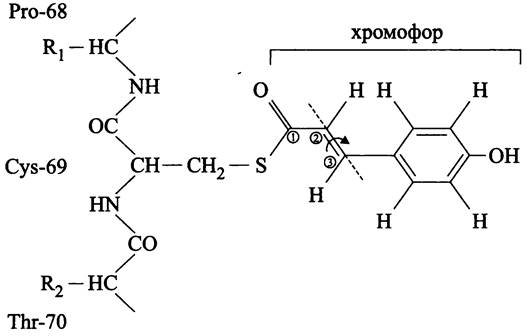
После поглощения кванта синего света E-PYP (максимум поглощения в основном состоянии 446 нм) проходит фотоцикл с двумя интермедиатами, парадоксально напоминающий фотоцикл сенсорного родопсина, несмотря на различие хромофоров. В ходе него n-гидроксикоричная кислота транс-цис изомеризуется, что вызывает конформационное изменение апопротеина и порождает сигнал, который передается гистидинкиназе Che А двухкомпонентной сигнальной системы.
Фототаксис у цианобактерий. У скользящих цианобактерий существуют два типа положительного фототаксиса — когда трихом периодически изменяет направление своего движения, в конечном счете, приближаясь к источнику света (Phormidium spp.), и когда происходит устойчивое движение к источнику света (Аnabaena sp.). Второй тип миграции описан также у беоцитов.
Механизм фототаксиса цианобактерий не выяснен. Особенно это касается фоторецепторов, обеспечивающих миграционный ответ. Хотя ретинопротеин ASR (сокр. англ. Аnabaenasensory rhodopsin), обнаруженный у цианобактерий, и гомологичен сенсорным родопсинам архей, он имеет необычные свойства — ретиналь под воздействием света не изомеризуется, а фоторецептор не проходит через фото цикл. Скорее всего, ASR используется в фоторегуляции метаболизма, например, участвует в хроматической адаптации.
18.4.1.3. Таксис, зависящий от метаболизма: энерготаксис
Жизнеспособность прокариотной клетки определяется тем, насколько последняя обеспечена энергией; при прочих благоприятных условиях от величины протонного градиента и энергетического заряда зависят клеточный рост и размножение.
Для поддержания оптимального уровня ассимиляции энергии существуют разные варианты энерготаксиса, когда бактерия воспринимает не изменение экзогенного регуляторного стимула, существенное для энергетического метаболизма, а изменение уровня самого энергетического метаболизма.
Соответственно, при энерготаксисе регуляторным стимулом служит не хемоэффектор, а скорость дыхания и уровень протонного градиента, отражающие активность использования хемоэффектора в энергетическом метаболизме.
Вариантами энерготаксиса являются:
— аэротаксис, или таксис к кислороду;
— таксис к альтернативному терминальному акцептору электронов;
— таксис к субстратам, изменяющим редокс-состояние промежуточных переносчиков дыхательной цепи;
— таксис к субстратам, восстанавливающим донорный участок дыхательной цепи.
Из всех типов энерготаксиса наиболее изучен таксис к молекулярному кислороду, или аэротаксис, при котором сенсором воспринимается не сам кислород, а редокс- состояние использующей кислород электрон-транспортной цепи.
Аэротаксис Е. coli. Аэротаксисом называется миграционный ответ на изменение скорости дыхания в результате уменьшения или увеличения концентрации кислорода в окружающей среде. Иными словами, аэротаксис направляет прокариотный организм в ту зону, где концентрация кислорода оптимальна для ассимиляции энергии.
Способность молекулярного кислорода влиять на динамическое поведение микроорганизмов впервые обнаружил Энгельман. В его опытах, относящихся к 1881 г., аэробные гетеротрофные бактерии скапливались вокруг освещенных клеток цианобактерий. Позже стало ясно, что бактерии мигрируют в зоны, где концентрация кислорода оптимальна для их роста (табл. 32).
Таблица 32. Уровни концентрации кислорода, оптимальные для отдельных групп бактерий
Экологическая группа (по отношению к кислороду) |
Вид бактерий (пример) |
O2 (мкМ) |
Облигатные аэробы |
В. subtilis |
~ 200 |
Факультативные анаэробы |
Е. coli |
~ 50 |
Микроаэрофилы |
Azospirillum brasiliense |
~ 4 |
Аэротолерантные анаэробы |
Desulfovibrio vulgaris |
~ 0, 4 |
Наконец, было показано, что при аэротаксисе бактерия предпочитает ту концентрацию кислорода, которая соответствует сродству этого акцептора электронов к главной кислородредуктазе дыхательной цепи. Характерно, что мутанты, дефектные по кислородредуктазам, одновременно теряют способность к аэротаксису.
При аэротаксисе Е. coli в качестве хеморецептора используется мембраносвязанный белок Аег (рис. 268). Его цитоплазматический С-концевой сигнальный модуль гомологичен С-концевым доменом других хеморецепторов, однако, в отличие от хеморецепторов Tsr, Таг, Таг и Trg, в нем нет сайтов для метилирования. В составе цитоплазматического N-концевого сенсорного модуля имеется PAS-домен, с которым нековалентно связан флавиновый кофактор — ФАД. Сигнальный и сенсорный модули заякорены в СМ с помощью двух трансмембранных модулей.
Предполагается, что PAS-домен белка Аег взаимодействует с хинонным пулом дыхательной цепи, в результате чего ФАДН2 обратимо окисляется. Механизм реакции неизвестен; теоретически, ФАДН2 может окисляться либо автоксидабельно, т. е. неферментативным путем, либо с помощью ФАД-зависимой сукцинатдегидрогеназы (см. II том учебника). Как регенерируется восстановленная форма ФАД, также неизвестно; скорее всего, электроны поступают от НАД(Ф)Н.
Таким образом, изменение скорости дыхания в результате уменьшения или увеличения концентрации кислорода отражается на редокс-состоянии ФАД в PAS-домене, что приводит к изменению конформации сенсорного модуля белка Аег. Изменение конформации сенсорного модуля передается сигнальному модулю, который при посредстве адапторного белка CheW активирует гистидинкиназу CheA (рис. 268).
Рис. 268. Механизм энерготаксиса. Объяснение в тексте. Сох — цитохромоксидаза; Sdh — сукцинатдегидрогеназа.
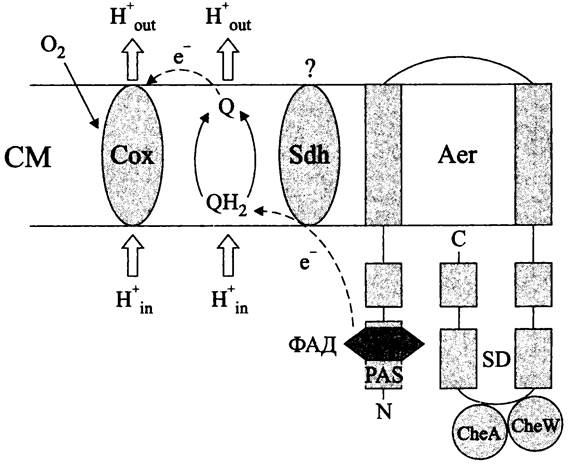
Аэротаксис у других прокариотов. Механизм аэротаксиса, изученный на примере Е. coli, не универсален. В частности, у таких разных объектов, как В. subtilis и Halobacterium, salinarium обнаружен ранее неизвестный у прокариотов тип хеморецептора — растворимый гемопротеин, соответственно, HemAT-Bs и НеmАТ-His (сокр. англ. heme-dependentaerotaxis).
N-терминальный сенсорный модуль белка HemАТ имеет небольшую степень гомологии с миоглобином, а С-терминальный сигнальный модуль на 30% гомологичен сигнальному домену хеморецептора Tsr Е. coli.
Предполагается, что связывание молекулярного кислорода гемом, находящимся в ферро-состоянии (Fe2+), вызывает конформационное изменение сенсорного модуля. В свою очередь, это влияет на активность сигнального модуля, который взаимодействует с CheA/CheW. Следует добавить, что, в отличие от хемосенсора Аег Е. coli, сенсор НеmАТ обратимо метилируется. Таким образом, гемзависимый аэротаксис по своей природе является не энерготаксисом, а хемотаксисом к кислороду.
Особая экологическая роль аэротаксиса. Энерготаксис и его главная форма, азротаксис доминируют над другими формами миграционного поведения, в частности над хемотаксисом, что можно продемонстрировать путем простого мыслительного эксперимента.
Реагируя на метаболизируемый хемоаттрактант, например, на аминокислоту, бактерии с аэробным дыхательным типом метаболизма скапливаются в одном месте, достигая плотности популяции >109 клеток • мл-1. При этом они потребляют весь имеющийся кислород и быстро оказываются в локальной анаэробной среде, что привело бы к опасному энергетическому стрессу, если бы миграционное поведение не корректировалось аэротаксисом. При первых же признаках энергетического дефицита бактерии преодолевают хемотаксис и устремляются вверх по градиенту концентрации кислорода, даже если при этом им приходится покинуть зону с более привлекательной концентрацией субстрата.
Особо важен аэротаксис там, где существует очень крутой градиент кислорода (стратифицированные микробные маты, морские «снежинки», хлопья «активного» ила очистных сооружений и т. д.; см. I том учебника).
18.4.1.4. Таксис, зависящий от транспорта
При этом уникальном таксисе миграционный ответ вызывается не экзогенным регуляторным стимулом (как при хемотаксисе или фототаксисе) и не уровнем энергетического метаболизма (как при энерготаксисе), а импортом аттрактанта, например, глюкозы или маннозы.
В данном случае рецептором внешнего стимула служит фосфотрансферазная система (см. раздел 18.3.2.2). Когда пермеаза ЕIIС переносит углевод, он одновременно с этим фосфорилируется ферментом EIIB, который получает фосфорильную группу по цепи: ФЭП —> EI —> НРr —> ЕIIА —> ЕIIВ (см. рис. 259).
Фермент EI непосредственно взаимодействует с комплексом гистидинкиназы CheA и адапторного белка CheW. При этом фосфорилированный фермент ЕI~Р служит аллостерическим активатором гистидинкиназы CheA, которая входит в состав двухкомпонентной сигнальной системы, контролирующей работу жгутика.
18.4.1.5. Другие формы таксисов
Хотя в литературе можно встретить упоминание таких форм таксисов, как гальванотаксис, осмотаксис и термотаксис, мы либо вообще не располагаем данными об их механизме, либо таких данных крайне мало.
Гальванотаксис. Гальванотаксис (англ. galvanotaxis), или активное движение по отношению к электрическому полю, был открыт немецким протистологом Максом Ферворном (М. Vervorn) в 1889 г.; по его описаниям, бактерии одних видов плыли к аноду, а бактерии других видов — к катоду.
В конце 1980-х гг. Адлер показал, что хаотичное плавание бактерий в отсутствии приложенного напряжения сменяется целеустремленной миграцией к одному из электродов, причем направление движения различается для Е. coli и Salmonella entérica серовар Typhimurium. При переключении полярности бактериия делала U- образный разворот, что указывало на существование у нее фиксированного диполя (т. е. заряд не наводился, а концы клетки имели знаки + и -). Вместе с тем, у плавающих бактерий скорость перемещения к электродам была на порядок выше, чем у бактерий, лишенных самостоятельной подвижности, т. е. эффект нельзя было объяснить электрофорезом.
Механизм гальванотаксиса до сих пор не понят; не исключено, что на самом деле наблюдаются не гальванотаксис, а гальваноориентация, т. е. клетки занимают положение вдоль силовых линий электрического поля (по аналогии с «магнитотаксисом»), но не реагируют на его градиент.
Осмотаксис. Осмотаксис. (англ. osmotaxis), или активное продвижение в область с оптимальной водной активностью, или с оптимальной осмомолярностью среды, впервые описал французский бактериолог Maccap (J. Massart) в 1889 г.
В конце 1980-х гг. Адлер установил, что клетки Е. coli активно перемещаются в раствор оптимальной осмомолярности (~0,2 М рибитола или сахарозы) и избегают чистой воды, причем используемый осмоаттрактант не являлся хемоаттрактантом или хеморепеллентом. Механизм осмотаксиса остается загадкой.
Термотаксис. В отличие от гальванотаксиса и осмотаксиса, термотаксис (англ. thermotaxis), или перемещение и сосредоточение бактерий в пространственном градиенте температуры, действительно существует, и его механизм изучен.
В опытах, проведенных на Е. coli, показано, что в основе термотаксиса лежит тот же самый механизм, который определяет хемотаксис (см. раздел 18.4.1.1). Если градиент стимула отсутствует, плавание чередуется с кувырками, но, когда он появляется (например, 19° —> 39°С), клетки воспринимают его с помощью рецепторов и изменяют частоту кувырков таким образом, чтобы обеспечить перемещение в область с благоприятной температурой (30°С). Как правило, умеренное повышение температуры способствует плаванию, а ее уменьшение вызывает кувырки. Первичными рецепторами температуры, как и при хемотаксисе; служат трансдукторы Tsr и Таг; термоадаптация осуществляется путем изменения уровня метилирования этих рецепторов.
В отличие от мезофилов, термофильная бактерия Thermotoga maritima проявляет негативный таксис к повышенной температуре и чаще кувыркается во всем интервале стимула, при котором сохраняется активная подвижность. Кроме того, эта бактерия не содержит гомологов MCP-белков, т. е. механизм термотаксиса у нее иной, чем у Е. coli.
18.4.2. Коллективное поведение на основе внутрипопуляционной коммуникации
Регуляция коллективного поведения требует взаимного обмена сигналами. В случае прокариотов такой обмен изучен только у бактерий на примере химических сигналов; использование других сигналов, например, звуковых волн, принципиально возможно, но достоверно не доказано.
Химический сигналинг и феромоны (общие сведения). Все организмы в той или иной степени используют химические агенты в качестве регуляторных сигналов. С их помощью многоклеточные ядерные существа общаются друг с другом, а также обмениваются информацией внутри своего тела на органном, тканевом и клеточном уровнях. В случае протистов и прокариотов химическими сигналами общаются между собой клетки одного или разных видов.
Обособленный класс сигнальных молекул составляют феромоны (от греч. pherein — переносить и hormon — возбуждать). Этот термин был предложен в 1959 г. Карлсоном (Р. Karlson) и Люшером (М. Liischer) для обозначения биологически активных веществ, которые выделяются организмом в окружающую среду и вызывают специфический ответ у другого организма того же вида. Феромоны принципиально отличаются от гормонов, которые секретируются во внутреннюю среду организма, обеспечивая связь между его отдельными частями.
Автоиндукторы (общие сведения). Феромоны прокариотов обычно называют автоиндукторами (англ. autoindncer). Эти диффундирующие низкомолекулярные соединения имеют три основные особенности: (1) они воздействуют извне на самого продуцента; (2) их активность требует пространственного сосредоточения многочисленных особей, т. е. она проявляется в зависимости от плотности популяции; (3) они могут служить средством не только внутривидового, но и межвидового общения.
Таким образом, автоиндукторы образуются популяцией клеток, выделяются в окружающую среду, а затем воспринимаются рецепторными системами продуцентов. Важно подчеркнуть, что в большинстве случаев это не генеральные метаболиты и не неспецифические побочные продукты жизнедеятельности, а специализированные метаболиты, которые служат сигнальными молекулами для межклеточного общения. Они образуются в ответ на изменение условий окружающей среды в определенной фазе роста, накапливаются снаружи клеток, распознаются специфическими рецепторами и вызывают координированный ответ по достижении концентрации 10-12-10-9 М. Добавим, что такой ответ выражается в изменении поведения, а не в детоксикации автоиндуктора и не в использовании его в качестве питательного субстрата.
Чувство кворума. Автоиндукторы проявляют свою активность, начиная с пороговой концентрации, что возможно только при достижении определенной плотности популяции. Поэтому по предложению Фукуа (W. С. Fuqua), высказанному в 1994 г., коллективная реакция бактерий на автоиндуктор была названа чувством кворума (англ. quorum sensing, QS). Концентрация автоиндуктора отражает концентрацию клеток, и начало его восприятия свидетельствует о достижении минимально необходимой численности, или кворума, что позволяет принять коллективное решение, в данном случае в форме того или иного адаптивного ответа. Чувство кворума позволяет особи, входящей в состав популяции, адаптироваться к изменению внеш-
них условий, воспринимая внешний сигнал, суммирующий индивидуально генерируемые внешние сигналы.
Функции, контролируемые с помощью автоиндукторов при появлении чувства кворума. Автоиндукторы влияют на экспрессию генов адаптивного ответа, а также на транскрипцию генов, которые отвечают за их собственный синтез и восприятие. С помощью QS-систем контролируются:
— вирулентность Agrobacterium tumefaciens, Pseudomonas aeruginosa и Vibrio spp.;
— биолюминесценция V. fisheri и V. harvey;
— синтез антибиотиков Photorhabdus luminescens;
— образование экзотоксина Clostridium perfringens;
— образование биопленок P. aeruginosa;
— приобретение состояния компетентности при генетической трансформации В. subtilis и Streptococcus pneumoniae;
— дифференциация эндоспор В. subtilis, а также дифференциация цист миксо- бактерий и цианобактерий;
— переход к стационарной фазе роста В. subtilis.
Благодаря чувству кворума, возникающему с помощью автоиндукторов, бактерии проявляют функции, целесообразные в коллективном исполнении, или решают проблемы, вытекающие из перенаселения локальной ниши. Ярким примером служит образование факторов вирулентности, которые часто обладают антигенными свойствами и распознаются иммунной системой хозяина. Целесообразно отложить образование этих факторов до того момента, когда популяция приобретет достаточно большой размер, что позволит избежать тотального уничтожения иммунной системой.
Разнообразие автоиндукторов и QS-систем (рис. 269). Чувство кворума, которое первоначально считалось свойством только некоторых морских светящихся вибрионов, в настоящее время продемонстрировано у двух десятков родов грамотрицательных бактерий, а также у некоторых грамположительных бактерий. В настоящее время описаны три основных типа QS-систем.
QS-система первого типа характерна для грамотрицательных бактерий (рис. 269, А). В большинстве случаев в ней используются автоиндукторы типа I (AI-1), или N-ацилированные лактоны гомосерина (англ. N-acylhomoserine lactone, AHL).
Рис. 269. QS-системы, обеспечивающие чувство кворума. А — у большинства грамотрицательных бактерий; Б — у грамположительных бактерий; В — у Vibrio harvey.
Объяснение и тексте.
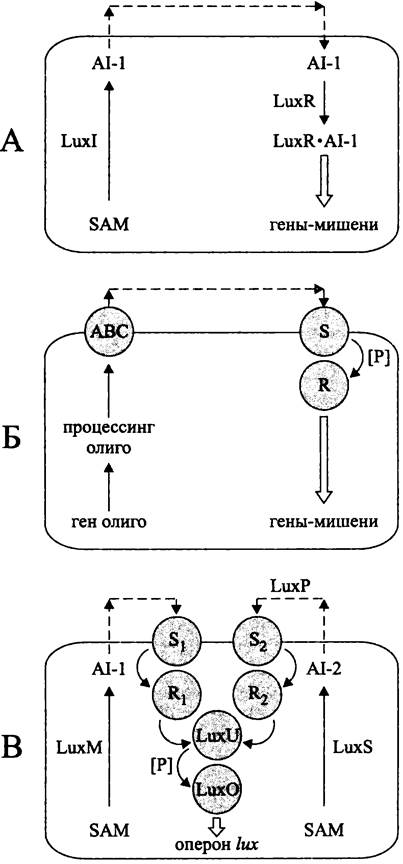
N-ацильные цепи AHL содержат четное, реже нечетное число атомов углерода (4-14), бывают насыщенными или ненасыщенными, а также могут содержать 2-кето- или 2-оксогруппы; при синтезе автоиндуктора эти цепи поступают от ацилированного ацилпереносящего белка (англ, acyl-carrier protein, АСР; см. II том учебника) или от ацил-СоА.
AHL образуются с помощью синтаз LuxI или LuxM, диффундируют в окружающую среду, а затем пассивно, по градиенту концентрации проникают обратно в клетку, где связываются с однокомпонентным сенсором — активатором транскрипции LuxR, который содержит N-концевой сенсорный модуль и С-концевой регуляторный модуль. LuxR может на время связаться с клеточной мембраной, но после активации он димеризуется и переходит в цитоплазму, где взаимодействует с ДНК.
Более редкими формами автоиндукторов у грамотрицательных бактерий являются циклические дипептиды (дикетопиперазины) у ряда псевдомонад и энтеробактерий, 2-гептил-3-гидрокси-4-хинолон у Pseudomonas sp., а также метиловый эфир 3-гидроксипальмитиновой кислоты у Ralstonia solanacearum.
QS-система второго типа характерна для грамположительных бактерий (рис. 269, Б). В данном случае автоиндукторами являются олигопептиды. Они синтезируются в виде предшественника, который подвергается протеолитическому процессингу, а затем секретируется в окружающую среду с помощью АВС-транспортера (см. II том учебника). На эти индукторы реагирует двухкомпонентная сигнальная система.
У патогенной бактерии S. pneumoniae роль автоиндуктора выполняет сигнальный пептид компетентности (англ. competence signaling peptide, CSP). Он имеет размер ~17 а. о. и образуется в результате посттрансляционного процессинга полипептида-предшественника СоmС (сокр. англ. competence).
CSP экспортируется с помощью секреторного аппарата СоmАВ, накапливается во внеклеточной среде, связывается с рецептором ComD и при посредстве гистидинкиназы СоmЕ активирует регулон компетентности сот.
Продуктом этого регулона является альтернативный сигма-фактор СоmХ, который, в свою очередь, активирует >100 генов. «Ранние» гены comABCDE отвечают за синтез CSP, в то время как «поздние» гены отвечают за образование биопленок, а также кодируют автолизин и бактериоцины. Эти ферменты вызывают лизис субпопуляции клеток с высвобождением их ДНК, которая затем поглощается нелизировавшимися компетентными клетками.
Возможно и одновременное использование сразу двух пептидных автоиндукторов. Например, В. subtilis образует автоиндукторы СоmХ и CSF (сокр. англ. competence and sporulationfactor). При посредстве гистидинкиназы ComP они регулируют активность транскрипционного фактора СоmА (не путать с субъединицей транспортера СоmАВ у S. pneumoniae), отвечающего за чувство кворума и приобретение компетентности. В то время как автоиндуктор СоmХ в основном обеспечивает чувство кворума, автоиндуктор CSF, в зависимости от его концентрации, активирует или подавляет СоmА, а также стимулирует споруляцию.
QS-система третьего типа имеется у светящейся бактерии Vibrio harvey (рис. 269, В). В ней одновременно участвуют два разных автоиндуктора. Как и другие грамотрицательные бактерии, V. harvey образует автоиндуктор AI-1, однако он распознается не однокомпонентной, а двухкомпонентной сигнальной системой — как у грамположительных бактерий. Второй автоиндуктор, AI-2 образуют очень многие грамотрицательные и грамположительные бактерии, используя при этом тиогидролазу LuxS. Стандартная химическая структура данного автоиндуктора позволяет предположить, что он играет роль «универсального» сигнала при межклеточном общении бактерий, принадлежащих к разным видам. Автоиндуктор AI-2 диффундирует в окружающую среду, а затем в виде комплекса с периплазматическим связывающим белком LuxP распознается двухкомпонентной сигнальной системой. Сигналы, поступающие от независимых двухкомионеитных систем, специфичных по отношению к автоиндукторам AI-1 и AI-2, интегрируются с помощью фосфореле LuxU/LuxO, и таким путем контролируется экспрессия генов оперона люциферазы lux (см. II том учебника).
Биосинтез автоиндукторов AI-1 и AI-2 (рис. 270). Большинство автоиндукторов представляет собой AHL; они обладают гидрофобными свойствами и покидают клетку путем простой диффузии. В то же время, для экскреции гидрофильных автоиндукторов олигопептидной природы используются специальные системы экспорта.
Исходным материалом при синтезе автоиндукторов AI-1 и AI-2 служит S-аденозилметионин (англ. S-adenosylmethionine, SAM; см. рис. 196).
Рис. 270. Биосинтез автоиндукторов AI-1 и AI-2. SAM — S-аденозилметионин; Luxl — синтаза; АСР —ацилпереносящий белок; МТА — метилтиоаденозин; Pfs — нуклеозидаза; ade —аденин; MTR — метилтиорибоза; МТ — метилтрансфераза; SAH — S-аденозилгомоцистеин; ТН — тиогидролаза; А — аденозин; hom — гомоцистеин; SRH — S-рибозилгомоцистеин; LuxS — гидролаза; DPD — 4,5-ди- гидрокси- 2,3-пентандион.
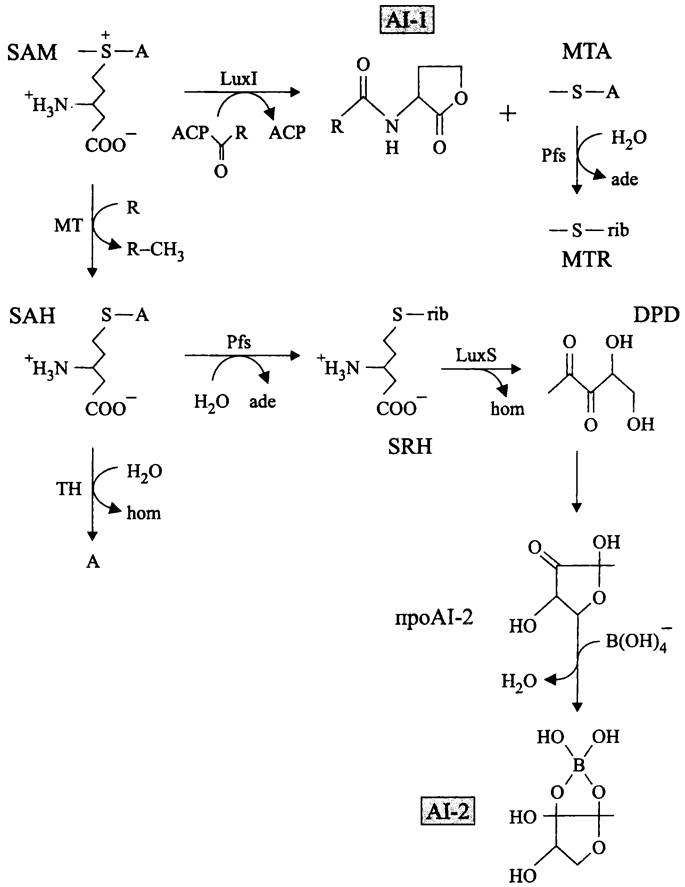
Автоиндуктор AI-1 образуется из SAM за один этап, с помощью синтазы Luxl. Донором жирнокислотного остатка для AHL, как правило, является ацилпереносящий белок. В качестве побочного продукта образуется токсичный метилтиоаденозин (англ. methylthioadenosine, МТА), который гидролизуется 5'-метилтиоаденозин/S- аденозилгомоцистеин-нуклеозидазой Pfs с образованием аденина и метилтиорибозы (англ. methylthioribose, MTR).
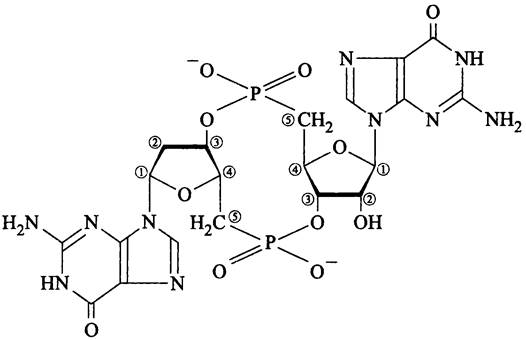
Рис. 271. Бис-(3'-5')-цикло-ди-ГМФ (циклический ди-ГМФ).
Автоиндуктор AI-2 образуется из SAM в пять этапов. Напомним, что SAM используется в качестве универсального донора метильной группы при модификации нуклеиновых кислот и белков (см. разделы 16.5.2 и 18.4.1.1). Под воздействием метилтрансферазы он превращается в токсичный интермедиат S-аденозилгомоци- стеин (англ. S-adenosylhomocysteine, SAH), который расщепляется тиогидролазой с образованием аденозина и гомоцистеина. Другим путем детоксикации SAH и, одновременно с этим, вторым этапом на пути синтеза автоиндуктора становится гидролиз нуклеозидазой Pfs с образованием аденина и S-рибозилгомоцистеина (англ. S-ribosylhomocysteine, SRH). На третьем этапе SRH расщепляется тиогидролазой LuxS на гомоцистеин и рибозильную часть, преобразованную в 4,5-дигидрокси-2,3- пентандион (англ. 4,5-dihydroxy-2,3-pentanedione, DPD). Ациклический DPD нестабилен и спонтанно циклизуется с образованием смеси фуранозных продуктов, одним из которых и является проАI-2. На завершающем этапе проАI-2 взаимодействует с тетрагидроксидом бора с образованием фуранозилборатного диэфира; неизвестно, происходит эта реакция спонтанно, или она катализируется белком LuxP.
Связь сигналинга посредством автоиндукторов с сигналингом посредством цикло-ди-ГМФ. Как правило, QS-системы действуют совместно с альтернативными сигма-факторами (в частности, это происходит при переходе Е. coli к стационарной фазе), а также совместно с глобальными транскрипционными факторами. Наряду с автоиндукторами могут также использоваться другие сигнальные молекулы — циклические нуклеотиды.
У фитопатогена Xanthomonas campestris восприятие автоиндуктора, цис-11-метил-2-додеценовой кислоты осуществляется двухкомпонентной сигнальной системой RpfC/RpfG и сопровождается гидролизом цикло-ди-ГМФ.
Бис-(3'-5')-цикло-ди-ГМФ, или цикло-ди-ГМФ (рис. 271) был впервые описан Бензименом (M.Benziman) в 1987 г. в качестве аллостерического регулятора синтазы целлюлозы у Gluconacetobacter xylinum. Позднее было выяснено, что белок PleD, обладающий гуанилатциклазной активностью, активируется при переходе швермеров Caulobacter crescentus к сидячему образу жизни (см. раздел 17.1.4).
В настоящее время общепризнанно, что у бактерий цикло-ди-ГМФ — это крайне важная и практически универсально распространенная сигнальная молекула, которая контролирует на уровне транскрипции такие функции, как клеточная дифференциация, агрегация и адгезия, а также образование биопленок и вирулентность.
Содержание цикло-ди-ГМФ определяется соотношением скоростей образования и распада этого соединения под воздействием, соответственно, дигуанилатциклазы и фосфодиэстеразы. Белки, проявляющие обе активности, обладают консервативными доменами GGDEF (Gly-Gly-Asp-Glu- Phe), EAL (Glu-Ala-Leu) и HD/GYP (His-Asp/Gly-Tyr-Pro). Большинство из них также содержит сенсорный модуль с PAS-доменом, благодаря чему они сопрягают внешние стимулы с ответом на транскрипционном или физиологическом уровне, а в качестве аллостерического регулятора используется цикло-ди-ГМФ.
* * *
На этом мы заканчиваем главу, посвященную регуляции, хотя не окончательно расстаемся с этой многогранной темой. В дальнейшем, говоря об экологических стрессах, симбиозах и популяционных явлениях, мы будем неоднократно возвращаться к вопросам регуляции метаболизма и поведения.