Фізіологія рослин - Мусієнко М.М. 2001
Водний режим рослин
Молекулярна структура та фізичні властивості води
Вода — єдина речовина на землі, яка одночасно і в великій кількості зустрічається в рідкому, твердому та газоподібному станах.
В рідкому стані вода поряд з простими молекулами має і більш складні асоціати (Н2О)n. Саме ця здатність води і зумовлює характерні специфічні особливості води.
Молекула води складається з атома кисню та двох атомів водню. Водень має позитивно заряджене Ядро (протон) та єдиний від’ємно заряджений електрон (рис. 21).
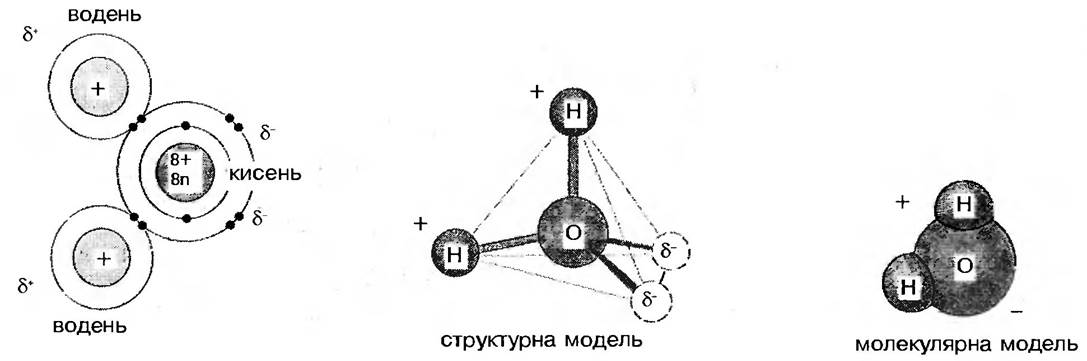
Рис. 21. Структура молекули води
Атом кисню містить 8 протонів та 8 електронів. На його внутрішній та зовнішній орбітах обертаються відповідно 2 та 6 електронів. До стійкої 2-електронної зовнішньої оболонки водню не вистачає одного електрона, а 8-електронної кисню — два, завдяки чому між ними існує спорідненість. В молекулі води це виражається утворенням двох -О-Н зв’язків. Центр молекули води — ядро кисню, а під кутом близько 105° розташовані ядра атомів водню (рис. 22). Зміщення атомів водню на один бік від атому кисню зробило молекулу води полярною, а значить, електрично активною.
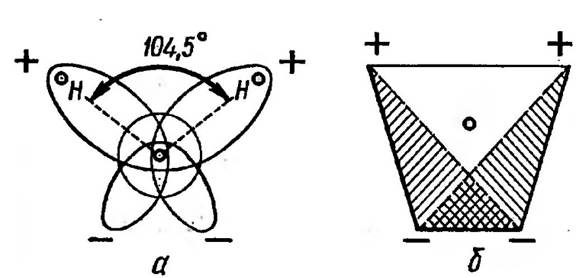
Рис. 22. Полярність молекули води
В молекулі води на атомах водню зосереджено надлишковий позитивний заряд, тоді як на двох нерозділених атомах кисню — від’ємний. Тому в цілому молекула води є диполем (диполь від грецького — два полюси). Отже, диполь — це сукупність двох точкових електричних зарядів, однакових за величиною та протилежних за знаком. Притягання таких зарядів зумовлює виникнення водневих зв’язків між молекулами води:
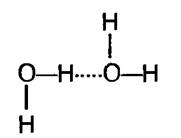
Це відносно слабкий зв’язок, так як в рідкій воді енергія, необхідна для його розриву становить 18,84 кДж на моль (для порівняння енергія ковалентного зв’язку Н-О- в моле-
кулі води складає 460,4 кДж на моль). Водневі зв’язки постійно виникають та руйнуються. Через те, що в молекулі води електрони міцніше зв’язуються з атомами кисню, відбувається відщеплення протонів, тобто ДИСОЦІАЦІЇ води на іони водню (Н+) та гідроксилу (ОН ). При 25° С концентрація водневих іонів в чистій воді становить 1x107 моль на літр, що відповідає pH 7. Кожна молекула води може бути зв’язана 4 водневими зв’язками з відповідне 4 сусідніми молекулами, в результаті виникає пентагональна структура.
Згідно з сучасними уявленнями, в основі будови води лежить впорядкована структура, що являє собою кристалічну решітку, з розмитою тепловим рухом частинок: молекул води.
Квазікристалічна (квазі — уявна, не справжня) структура води є головною ознакою, за якою її відрізняють від інших рідин. Структурні особливості води як в твердому (рис. 23), так і в рідкому (рис. 24) станах визначають унікальні властивості її.
Так, універсальність води як розчинника зумовлена полярністю її молекул та здатністю утворювати водневі зв’язки. Розчинення кристалів неорганічних солей відбувається завдяки гідратації іонів таких солей.
Добре розчиняються у воді також органічні речовини, з карбоксильними, гідроксильними і іншими групами в яких вода утворює водневі зв’язки.
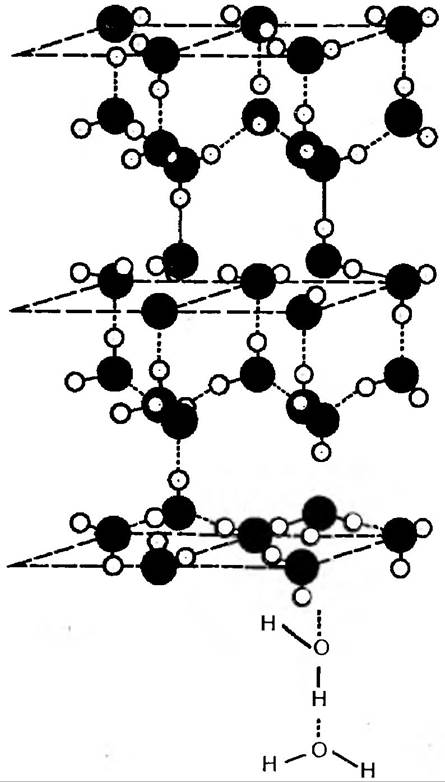
Рис. 23. Розташування водневих зв язків між молекулами води в просторовій гратці льоду. Внизу — направленість водневого зв'язку
Фізіологічна роль води визначається насамперед фізичними властивостями її.
Вода — найбільш аномальна речовина, хоча і прийнята за еталон міри густини (щільності) та об’єму для інших рідин. Всі речовини збільшують свій об’єм при нагріванні, зменшуючи при цьому свою густину (щільність). Однак при тиску в 1 атм. (0,1013 МПа) у води в проміжку від 0 до 4 °С при підвищенні температури об’єм зменшується і максимальна густина її спостерігається при 4 °С (за такої
температури 1 см3 води має масу 1 г, а густина дорівнює 1). Ця властивість води, в силу якої найбільшої густини вона досягає при 4 °С і в міру подальшого охолодження уже не стискується, а розширюється, має вирішальне значення для життя організмів у різних водоймах, так як в іншому випадку вся вода в них охолола б до 0 °С і перетворилась в лід. Завдяки такій аномалії води при охолодженні водойм її густина на поверхні підвищуються, так як першими охолоджуються поверхневі її шари. Охолоджені шари води, як більш важкі, спускаються вниз до тих пір, доки Температура води на всій глибині не досягне межі густини, тобто 4 °С. При подальшому охолодженні вода стає легшою і тому не опускається на дно, тобто не перемішується з глибинними шарами, захищаючи їх від охолодження до більш низької температури. При 0 °С водойма вкривається льодом. Під час замерзання об’єм води різко зростає, а під час таненні льоду так же різко зменшується. Об’ємні зміни води — найважливіший фактор впливу на материнські породи в процесі формування грунту. Вона здатна розвивати тиск до 2400 атмосфер, чим руйнує гірську породу.
Наявність водневих зв’язків приводить до підвищення температури кипіння і теплоти випаровування за рахунок додаткової енергії, необхідної для розриву або зміни їх.
Результатом наявності водневих зв’язків є такі аномалії води в порівнянні з іншими рідинами, як досить висока температура кипіння (100 °С), найбільша в порівнянні з усіма іншими рідинами, а також і твердими тілами питома теплоємність. Величина теплоємності води (тобто кількість тепла, що необхідно для підвищення температури на 1 °С) в 5-10 разів вище, ніж у інших речовин. Температура кипіння води зростає при підвищенні тиску, а температура плавлення (замерзання, яка у води 0 °С) — падає.
Висока теплоємність води захищає рослини від різкого підвищення температури при підвищенні температури повітря, а висока теплота пароутворення (2,3 кДж на 1 г) забезпечує терморегуляцію організмів.
Вода володіє виключно високим поверхневим натягом за рахунок потужних сил зчеплення (когезії) між її молекулами; вище поверхневий натяг лише у ртуті. Для води характерна також властивість прилипання (адгезії), яка проявляється при підніманні її проти гравітаційних сил наприклад, в тканинах дерев. Різко виражена здатність до адгезії має важливе значення при взаємодії води з іншими компонентами клітини.
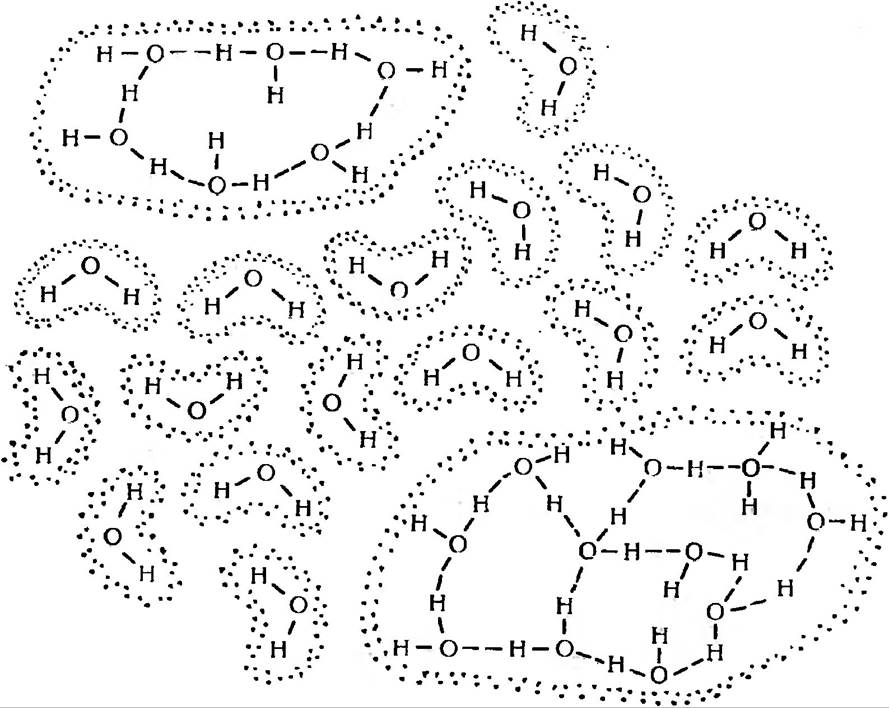
Рис. 24. Модель кластерноі структури рідкої води
Вода має також високу теплопровідність (перенесення енергії від більш нагрітих ділянок тіла до менш нагрітих, внаслідок теплового руху і взаємодії мікрочастинок), що дає їй змогу випаровуватися навіть при 0 °С.
До розряду найважливіших властивостей належить також і відома здатність води розчиняти гази.
Завдяки переліченим унікальним фізико-хімічним властивостям вода і виявилась найбільш придатним внутрішнім середовищем для всіх живих організмів, в тому числі і для рослин.
Для вивчення багатьох процесів водного обміну рослин, в тому числі для досліджень поглинання і пересування води, проникності мембран, досить широко використовують мічену (Ізотопну) воду. При цьому як індикатори використовують стабільний ізотоп водню — дейтерій (D), радіоактивний ізотоп— тритій (Т), а також воду помічену стабільним ізотопом кисню 18О.
Дейтерій — важкий водень, стабільний ізотоп водню з масовим числом 2 (D або 2Н). Ядро атома (дейтрон) складається із протона і нейтрона. З киснем утворює важку воду (D2О). Важка вода (D2O) присутня в незначній кількості (приблизно 0, 015%) в річках, озерах, морях.
Радіоактивний ізотоп водню — тритій (Т, 3Н), важкий бета-радіоактивний ізотопводню з масовим числом 3. Ядро атома складається із протону і двох нейтронів.
Стабільний ізотоп кисню 18О в природі складає лише 0, 003% відносно 16О.
Суть ізотопного методу полягає в тому, що до звичайної води, яка використовується для вивчення водного обміну рослин, додається ізотопна вода. Через певні проміжки часу відбирають проби води із досліджуваних частин рослин і визначають вміст ізотопів. На основі одержаних даних можна судити про швидкість надходження води в рослину та її пересування, проникність клітинних мембран, швидкість обміну води в клітинах та інше.
Последнее обновление: 23/05/2024
Редакционная и учебная адаптация: Данный материал сведен на основе первоисточника/оригинального текста. Команда проекта осуществила редакционную обзорную обработку, исправление технических неточностей, структурирование разделов и адаптацию содержания к учебному формату.
Что было обработано:
- устранение форматных дефектов (OCR-ошибки, разрывы структуры, дефектные символы);
- редакционное упорядочивание содержания;
- унификация терминов в соответствии с академическими источниками;
- проверка соответствия фактических утверждений текста первоисточнику.
Все упоминания об авторе, годе издания и происхождении первичного текста сохранены в соответствии с источником.